Clear Sky Science · ar
تعديل m6A الوسيط بواسطة METTL3 ينظم CDKN1A للحد من تضرر الإدراك واستماتة الخلايا العصبية الناجمة عن الحرمان المزمن من النوم في الفئران
لماذا قد تضر الليالي السهر بذاكرتك
يتجاهل كثير من الناس فقدان النوم المزمن باعتباره جزءاً طبيعياً من الحياة الحديثة، لكن الأبحاث تكشف أن الحرمان من النوم يمكن أن يضر بصمت بمناطق الدماغ المسؤولة عن التعلم والذاكرة. تتعمق هذه الدراسة في الفئران إلى مستوى الجزيئات داخل خلايا الحُصين وتحدد مفتاحاً كيميائياً محدداً — يُسمى METTL3 — يبدو أنه يحمي الخلايا العصبية من الآثار الضارة للحرمان المزمن من النوم. فهم هذا المفتاح قد يشير في المستقبل إلى طرق جديدة لحماية الذاكرة لدى الأشخاص الذين لا يستطيعون تجنب فقدان النوم بسهولة، مثل العاملين بنوبات، ومقدمي الرعاية، والمرضى الذين يعانون اضطرابات النوم.
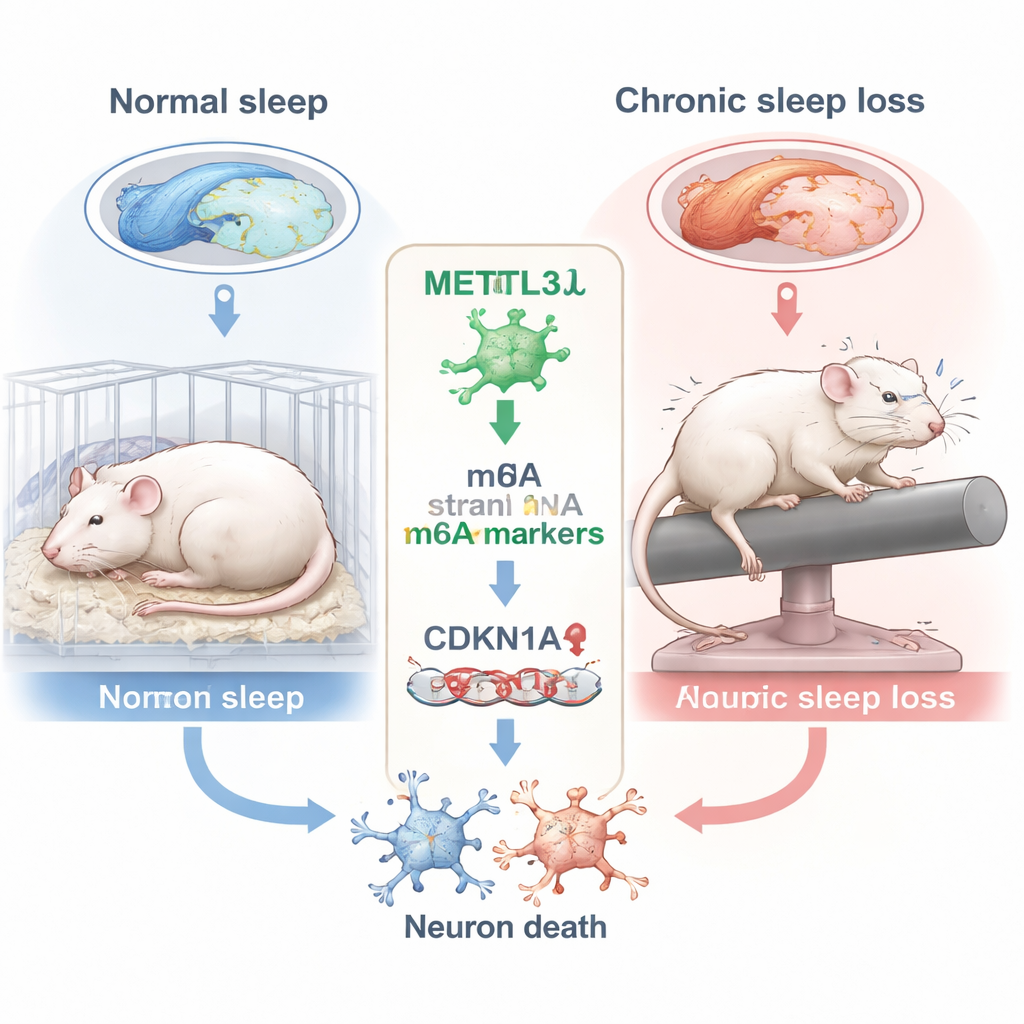
كيف يضر فقدان النوم طويل الأمد بمركز الذاكرة
ركز الباحثون على الحُصين، المنطقة الدماغية ذات الشكل الشبيه بالفرس النابح والتي تعد أساسية لتشكيل الذكريات الجديدة. داخل الحُصين ركزوا على منطقة فرعية تُسمى CA3، التي تساعد في ترميز واسترجاع المعلومات المكانية — مهارات تُختبر بمهام مثل العثور على منصة مخفية في الماء. أبقيت الفئران مستيقظة لمدة 10 ساعات يومياً على مدار ستة أسابيع باستخدام قضيب دوّار لطيف يوقظها مراراً. عند اختبار ذاكرتهم في متاهة موريس المائية المعروفة، سلكت الفئران المحرومة من النوم طرقاً أقل مباشرة، عبرت موقع المنصة السابق مرات أقل، وقضت وقتاً أقل في الربع الهدف، وهي كلها علامات على ضعف الذاكرة المكانية مقارنة بالحيوانات التي نالت قسط الراحة.
علامة كيميائية على الحمض النووي الريبي تختفي
لفهم ما كان يحدث داخل خلايا CA3، حلل الفريق علامة كيميائية على الحمض النووي الريبي تُسمى m6A، وهي واحدة من أكثر العلامات الداخلية شيوعاً على الرنا الرسول. تساعد هذه العلامات في التحكم في مدة بقاء جزئيات الرنا وكيفية استخدامها لإنتاج البروتينات. إنزيم رئيسي يضيف علامات m6A هو METTL3. باستخدام تسلسل m6A عالي الإنتاجية وتحليل التعبير الجيني، وجد العلماء أن الحرمان المزمن من النوم خفّض بشكل كبير مستوى METTL3 في منطقة CA3. تم تأكيد هذا الانخفاض على مستوى الرنا والبروتين. نمط الجينات المتأثرة أشار إلى اضطرابات في التحكم بدورة الخلية واستجابات الإجهاد، مما يوحي بأن فقدان النوم قد يدفع الخلايا العصبية نحو حالات غير صحية.
من التغيير الجزيئي إلى موت الخلايا العصبية
لمعرفة كيف قد يؤثر خفض METTL3 مباشرة على الخلايا العصبية، لجأ الباحثون إلى خلايا حُصينية فئرية نمت في أطباق. عندما استخدموا حمضيات رنوية متداخلة صغيرة لإسكات METTL3، أصبحت الخلايا أكثر عرضة بكثير للعلاج المؤذي برابامايسين، وهو دواء يجهد الخلايا العصبية. أظهرت هذه الخلايا المنقوصة من METTL3 مستويات أعلى من بروتينات ‘‘انتحار الخلية’’ الكلاسيكية مثل Bax وcleaved caspase-3، وتم تمييز المزيد من الخلايا على أنها خاضعة للاستماتة بواسطة قياس التدفق الخلوي. أشارت تحليلات رنا أعمق إلى جين واحد، CDKN1A (الذي يصنع بروتين p21)، باعتباره لاعباً أساسياً: عندما تم خفض METTL3، ارتفعت مستويات CDKN1A بشكل حاد.
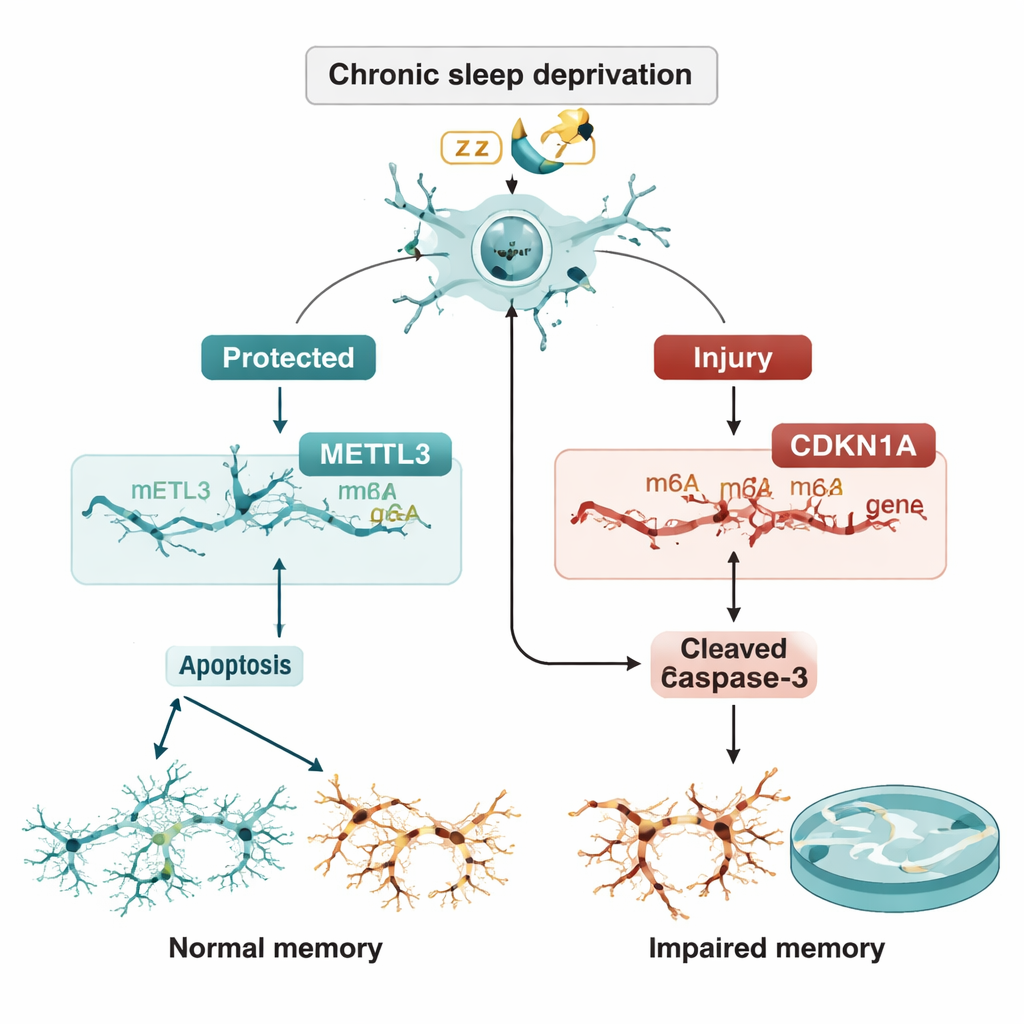
توازن هش بين الحماية والتدمير الذاتي
سأل الفريق بعد ذلك ما إذا كان METTL3 يتحكم في CDKN1A عبر وسم m6A. أظهروا أن خفض METTL3 قلل من علامات m6A على رنا CDKN1A وجعل ذلك الرنا أكثر استقراراً، فارتفعت مستوياته بدلاً من أن تُحطَّم. أدت زيادة CDKN1A بدورها إلى دفع الخلايا العصبية نحو الاستماتة. والأهم من ذلك، عندما تم إسكات CDKN1A نفسه، تراجع الموت الخلوي الإضافي الناجم عن فقدان METTL3 إلى حد كبير. في الفئران الحية، أدى توصيل METTL3 إضافي مباشرة إلى منطقة CA3 بواسطة ناقل فيروسي إلى خفض مستويات CDKN1A، وتقليل وفرة بروتينات الاستماتة، والحفاظ على بنية الخلايا العصبية في تلوين الأنسجة، وتحسين الأداء في متاهة الماء رغم استمرار فقدان النوم.
ماذا يعني هذا للأشخاص الذين لا يحصلون على قدر كافٍ من النوم
ببساطة، يبدو أن الحرمان المزمن من النوم يخفت إنزيم الحماية METTL3 في دائرة ذاكرة حرجة في الدماغ. عندما ينخفض METTL3، يعجز عن وسم بعض جزيئات الرنا بشكل صحيح، خاصة الرنا المشفر لـ CDKN1A. يتراكم هذا الرنا بعدها، مما يدفع الخلايا العصبية نحو الموت المبرمج ويساهم في مشاكل الذاكرة. باستعادة METTL3، تمكن الباحثون من خفض CDKN1A، وتقليل فقدان الخلايا العصبية، وإنقاذ الذاكرة في الفئران المحرومة من النوم. ومع بقاء هذه النتائج في مرحلة الحيوانات، تحدد الدراسة مسار METTL3–CDKN1A كهدف واعد لأدوية مستقبلية تهدف إلى حماية الدماغ من التبعات المعرفية للحرمان المزمن من النوم.
الاستشهاد: Xing, F., Shi, XS., Gu, HW. et al. METTL3-mediated m6A modification regulates CDKN1A to attenuate chronic sleep deprivation-induced cognitive impairment and neuronal apoptosis in rats. Transl Psychiatry 16, 96 (2026). https://doi.org/10.1038/s41398-026-03855-4
الكلمات المفتاحية: الحرمان المزمن من النوم, الحُصين, مثيلة الحمض النووي الريبي, استماتة الخلايا العصبية, ضعف الذاكرة