Clear Sky Science · ar
أدوار متنوعة ومحددة مكانيًا لـ PlexinA2 وPlexinA4 وNCAM في ألياف الموسى الحُصَينية النامية
كيف تشكل مسارات الأعصاب دوائر الذاكرة
الحُصَيْن، منطقة دماغية أساسية لتكوين واسترجاع الذكريات، يُبنى بألياف عصبية دقيقة يجب أن تتنقل بدقة خلال الحياة المبكرة. تطرح هذه الدراسة سؤالًا يبدو بسيطًا: كيف تعرف هذه الألياف النامية بالضبط إلى أين تذهب — وماذا يحدث عندما يختل نظام توجيهها، مما قد يساهم في حالات مثل الفصام أو التوحّد أو الصرع؟
طريقتان رئيسيتان إلى مركز الذاكرة
داخل الحُصَيْن، ترسل الخلايا العصبية في منطقة تُسمى التجويف السنخي (dentate gyrus) أليافًا طويلة تُعرف بألياف الموسى نحو منطقة أخرى تُسمى CA3. عند دخولها CA3، تنقسم هذه الألياف عادةً إلى «طريقتين سريعتين» مميزتين: واحدة تجري فوق طبقة أجسام خلايا CA3 وأخرى تجري تحتها. كل طريق يتصل بأجزاء مختلفة من خلايا CA3 ويساعد على ضبط توازن النشاط في هذه الدائرة الذاكرية. إذا فشلت هذه المسارات في الانفصال بشكل صحيح، فقد تنتهي الألياف في مواضع خاطئة، مما قد يعطل كيفية تدفق المعلومات عبر الحُصَيْن.
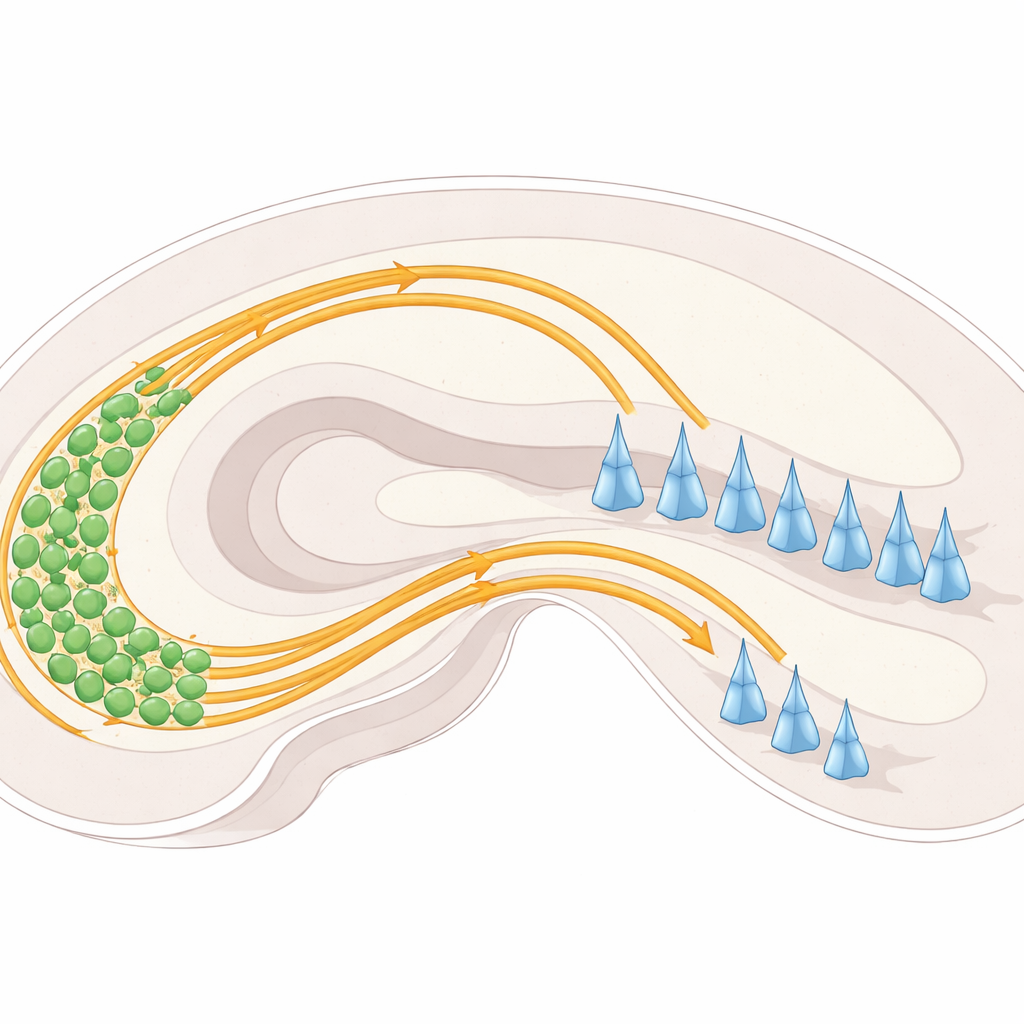
إشارات التوجيه: دفع، جذب، والتماسك بين الخلايا
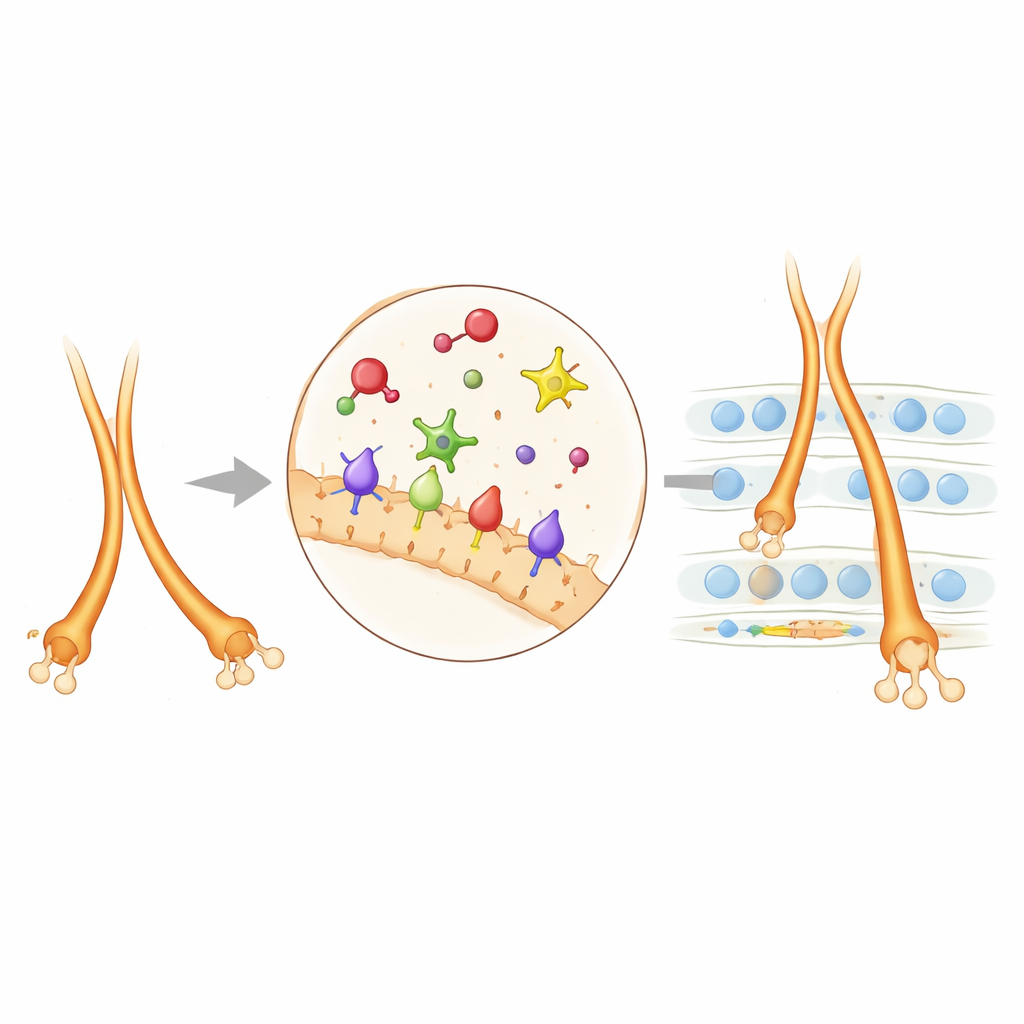
ركز الباحثون على مجموعة من إشارات جزيئية ومقابض سطحية على الخلايا العصبية التي توجه ألياف الموسى. عائلة بروتينات تُسمى بلكسينات (PlexinA2 وPlexinA4) تجلس على أسطح الخلايا العصبية وتستجيب لجزيئات شريكة تُعرف بالسيمافورينات، لا سيما Sema6A. يمكن أن تعمل هذه التفاعلات كإشارات «ممنوع الدخول»، تدفع الألياف بعيدًا عن مناطق معينة، أو تضبط بدقة مدى تلاصق الألياف المجاورة معًا. بروتين سطحي آخر، NCAM، يتصرف أشبه بشرائط الفيلكرو، يعزز الالتصاق ويساعد حزم الألياف على التماسك. من خلال فحص أماكن التعبير عن هذه البروتينات وما يحدث عند إزالتها أو تغييرها في الفئران، رسم الفريق خريطة كيفية تعاونها في أدمغة حية بدلًا من خلايا معزولة.
تفكيك الأدوار باستخدام فئران مُصمّمة
لفصل دور كل مكوّن، أنشأ العلماء وجمعوا 27 سلالة فئران مختلفة. بعضها كانت تفتقر تمامًا إلى Sema6A، وآخرون خلت أجسادهم من PlexinA2 أو PlexinA4، بينما حملت مجموعات أخرى طفرات نقطية دقيقة عطّلت جزءًا محددًا فقط («لب إنزيمي») داخل البلكسينات بينما تركت بقية الجزيء سليمًا. كما أزالوا Sema6A أو NCAM انتقائيًا من أنواع خلايا معينة، مثل خلايا الحبيبات في التجويف السنخي، لاختبار المكان الذي تُحدث فيه الإشارة الفارق فعلاً. في الفئران التي تفتقد Sema6A في هذه الخلايا الحبيبية، فشلت ألياف الموسى في الانقسام بوضوح إلى حزم علوية وسفلية ونمت الحزمة السفلية بشكل مفرط وتجاوزت نقطة النهاية الاعتيادية. ظهرت أخطاء توصيل مشابهة ولكن ليست متماثلة في الفئران التي تفتقد PlexinA2 أو PlexinA4، ما كشف أن هذه البروتينات تعمل عند نقاط تفتيش مميزة على طول نفس المسار.
التدقيق في الآليات والشراكات
عندما عطل المؤلفون اللبَ الحفّازي لبلكسينA4، ظهرت العديد — لكن ليس كل — العيوب نفسها التي لوحظت في حيوانات فقدان PlexinA4 الكاملة. هذا أظهر أن PlexinA4 غالبًا ما يعتمد على هذا اللب لإعادة تشكيل الهيكل الداخلي للألياف العصبية النامية، مساعدًا إياها على التكتل بشكل صحيح والتوقف عند الطبقة المناسبة. أما PlexinA2 فتبين أنه مختلف: بعض أدواره اعتمدت على اللب الإنزيمي، بينما لم تعتمد أدوار أخرى عليه، مما يشير إلى مسارات إشارية إضافية مستقلة عن الإنزيم. ثم استخدم الفريق تقنية وسم القرب لتحديد البروتينات المجاورة حول PlexinA2 على الخلايا العصبية الحُصَينية الشابة. ظهرت عدة جزيئات لالتصاق الخلايا، وكان NCAM بارزًا بينها. جينيًا، أدى تقليل كل من PlexinA2 وNCAM معًا إلى تشويه توجيه ألياف الموسى أقوى مما يحدث عند تقليل أيٍ منهما بمفرده، مما يبيّن أن هذين النظامين يتعاونان: يوفر NCAM الالتصاق، بينما تضبط قوى النفور المولَّدة عبر PlexinA2 كيفية انقسام الألياف إلى المسارين العلوي والسفلي وإلى أي مدى يمتد المسار السفلي.
عندما تسير الإشارات بالعكس
بطريقة مثيرة للاهتمام، لا يعمل Sema6A فقط كإشارة خارجية تقرأها البلكسينات؛ بل يمكن أن يعمل أيضًا كمتلقٍ على ألياف الموسى نفسها. درس الباحثون فئرانًا حُذفت فيها ذيل Sema6A الداخلي بينما بقي جزءها الخارجي سليمًا. في هذه الحيوانات، استمرت بعض عيوب التوجيه — خاصة فرط نمو الحزمة السفلية — مما يدل على أن الإشارات الداخلة عبر ذيل Sema6A («الإشارات العكسية») ضرورية للتقليم والتشكيل الطبيعي لألياف الموسى. من المحتمل أن يعمل هذا النمط العكسي جنبًا إلى جنب مع إشارة البلكسين الأكثر شيوعًا بطريقة تعتمد على المرحلة والموقع.
لماذا يهم هذا التوصيل لصحة الدماغ
ربطت طفرات في النسخ البشرية من PLXNA2 وSEMA6A وNCAM1 بحالات تطور عصبي ونفسية، من تأخر عقلي إلى الفصام والتوحّد. من خلال إظهار كيفية تعاون هذه الجزيئات بدقة لنحت مسارات ألياف الموسى لدى الفئران، تقدم هذه الدراسة نموذجًا ملموسًا لكيفية تأثير تغييرات جينية طفيفة على تشكيل وفصل وتقليم دوائر الذاكرة الأساسية. وبعبارات يومية، تقترح الدراسة أن مجموعة أدوات التوجيه في الدماغ تستخدم مزيجًا زمنيا محكمًا من إشارات «دفع» و«جذب» و«اللزوجة» لبناء مخطط توصيل الحُصَيْن — وأن حتى الاضطرابات الصغيرة في هذه الأدوات قد تتسع آثارها إلى تغييرات في التعلم والذاكرة والصحة العقلية.
الاستشهاد: Zhao, XF., Kohen, R., Van Battum, E.Y. et al. Diverse and location-specific roles of PlexinA2, PlexinA4, and NCAM in developing hippocampal mossy fibers. Transl Psychiatry 16, 126 (2026). https://doi.org/10.1038/s41398-026-03846-5
الكلمات المفتاحية: ألياف الموسى الحُصَينية, توجيه المحاور العصبية, إشارة السيمافورين-بلكسين, NCAM والتلاصق الخلوي, اضطرابات التطور العصبي