Clear Sky Science · ar
خلل الخلايا العصبية البينية المثبطة غابا يسبب تغيرات في تذبذبات الشبكة العصبية المرتبطة بنشاط صرعي لدى فئران ناقصة إنزيم PPT1
عندما تختل إيقاعات الدماغ
النوبات ليست مجرد عواصف مفاجئة من النشاط الدماغي؛ فهي غالبًا ما تنشأ من تغييرات دقيقة في كيفية تواصل الخلايا العصبية مع بعضها. تتناول هذه الدراسة اضطرابًا دماغيًّا نادرًا للأطفال، مرض CLN1، وتطرح سؤالًا بسيطًا له آثار بعيدة المدى: ماذا يحدث لحافظي «الإيقاع» الداخلي للدماغ عندما يفتقد إنزيم واحد اسمه PPT1؟ من خلال متابعة هذه التغيرات في الفئران عبر الزمن، يكشف الباحثون كيف يمكن لعيوب صغيرة مبكرة في التثبيط أن تتصاعد لتؤدي إلى نوبات وضرر واسع النطاق في الدماغ.
حراس توازن الدماغ
يعتمد دماغنا على نوعين عامين من الخلايا العصبية. الخلايا المنشِّطة، مثل الخلايا الهرمية في الحصين، تدفع النشاط إلى الأمام. أما الخلايا المثبطة، المسماة بالخلايا العصبية البينية، فتمثل الفرامل، تحافظ على ضبط هذا النشاط وتشكل الإيقاعات الكهربائية للدماغ. من بين هذه الخلايا مجموعتان مهمتان هما الخلايا البينية موجبة البارفالبيومين (PV+) والخلايا البينية موجبة السوماتوستاتين (SST+). تسهم هاتان المجموعتان في توليد وتنسيق موجات دماغية إيقاعية مثل تذبذبات الثيتا والغاما، التي تدعم وظائف مثل التعلم والذاكرة. في مرض CLN1، يفقد الأطفال إنزيم PPT1 الذي يزيل مجموعات دهنية من البروتينات. استخدم المؤلفون نموذجًا فأريًا يحمل نفس الطفرة الموجودة لدى المرضى ليروا كيف يؤثر فقد هذا الإنزيم على الخلايا البينية وعلى الإيقاعات التي تساعد في تنظيمها.
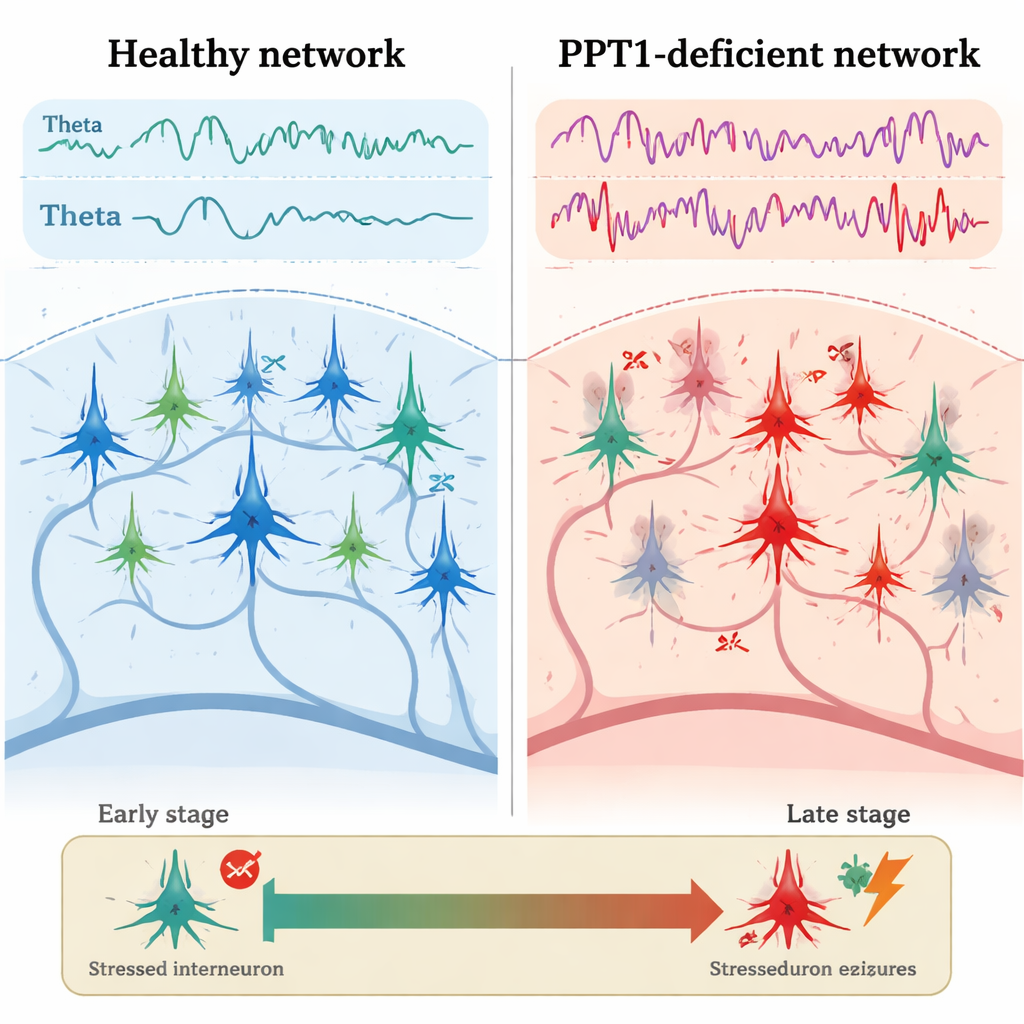
شقوق مبكرة في نظام التثبيط
في الفئران الطافرة البالغة الصغيرة، بعمر نحو ثلاثة إلى أربعة أشهر، ظهر أول خلل واضح في الخلايا البينية PV+. أظهرت التسجيلات الكهربائية من الحصين أن هذه الخلايا المثبطة كانت تطلق نبضات أقل تكرارًا مقارنة بالفئران السليمة، بينما أطلقت الخلايا الهرمية المجاورة نبضات أكثر سرعة ومع فترات توقف أقصر بين الشُظَف. كشفت المجهرية أن العديد من الخلايا البينية PV+ أظهرت تنشيط الكاسبيز-3، وهو عامل تنفيذي رئيسي في الموت المبرمج للخلايا، رغم أن أعدادها الإجمالية لم تنخفض بعد. في الوقت نفسه، ازدادت قوة موجات الثيتا والغاما، وأظهرت تصوير الكالسيوم نشاطًا أقوى في خلايا الحصين أثناء تحرك الحيوانات. والأهم من ذلك، تضعف «التداخل» الطبيعي بين تذبذبات الثيتا والغاما—حيث تساعد الموجات البطيئة في تنظيم الأسرع—مما يشير إلى انهيار مبكر في توقيت النشاط الشبكي الدقيق.
من الإيقاعات المضطربة إلى نوبات متفجرة
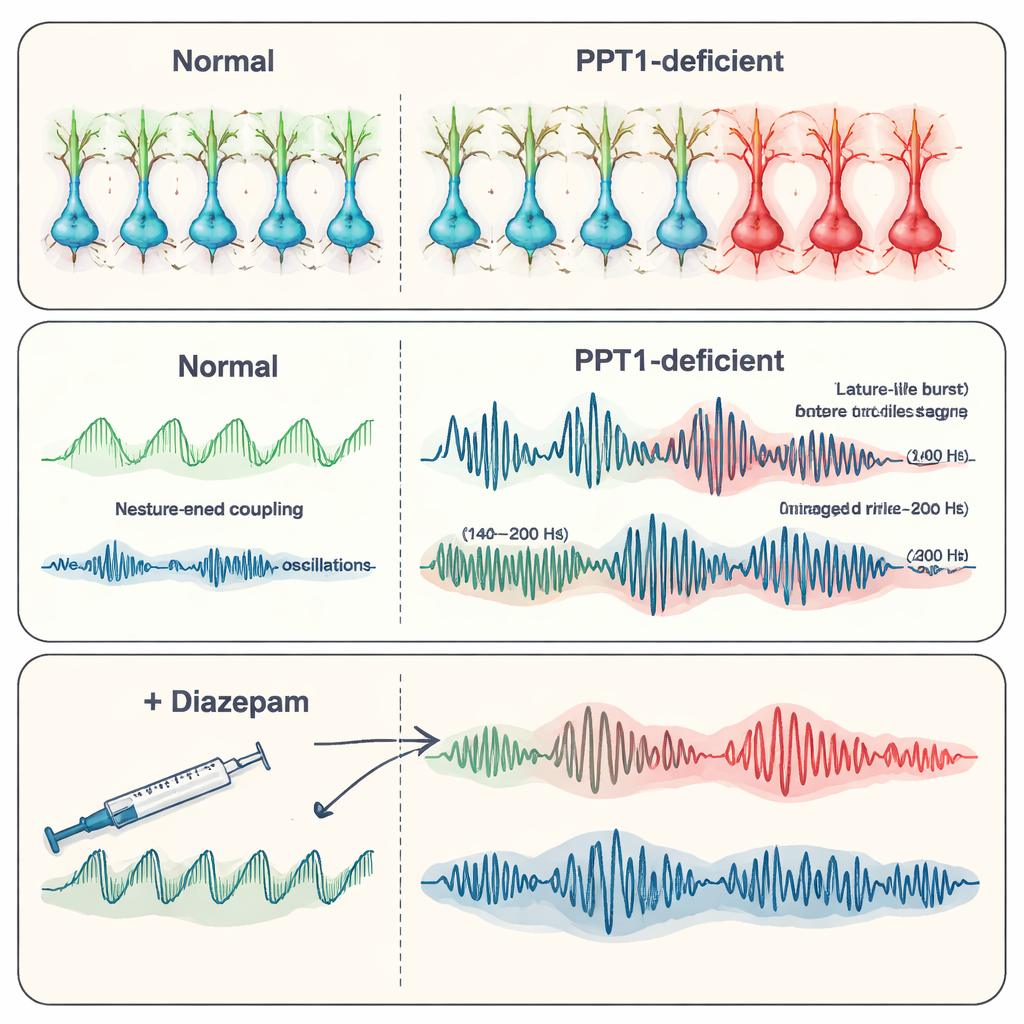
بحلول سن ستة إلى سبعة أشهر، تفاقم الوضع. فقدت العديد من الخلايا البينية PV+، وظهرت الآن علامات تنشيط الكاسبيز-3 أيضًا في الخلايا البينية SST+. كشفت التسجيلات من الحصين عن تفريغات صرعية عفوية—اندفاعات قصيرة غير طبيعية من النشاط مرتبطة بالنوبات. ركز الفريق على «التموجات» عالية التردد، تذبذبات سريعة تساعد عادة في تخزين الذكريات. في الفئران الطافرة، أصبحت التموجات الفسيولوجية (حوالي 140–200 هرتز) أقل تكرارًا لكن ذات سعة أكبر، بينما ازدادت التموجات «المرضية» الأسرع (200–500 هرتز)، المرتبطة ارتباطًا وثيقًا بالصرع، قوة وشيوعًا. تقترح هذه التغيرات تحوّلاً من إيقاعات منظمة متعلقة بالذاكرة نحو أنماط فوضوية مهيأة للصرع مع فشل السيطرة التثبيطية.
تآكل الخلايا وتأثير الديازيبام
مع تقدم المرض، بدأ الحصين نفسه في التآكل. انخفضت إشارات الكالسيوم في الخلايا العصبية، أظهر تلطيخ غولجي أشجارًا شجيرية أرق وأقل تفريعًا، وانخفض عدد النتوءات الصغيرة التي تتشكل عند المشابك. أكدت تعداد الخلايا في مناطق الحصين الرئيسية (CA1 وCA3) فقدان خلايا واسع النطاق، وأصبحت الوحدات النشطة أقل قابلية للاكتشاف في التسجيلات الكهربائية. ثم اختبر الباحثون ديازيبام، دواء شائع مضاد للنوبات يعزز فعل الناقل المثبط غابا. في الفئران الطافرة الأكبر سنًا خفف الديازيبام من تكرار التفريغات الصرعية وأعاد جزئيًا أنماط تذبذبات أكثر طبيعية، بما في ذلك سلوك التموجات، رغم أنه لم يعالج فقدان المستقبلات الأساسي. يشير ذلك إلى أن تقوية الإشارات المثبطة المتبقية قد تُهدئ الشبكة، على الأقل مؤقتًا.
لماذا تهم هذه النتائج
بالنسبة للقارئ العام، الرسالة الأساسية هي أن مرض CLN1 ليس مجرد تراكم نفايات داخل خلايا الدماغ. يؤدي فقدان PPT1 إلى سلسلة من التفاعلات: أولًا، تتعرض الخلايا البينية المثبطة المتخصصة للإجهاد وتبدأ في الفشل، مما يطلق نشاط الخلايا الهرمية المفرط ويشوّه إيقاعات الدماغ. مع مرور الوقت، يؤدي هذا الخلل إلى نوبات وفي النهاية إلى فقدان كبير للخلايا والاتصالات الدماغية. تشير الدراسة إلى وجود نافذة مبكرة من الفرص، عندما قد يمنع حماية أو إنقاذ خلايا PV+ البينية—ربما عبر حجب تنشيط الكاسبيز—حدوث النوبات والتدهور اللاحق. وبينما لا يستطيع الديازيبام شفاء CLN1، يبرز قدرته على كبح الإيقاعات الشاذة في هذا النموذج الفكرة الأوسع بأن استعادة التثبيط يمكن أن تكون استراتيجية فعالة في الصرع واضطرابات دماغية ذات صلة.
الاستشهاد: Tong, J., Liu, W., Wang, Q. et al. Dysfunction of GABAergic interneurons underlies altered neural network oscillations associated with epileptiform activity in PPT1-deficient mice. Transl Psychiatry 16, 106 (2026). https://doi.org/10.1038/s41398-026-03843-8
الكلمات المفتاحية: الصرع, الخلايا العصبية البينية, الحصين, تذبذبات الدماغ, مرض تراكم الليسوسومات