Clear Sky Science · ar
التغيرات الوظيفية المبكرة والبروتين GFAP في البلازما لدى عائلات سويدية تحمل طفرات مرض الزهايمر المهيمنة جسمياً
لماذا تهم هذه الدراسة العائلات
غالباً ما يبدو مرض الزهايمر وكأنه يظهر فجأة، لكن في الواقع تتراكم التغيرات الضارة في الدماغ بصمت على مدى سنوات طويلة. في العائلات النادرة التي تحمل طفرات موروثة («مهيمنة جسمياً») لمرض الزهايمر، يستطيع العلماء تقدير متى من المرجح أن تبدأ الأعراض ومراقبة هذه التغيرات المبكرة أثناء تطورها. تابعت هذه الدراسة عائلات سويدية تحمل مثل هذه الطفرات لفهم كيف يتغير استخدام الدماغ للطاقة، والقدرات الإدراكية، وعلامة دموية لخلايا الدعم الدماغي (GFAP) قبل سنوات طويلة من ظهور مشاكل الذاكرة — وكيف تختلف هذه التغيرات بين الجينات.
متابعة ساعة المرض في العائلات عالية المخاطر
لأن الأشخاص المصابين بمرض الزهايمر المهيمن جسمياً (ADAD) عادة ما تظهر لديهم الأعراض في عمر متوقع بشكل معقول، يمكن للباحثين حساب «السن المقدر لبدء الأعراض» (EYO) — عدد السنوات المتبقية قبل أو بعد العلامات الأولى المتوقعة للمرض. درس الفريق 45 بالغاً من عائلات سويدية تحمل طفرات في جينات APP أو PSEN1، إضافة إلى أقارب لا يحملون الطفرات. على مدى أكثر من سبع سنوات في المتوسط، خضع المشاركون لفحوص تصويرية للدماغ تقيس مدى استهلاك الدماغ للسكر (FDG PET)، واختبارات إدراكية وذاكرية مفصلة، ولجزء منهم اختبارات دم لمستوى GFAP، وهو بروتين يفرز عندما تصبح خلايا الدعم الدماغي المعروفة بالخلايا النجمية تفاعلية. سمح هذا التصميم للعلماء بمواءمة التغيرات البيولوجية المختلفة على خط زمني مشترك للمرض بدلاً من مقارنة الأشخاص في لحظة واحدة فقط.
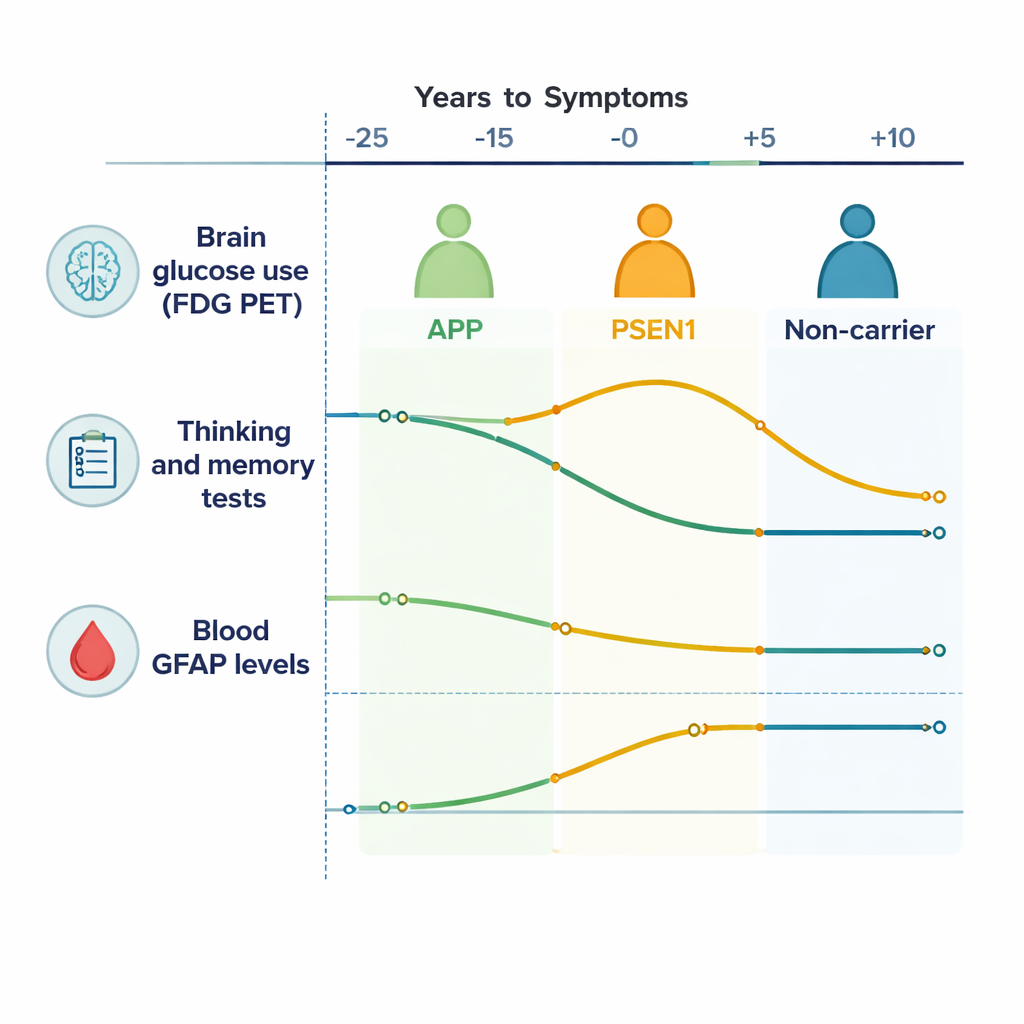
تعقب طاقة الدماغ والقدرات الإدراكية مع مرور الوقت
عبر قشور الدماغ الخارجية، أظهر الأشخاص الحاملون لطفرات الزهايمر انخفاضاً تدريجياً في إشارة FDG PET مقارنة بأفراد العائلات غير الحاملين للطفرات، ما يعني أن أدمغتهم كانت تستهلك كمية أقل من السكر مع مرور الوقت — علامة على تراجع خلايا الدماغ. كما أظهرت مناطق تحت القشرة داخلية في الدماغ، خصوصاً النواة الذيلية والمهاد، نشاطاً متراجعاً، وكان هذا مدفوعاً أساساً بأصحاب طفرات APP. تدهورت الاختبارات المعرفية والذاكرية عبر عدة مجالات، بما في ذلك الذاكرة العرضية والمرونة الذهنية، بدءاً من نحو 10–15 سنة قبل العمر المتوقع لظهور الأعراض. بعبارة أخرى، حتى عندما كان الأشخاص يشعرون بأنهم طبيعيون ويؤدون مهامهم اليومية، كشفت الاختبارات والحساسيات التصويرية أن أدمغتهم كانت تعمل بجهد أكبر وبكفاءة أقل.
أنماط مختلفة لجينات مختلفة للزهايمر
أحد الاستنتاجات الرئيسية كان أن مجموعتي الطفرات الرئيسيتين — APP وPSEN1 — لم تتبعا مساراً موحداً. في حاملي PSEN1، رصد الباحثون فترة مبكرة، نحو 20 إلى 10 سنوات قبل الأعراض المتوقعة، أظهرت أجزاء من الدماغ خلالها استهلاكاً غير اعتيادي عالٍ للسكر («زيادة الأيض»)، إلى جانب أداء أفضل في الاختبارات، قبل أن يتراجع النشاط لاحقاً. يُعزى ذلك على الأرجح إلى مرحلة تعويضية مؤقتة، حيث يزيد الدماغ وخلايا الدعم نشاطهما للتأقلم مع تلف متزايد. أما حاملو APP، فبدت لديهم عملية أكثر بساطة تتمثل في انخفاض تدريجي في أيض الدماغ دون ذروة مبكرة. تشير هذه الأنماط الخاصة بالجين إلى أن «مرض الزهايمر» ليس قصة بيولوجية واحدة حتى في الأشكال الموروثة، بل مجموعة من العمليات المرتبطة التي تتطور بشكل مختلف اعتماداً على الطفرة الأساسية.
ما الذي تكشفه فحوصات الدم عن الضغط المبكر في الدماغ
قدم GFAP، المقاس من عينة دم بسيطة، نافذة على كيفية استجابة الخلايا النجمية للتغيرات المبكرة المرتبطة بالزهايمر. مال مستوى GFAP إلى الارتفاع تدريجياً مع اقتراب الأشخاص من عمر الأعراض المتوقع لدى كل من الحاملين وغير الحاملين للطفرات، لكن العلاقات بين GFAP، وأيض الدماغ، والأداء المعرفي كانت خاصة بكل جين. في حاملي APP، ارتبط ارتفاع GFAP بانخفاض استهلاك السكر في مناطق عميقة من الدماغ وبتراجع الأداء في معظم الاختبارات المعرفية، مما يوحي بأن تنشيط الخلايا النجمية مرتبط ارتباطاً وثيقاً بالتلف المبكر وفقدان الوظيفة. في حاملي PSEN1، كانت هذه الروابط أضعف أو غائبة، مما يشير مرة أخرى إلى مسارات بيولوجية مختلفة تؤدي إلى نفس النتيجة السريرية المتمثلة في الخرف.
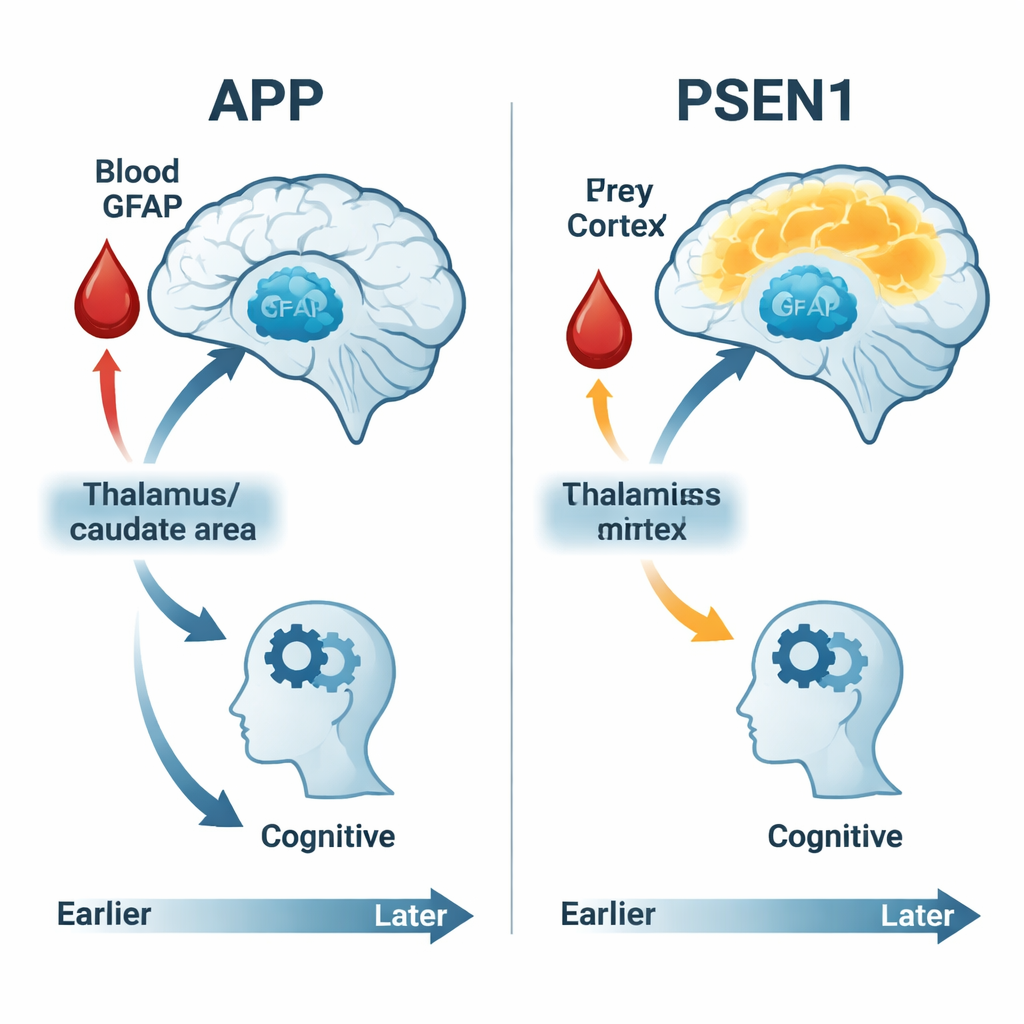
ماذا يعني هذا للكشف المبكر والعلاج
للقارئ العام، الرسالة الأساسية هي أن التغيرات المتعلقة بالزهايمر في هذه العائلات عالية المخاطر تبدأ قبل عقود من فقدان الذاكرة الواضح — وهي لا تظهر بنفس الشكل لدى الجميع. يمكن لتصوير استهلاك السكر في الدماغ، والاختبارات المعرفية الدقيقة، وعلامة دم واحدة مثل GFAP أن تكشف معاً متى يبدأ الدماغ في المعاناة ومدى سرعة تقدمها. والأهم أن الأشخاص ذوي الأشكال الجينية المختلفة من الزهايمر يظهرون تسلسلات تغير مختلفة: لدى البعض مرحلة مبكرة مفرطة النشاط، ولدى آخرين انحدار ثابت، وترتبط علامة دم الخلايا النجمية بالضرر بقوة أكبر في بعض المجموعات مقارنة بغيرها. قد يساعد التعرف على هذه المسارات المميزة في تخصيص الأدوية والتجارب المستقبلية للأشخاص المناسبين في الوقت المناسب، ويؤكد وعد فحوصات الدم مثل GFAP في التقاط مرض الزهايمر في مرحلة أبكر — قبل أن تسلب الأعراض الناس استقلاليتهم.
الاستشهاد: Luckett, E.S., Zapater-Fajari, M., Almkvist, O. et al. Early functional changes and plasma GFAP in Swedish families with Autosomal Dominant Alzheimer’s disease mutations. Transl Psychiatry 16, 67 (2026). https://doi.org/10.1038/s41398-026-03829-6
الكلمات المفتاحية: مرض الزهايمر المهيمن جسمياً, علامة حيوية GFAP في الدم, أيض الجلوكوز الدماغي, الخلايا النجمية والتنكس العصبي, الكشف المبكر عن الزهايمر