Clear Sky Science · ar
مؤشرات التنبؤ الحاسوبية للتغيرات الجينية في الصيدلة الوراثية: من تقييم الأليلات الفردية إلى تقدير تفاعلات الأدوية الضارة مع مضادات الاكتئاب
لماذا تهم جيناتك لسلامة استخدام مضادات الاكتئاب
عندما يتناول شخصان نفس مضاد الاكتئاب، قد يتحسن أحدهما مع آثار جانبية قليلة بينما قد يواجه الآخر مشكلات خطيرة، بما في ذلك سمية الدواء. تستكشف هذه الدراسة ما إذا كانت البرامج الحاسوبية قادرة على قراءة الاختلافات الطفيفة في حمضنا النووي للتنبؤ بمن من المحتمل أن يعالج مضادات الاكتئاب بأمان ومن قد يكون عرضة أكثر لتفاعلات ضارة، مما قد يجعل وصف الأدوية اليومي أكثر أمانًا ودقة.

من التصنيفات الجامدة إلى درجات جينية مرنة
تعتمد العديد من العيادات اليوم على نظام يُسمى «الأليلات النجمية» (star alleles)، الذي يجمع التغيرات المعروفة في جينات معالجة الأدوية إلى فئات وظيفية عامة، مثل النشاط الطبيعي أو المنخفض. ساعد هذا النهج في توجيه العلاج، لكنه يتعثر عندما يحمل الشخص طفرات نادرة أو غير معروفة من قبل، أو تراكيب معقدة من التغيرات غير المدرجة في القوائم الرسمية. يرى المؤلفون أن هذه ثغرة كبيرة: معظم متغيرات الصيدلة الوراثية نادرة، وجزء كبير من التباين في كيفية تعامل الأفراد مع الأدوية يبقى غير مفسر بواسطة التصنيفات الحالية.
اختبار أدوات أذكى على طفرات معروفة وجديدة
قيّم الفريق عشرة أدوات حاسوبية تقيم مدى احتمال أن يكون تغيير في الحمض النووي مهيِّجًا للوظيفة، بما في ذلك إطارين جديدين طوروهما (PharmGScore وPharmMLScore). أولًا، سألوا ما إذا كانت هذه الأدوات قادرة على إعادة إنتاج الفئات الوظيفية المعينة مسبقًا لـ 541 أليلًا نجميًا مُنقَّحًا عبر ثمانية من الجينات الرئيسة لمعالجة الأدوية. من خلال جمع درجات كل المتغيرات داخل كل هابلوتيب، طابقت عدة أدوات أداء نظام النجوم أو حتى تفوقت عليه، مع تقدم PharmGScore على البقية. بعد ذلك، اختبروا الأدوات ببيانات من تجارب مخبرية عالية الإنتاجية على إنزيمين مهمين، CYP2C9 وCYP2C19، الذين يعالجان العديد من الأدوية. قاست هذه التجارب كيف أثرت آلاف الطفرات الفردية على نشاط الإنزيم ومستويات البروتين، وغالبية هذه الطفرات لم تُرَ من قبل في المرضى. هنا أيضًا، حددت الأدوات الأفضل أداءً، خصوصًا التجميعات المصممة لجينات الصيدلة وCADD، بدقة المتغيرات التي أضعفت وظيفة الإنزيم بشدة.
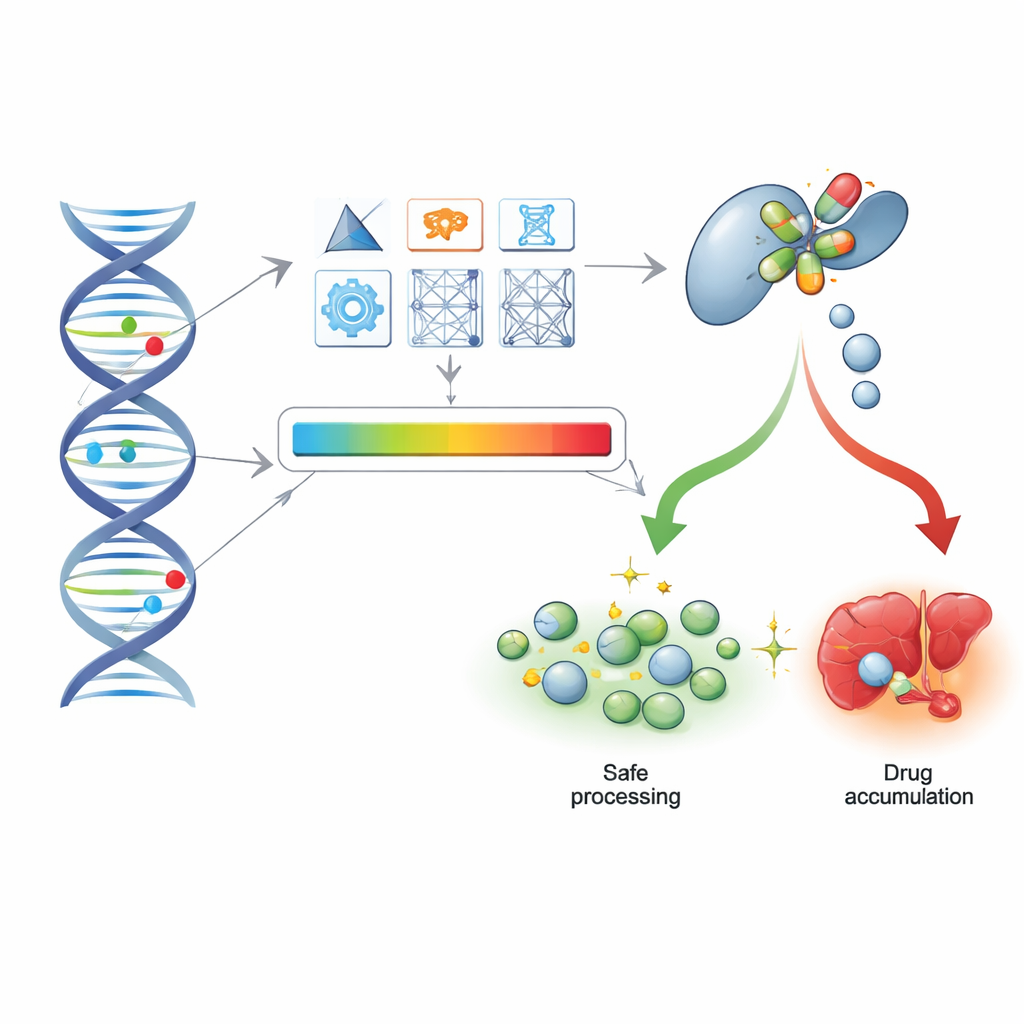
من تسلسلات الحمض النووي إلى سجلات المرضى في العالم الحقيقي
لمعرفة ما إذا كانت هذه الدرجات الحاسوبية تصمد في الممارسة الطبية اليومية، لجأ الباحثون إلى بيانات تسلسل الإكسوم لأكثر من 200,000 مشارك في بنك جسد المملكة المتحدة (UK Biobank)، إلى جانب سجلات وصفاتهم الطبية وسجلات المستشفيات. قارَنوا توقعات الأدوات باستدعاءات الأليلات النجمية لخمسة جينات رئيسية لمعالجة الأدوية ووجدوا أن أفضل الطرق قادرة إلى حد كبير على استرجاع نفس التجميعات الوظيفية، على الرغم من أن بيانات الإكسوم تفوِّت بعض التغيرات غير المشفرة والتغيرات التركيبية. والأهم من ذلك، أن النهج الجمعي — جمع تأثير كل المتغيرات في الجين — عمل جيدًا بما يكفي ليفصل الأشخاص ذوي الجينوتايب عديم الوظيفة عن أولئك ذوي النشاط الطبيعي.
كشف الأشخاص المعرضين لخطر تفاعلات خطيرة مع مضادات الاكتئاب
ركز المؤلفون بعد ذلك على استخدام مضادات الاكتئاب وسلامتها، موجهين الانتباه إلى إنزيم CYP2C19 الذي يساعد في تفكيك عدة أدوية شائعة للاكتئاب. بين أكثر من 75,000 مستخدم لمضادات الاكتئاب، فحصوا نتيجتين: التبديل المتكرر للأدوية كمؤشر تقريبي للاستجابة الضعيفة، وسجلات المستشفى أو الوفاة التي تشير إلى تسمم بمضادات الاكتئاب. بينما لم يظهر لا النظام النجمي ولا معظم الدرجات إشارة قوية أو واضحة لموضوع تبديل العلاج، كشفت عن نمط ذا دلالة للتفاعلات الشديدة. كان حاملو المتغيرات الضارة في CYP2C19 لديهم احتمالات أعلى بحوالي 20–35% لتسجيل رموز تسمم خطير بمضادات الاكتئاب في سجلاتهم، سواء صنفتهم الأليلات النجمية أو الأدوات الحاسوبية عالية الأداء مثل PharmGScore وPharmMLScore وCADD. ظل هذا الارتباط مشابهًا حتى عندما اقتصر التحليل على الحالات التي لم تُوثّق فيها إيذاء ذاتي.
ما الذي قد يعنيه هذا للوصفات المستقبلية
بشكل عام، تُظهر الدراسة أن مؤشرات التنبؤ الحاسوبية المصممة بعناية يمكن أن تصل إلى نفس مستوى الدقة لنظام الأليلات النجمية التقليدي، مع تجاوز أضعف نقاطه: العجز عن التعامل مع المتغيرات الجديدة أو النادرة أو المعقدة. من خلال تحويل تسلسلات الحمض النووي الخام إلى درجات مخاطرة مستمرة تعمل على مستوى الجينوم بأكمله، قد تسمح هذه الأدوات في النهاية للأطباء بالنظر أبعد من قائمة قصيرة من الأنماط الجينية المعروفة وتوقع من هم أكثر عُرضة لآثار جانبية خطيرة لمضادات الاكتئاب. قبل أن تُستخدم في الرعاية الروتينية، ستحتاج إلى مزيد من التحقق والتكامل مع عوامل سريرية أخرى، لكن هذا العمل يؤسس قاعدة قوية لوصف علاجي أكثر أمانًا وتخصيصًا بناءً على معلومات جينية شاملة.
الاستشهاد: Hajto, J., Piechota, M., Krätschmer, I. et al. Computational variant predictors for pharmacogenomics: from evaluation of single alleles to assessment of adverse drug reactions to antidepressants. Pharmacogenomics J 26, 8 (2026). https://doi.org/10.1038/s41397-026-00399-0
الكلمات المفتاحية: الصيدلة الوراثية, مضادات الاكتئاب, الطفرات الجينية, تفاعلات دوائية ضارة, التنبؤ الحاسوبي