Clear Sky Science · ar
قمع إنتاج الطاقة الميتوكوندرية بواسطة ببتيد كوبريدوكسين بكتيري ضوئي يثبط نمو الأورام
تحويل البكتيريا إلى مقاتلين ضد السرطان
الخلايا السرطانية جائعة للطاقة. تعتمد على “محطات طاقة” داخلية صغيرة تُسمى الميتوكوندريا لتوليد الطاقة التي تحتاجها للنمو والانتشار ومقاومة العلاج. تستكشف هذه الدراسة حليفًا غير متوقع في مكافحة السرطان: قطعة قصيرة من بروتين وُجد أصلاً في بكتيريا ضوئية. يبيّن الباحثون أن هذا الببتيد المصمم يمكنه التسلل إلى خلايا السرطان، وإيقاف مصدر طاقتها عند المنشأ، وجعل العلاج بالإشعاع أكثر فعالية بكثير — مع ترك الخلايا السليمة إلى حد كبير.
ببتيد صغير بمهمة كبيرة
بدأ الفريق من اكتشاف سابق مفاده أن بروتينًا بكتيريًا يُدعى أزورين يمكن أن يبطئ نمو الورم عن طريق التأثير على المكبوح الورمي الشهير p53. بحثوا بعد ذلك في البكتيريا التي تعيش داخل الأورام وحولها، مع تركيز على الميكروبات الضوئية التي تستخدم الضوء لتوليد الطاقة. تحمل هذه البكتيريا عائلة ذات صلة من البروتينات تُعرف بالكوبريدوكسينات. عبر مقارنة هياكلها وتاريخها التطوري، حدد الباحثون كوبريدوكسينًا واحدًا، أوراسينين B، واستخلصوا منه منطقة قصيرة مكونة من 28 حمضًا أمينيًا أسموها aurB. هذه الشظية قابلة للذوبان في الماء، ويمكنها عبور أغشية الخلايا، ولها شكل يوحي بأنها قد تتفاعل مع آلات توليد الطاقة الأساسية داخل الخلايا.
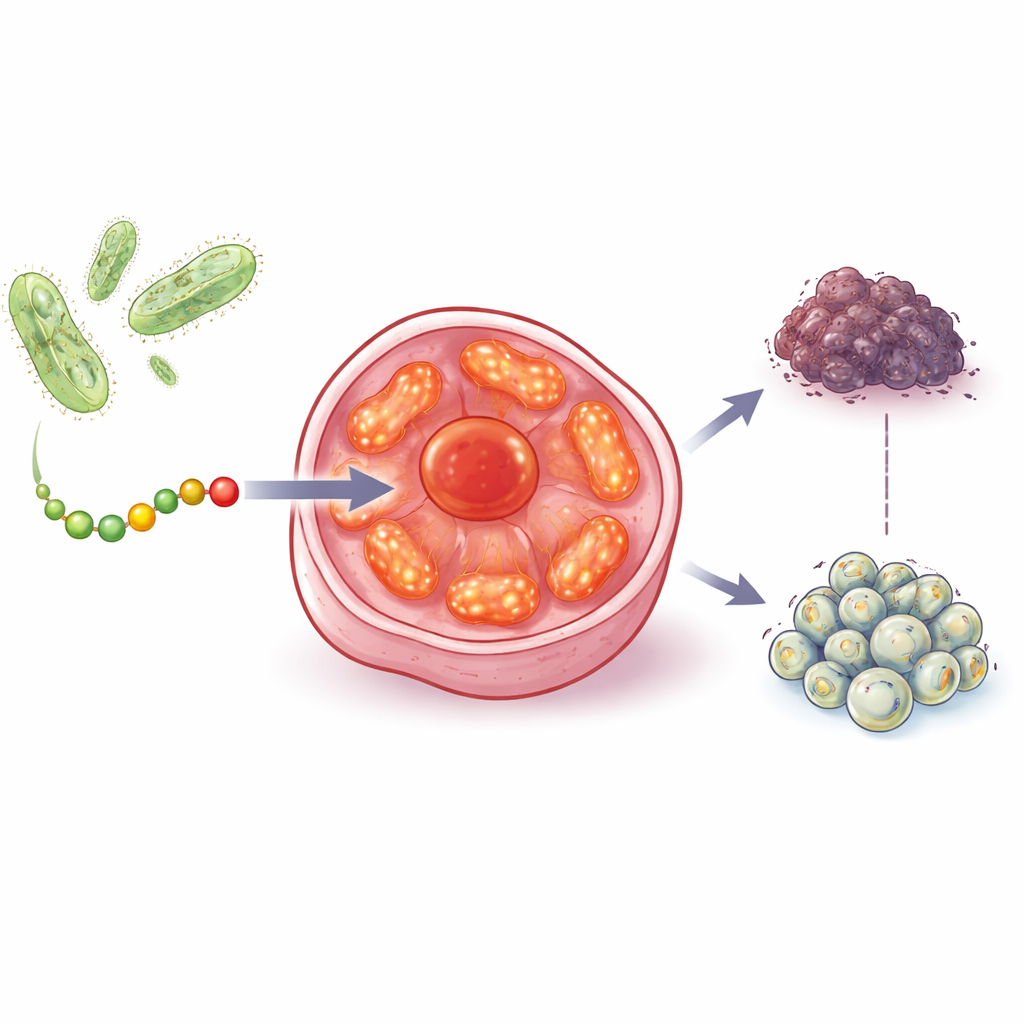
اكتشاف واستهداف محطات طاقة السرطان
في اختبارات مخبرية، قلل aurB من بقاء خطوط خلايا سرطان الثدي والبروستاتا والقولون والمبيض، حتى عندما كانت تلك الخلايا تفتقر إلى p53 العامل أو مستقبلات هرمونية التي تتطلبها العديد من الأدوية الحالية. ومن المهم أن آثار aurB على الخلايا السليمة في البروستاتا والقلب والعضلات كانت أضعف بكثير، على الرغم من أن هذه الخلايا الصحية غنية بالميتوكوندريا. أظهرت تجارب التصوير أن aurB دخلت الخلايا السرطانية بشكل تفضيلي ثم تراكمت داخل ميتوكوندرياتها. كما أكدت الميكروسكوبية الإلكترونية، باستخدام aurB مرتبطًا بقضبان ذهبية صغيرة كمؤشر بصري، أن الببتيد تراكم فعليًا داخل هذه العضيات.
قطع مصدر الإمداد بالطاقة
بمجرد دخوله الميتوكوندريا، ربط aurB مكونًا محددًا من سينثاز ATP — التوربين الجزيئي الذي يصنع ATP، العملة الرئيسية للطاقة في الخلية. حددت تجارب السحب الكيميائية والطيف الكتلي هذا الشريك على أنه ATP5C، جزء من النواة المركزية للإنزيم. أظهرت قياسات التشتت السطحي للبلازمون أن aurB يلتصق بـ ATP5C بقوة متوسطة وإفراج بطيء، متسقة مع تفاعل مستقر. كشفت الاختبارات الوظيفية ما يفعله هذا الارتباط: خفّض aurB بشكل حاد مستويات ATP الميتوكوندري في خلايا سرطان البروستاتا، وأبطأ معدل استهلاكها للأكسجين، وعرقل كلًا من التنفس والمسار الاحتياطي للتحلل السكري. ومع انهيار إنتاج الطاقة، ظهرت علامات موت مبرمج للخلايا يقوده الكاسباس-3، الإنزيم التنفيذي الرئيسي.
إيقاف الأورام وتعزيز الإشعاع
اختبر الباحثون بعد ذلك aurB في نماذج فأرية لسرطان البروستاتا العدواني. في الحيوانات التي تحمل أورام بروستاتا بشرية تحت الجلد، قللت الحقن المنتظمة من aurB نمو الورم بحوالي ثلثي حجمه، وهو ما يعادل أو يتفوق على الدواء الكيميائي باكليتاكسيل، لكن دون فقدان واضح للوزن أو معاناة. احتوت عينات الأورام من الفئران المعالجة على خلايا منقسمة أقل والعديد من الخلايا المحتضرة. في نموذج ثاني يحاكي نقائل عظمية — موقع شائع ومميت لانتشار سرطان البروستاتا — أبطأ aurB وحده توسّع الورم في عظم الساق وقلل عدد النقائل في الرئة. عندما جمعوه مع جرعة متواضعة من الإشعاع، كان التأثير دراماتيكيًا: كادت الأورام في الطرف المعالج أن تُمحى تمامًا، وانخفضت النقائل الرئوية بأكثر من 90 بالمئة مقارنةً بالمجموعات الضابطة.
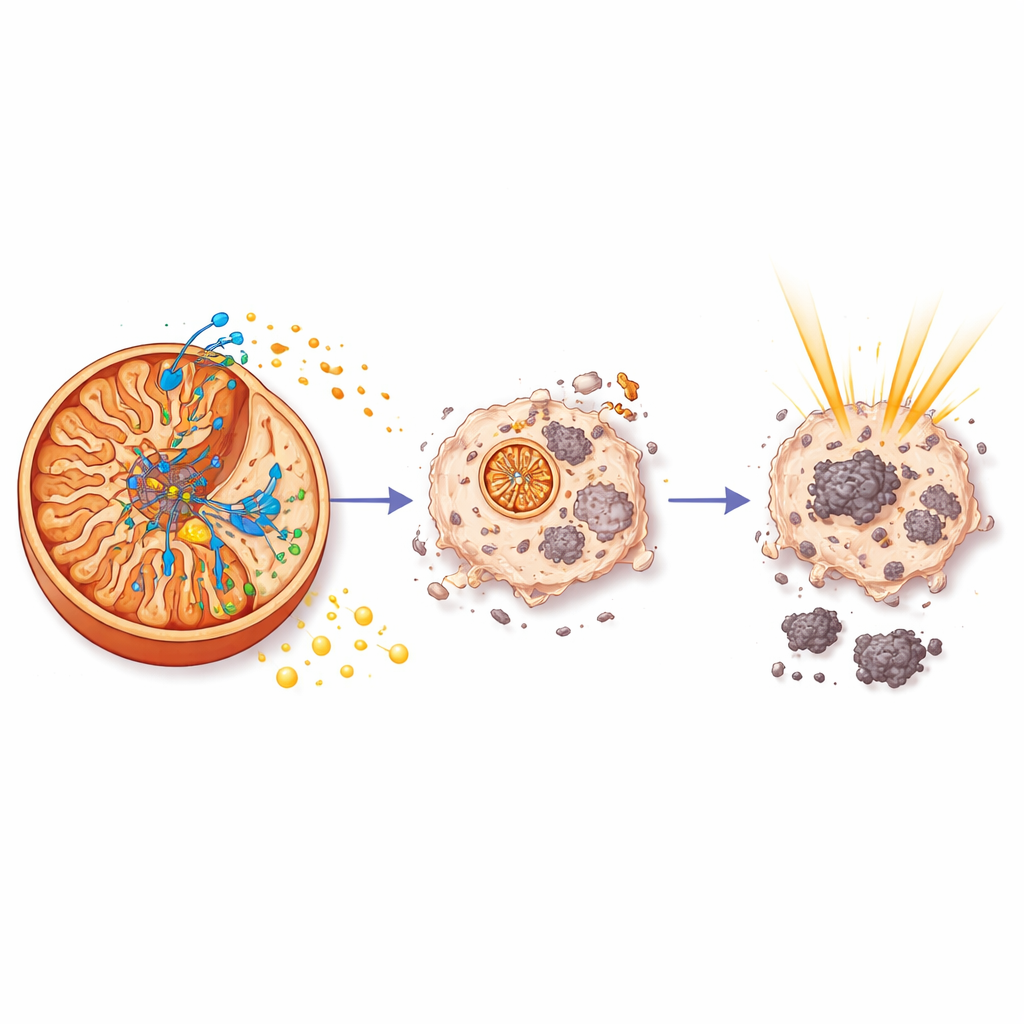
لماذا تهم الطاقة بالنسبة للإشعاع
لفهم سبب جعل aurB الإشعاع أكثر فعالية، فحص الفريق نشاط الجينات في أورام الفئران المعالجة. وجدوا أن aurB، وليس الإشعاع وحده، كبّح شبكة من الجينات يتحكم بها HIF-1، المنظم الرئيسي الذي يساعد الخلايا السرطانية على التكيّف مع نقص الأكسجين ويعزز المقاومة للعلاج. تحت ظروف الفقر الطاقي التي أحدثها aurB، خفّضت مسارات النمو والبقاء الأساسية المدفوعة بواسطة PI3K وc-Myc نشاطها، كما تم كبح الآلة التحللية السكريّة التي تسمح للأورام بالازدهار في بيئات صعبة. في الجوهر، عبر تخريب إنتاج ATP مباشرة عند توربين الميتوكوندريا، دفع aurB الخلايا السرطانية إلى أزمة طاقة جعلتها أكثر عرضة بكثير لأضرار الإشعاع.
فئة جديدة من حاصرات الطاقة الموجهة بدقة
تقدم هذه الدراسة استراتيجية جديدة للعلاج السرطاني: تصميم ببتيدات صغيرة مستوحاة من البكتيريا تتوجه نحو أنظمة الطاقة الميتوكوندرية المتغيرة في الأورام. يستهدف aurB، المشتق من بروتين بكتيري ضوئي، بشكل انتقائي مكونًا من سينثاز ATP الذي يكون غالبًا مفرط النشاط في سرطانات مثل البروستاتا والثدي والمبيض والدماغ. عبر تجويع الخلايا السرطانية مباشرة من الطاقة وإضعاف دفاعاتها، لا سيما ضد الإشعاع، يمكن لمثل هذه الببتيدات أن تكمل العلاجات الحالية وتقدّم خيارات حيث تفشل المناهج المعتمدة على المناعة. وبينما ما يزال العمل كثيرًا قبل أن يصل هذا المفهوم إلى العيادة، تُظهر الدراسة أن بروتينات الطاقة البكتيرية القديمة يمكن تحويلها إلى أدوات سرطانية حديثة وموجَّهة للغاية.
الاستشهاد: Naffouje, S.A., Tran, D.B., Rademacher, D.J. et al. Suppression of mitochondrial energy production by a photosynthetic bacterial cupredoxin peptide inhibits tumor growth. Sig Transduct Target Ther 11, 124 (2026). https://doi.org/10.1038/s41392-026-02703-7
الكلمات المفتاحية: سينثاز ATP الميتوكوندري, تمثيل سرطاني, ببتيدات علاجية, سرطان البروستاتا, تحسس للإشعاع