Clear Sky Science · ar
إشارة جوانين أحادي الفوسفات الدائري-بروتين كيناز G تقلل تكلس صمام الأبهر عبر الالتهام الذاتي الموجه بواسطة ULK1
لماذا يهم «صدأ» صمام القلب
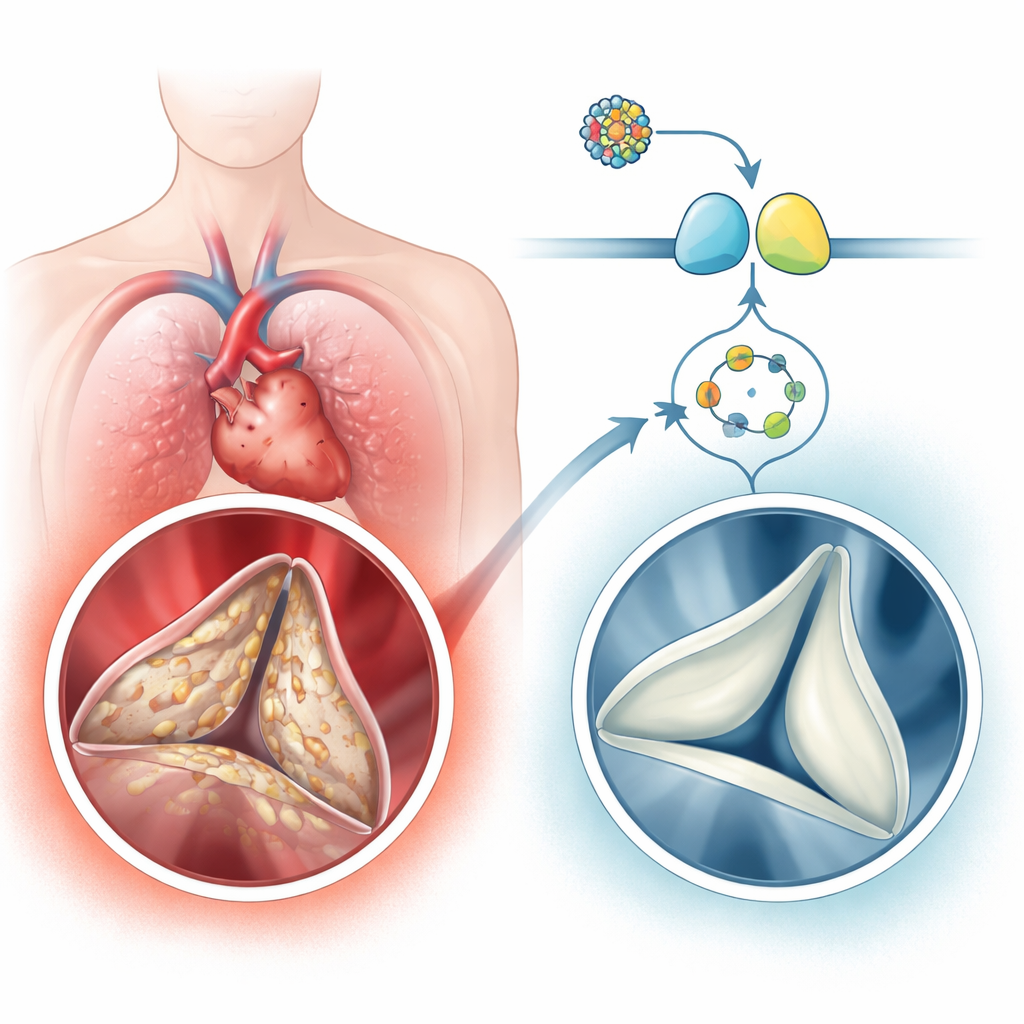
مع تقدّم العمر، قد يتيبس صمام الأبهر — البوابة الرئيسة لخروج الدم من القلب — ويتغطّى تدريجياً بكالسيوم، حالة تُسمّى مرض تكلس صمام الأبهر. هذا «التصلّب» يجبر القلب على الضخ بقوّة أكبر وقد يؤدي إلى ألم صدري أو إغماء أو فشل قلبي أو الحاجة إلى جراحة استبدال الصمام. حالياً لا يوجد دواء يُبطئ هذه العملية بشكل موثوق؛ والأطباء لا يفعلون سوى الانتظار حتى يتضرّر الصمام بشدّة ثم يجري الاستئصال الجراحي. تستكشف هذه الدراسة مساراً خلوياً مدمجاً يبدو أنه يحمي الصمام من التكلّس، وتختبر دواءً حديثاً لفشل القلب كطريقة محتملة لإعادة تفعيل ذلك الحماية.
مشكلة قلبية شائعة لكن مُهملة
يُعد مرض تكلس صمام الأبهر شائعاً بشكل مفاجئ لدى كبار السن، حيث يصيب نسبة قليلة بالمئة من الأشخاص فوق 65 عاماً وحتى شخصاً واحداً من كل عشرة فوق 75. المرض ليس مجرد «بلى وتآكل» سلبي. بل تتحول خلايا النسيج الضام الطرية في الصمام، المعروفة بخلايا الفواصل الصمامية، إلى حالات شبيهة بالتئام الجروح وبنيّة عظمية. تودع هذه الخلايا المزيد من الكولاجين ثم ترسّب الكالسيوم، فتتحول الأوريقات المرنة سابقاً إلى شفرات صلبة تشبه الصخر. حلّل الباحثون نسيج صمامي بشري ومجموعات كبيرة من بيانات التعبير الجيني ووجدوا أن مسار إشارياً مبنياً حول جزيء صغير يُدعى cGMP وإنزيمه الشريك بروتين كيناز G (PKG) كان مُثبَطاً بشكل ثابت في الصمامات المتكلّسة، في حين ارتفعت الجينات والبروتينات المرتبطة بتكوين العظام. كما أن الأشخاص الذين لديهم تكلس صمامي شديد كانوا يمتلكون مستويات أقل من cGMP في دمهم، وارتبط ذلك بمدى تضييق وعرقلة الصمامات لديهم.
إشارة واقية تختفي
للبحث عن السببية، استخدم الفريق فئراناً وخلايا صمامية بشرية مزروعة. طوّرت الفئران المعدّلة وراثياً لإنتاج كمية أقل من PKG أورقاً صمامية أثخن وأكثر تكلساً بعد إصابة محكمة لصمام الأبهر، وأظهرت صماماتها مستويات أعلى لبروتين رئيسي في تشكيل العظام. في خلايا صمامية بشرية نمت في طبق تحت ظروف تشجع تراكم الكالسيوم، أدى خفض PKG باستخدام أدوات جينية إلى تسريع هذا التحول الشبيه بالعظام. تشير هذه النتائج إلى أن إشارة cGMP‑PKG تعمل عادةً ككبح لإعادة برمجة الخلايا الضارّة في الصمام — وعندما يضعف هذا الكبح يتسارع التكلّس.
إعادة استخدام دواء لفشل القلب
ثم سأل الباحثون إن كان تعزيز هذا المسار قد يبطئ أو يغيّ ر التكلّس. اختبروا ثلاثة أدوية تزيد cGMP بطرق مختلفة، بما في ذلك فيريسغوات (vericiguat)، دواء معتمد لمرضى محددين بفشل القلب. في الخلايا الصمامية البشرية، قلّلت الأدوية الثلاثة جميعها الترسبات الكلسية ومؤشرات التحول الشبيه بالعظام، وكان لتيريسغوات التأثير الأقوى. كما خفّض فيريسغوات التكلّس في قطع صغيرة من نسيج الصمام البشري المحفوظ حياً خارج الجسم. في نموذجي فأر — أحدهما ناجم عن نظام غذائي عالي الكوليسترول والآخر عن إصابة ميكانيكية للصمام — أدى علاج يومي بالفيريسغوات إلى أوراق صمامية أنحف وأقل تكلساً وتدفق دم أفضل عبر الصمام، دون إضعاف قوة ضخ القلب. عندما قلّصوا PKG وراثياً، فقد فيريسغوات إلى حد كبير فوائده، مما يشير إلى أن PKG هو اللاعب الرئيسي في المسار السفلي.
تنظيف خلوي، صمامات أكثر صحة
بتعمق أكبر، وجد الفريق أن فيريسغوات وPKG حمى نوى الطاقة الصغيرة للخلايا، الميتوكوندريا. تحت ظروف التكلّس، تراكمت أنواع أكسجين تفاعلية ضارة، فُقد الجهد الغشائي الميتوكوندري، وانتجت الخلايا طاقة أقل. أعاد فيريسغوات أداء الميتوكوندريا وخفّض الضغط التأكسدي. وجّهت حِفَظات كبيرة من بيانات البروتينات وعلامات الفسفرة الانتباه إلى الالتهام الذاتي — نظام التنظيف وإعادة التدوير الداخلي للخلايا. في الصمامات البشرية المتكلسة، أظهرت التصوير المجهري وعلامات بروتينية انخفاضاً في تكوّن ونشاط الحويصلات الالتهامية، «أكياس النفايات» في الالتهام الذاتي. في تحليلات الخلية الواحدة، أظهرت عدة أنواع فرعية من خلايا الصمام المستخرجة من صمامات مريضة كبحاً واسعاً للبرامج المرتبطة بالالتهام الذاتي. في الخلايا المزروعة، أزال حظر الالتهام الذاتي الأثر الواقي لتنشيط PKG، ما يوحي بأن PKG يعمل إلى حد كبير بإحياء هذا النظام التنظيفي.
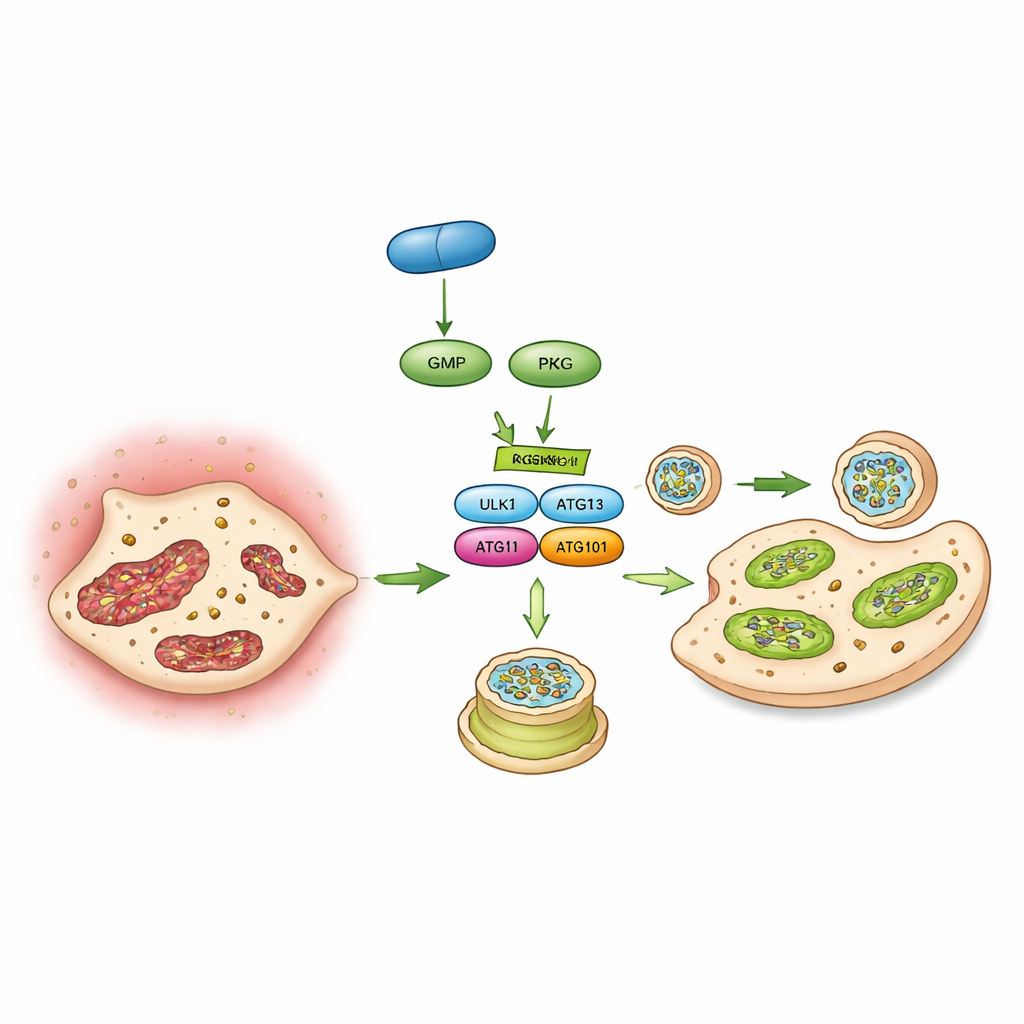
قلب مفتاح جزيئي
أخيراً، حدّد المؤلفون مفتاحاً جزيئياً يربط PKG بالالتهام الذاتي: بروتين يُدعى ULK1 يبدأ تكوّن الحويصلات الالتهامية. باستخدام الفوسفوبروتيوميات ودراسات التفاعل وتجارب كايناز في أنابيب الاختبار، أظهروا أن PKG يلحِق مباشرة مجموعة فوسفات إلى ULK1 في موقع محدد (حمض أميني يُدعى سيرين 556). عندما طُعِّم هذا الموقع بحيث لا يمكن تعديله، لم يعُد PKG قادراً على تعزيز الالتهام الذاتي أو منع التكلّس في خلايا الصمام. في الفئران، أدى دفع التعبير عن هذه الطفرة غير المستجيبة في ULK1 داخل خلايا الصمام أيضاً إلى إبطال قدرة فيريسغوات على حماية الصمام. معاً، ترسم هذه النتائج سلسلة أحداث: يحفّز فيريسغوات cGMP، الذي ينشط PKG، الذي يبدّل مفتاح ULK1، فيُحيي الالتهام الذاتي، فيحافظ على الميتوكوندريا ويمنع خلايا الصمام من التحول إلى خلايا مُكوِّنة للعظم.
ما الذي قد يعنيه هذا للمرضى
تضع هذه الدراسة محور cGMP–PKG–ULK1–الالتهام الذاتي كنظام دفاع مدمج ضد «صدأ» صمام الأبهر. في مرض الصمام المتكلس، يضعف هذا الدفاع مما يسمح للخلايا بتراكم الضرر والانجراف نحو هوية شبيهة بالعظم. من خلال استعادة الإشارة دوائياً باستخدام دواء مُستخدم بالفعل في عيادات فشل القلب، أبطأ الباحثون التكلّس في عدة نماذج تجريبية. وبينما ستكون هناك حاجة لتجارب بشرية في مرض الصمام، تقدّم الدراسة فكرة واضحة قابلة للاختبار: قد يؤدي تعزيز هذا المسار التنظيفي الخلوي بعناية في يوم من الأيام إلى تأخير أو تقليل الحاجة إلى جراحة استبدال الصمام لدى كبار البالغين المعرضين لخطر تضيق الأبهر.
الاستشهاد: Wang, Y., Xu, F., Song, C. et al. Cyclic guanosine monophosphate-protein kinase G signaling attenuates aortic valve calcification through ULK1-mediated autophagy. Sig Transduct Target Ther 11, 90 (2026). https://doi.org/10.1038/s41392-026-02624-5
الكلمات المفتاحية: مرض تكلس صمام الأبهر, إشارة cGMP PKG, فينيسيغوات (vericiguat), الالتهام الذاتي, تكلس صمامات القلب