Clear Sky Science · ar
فعالية وتأثير تعديل المناعة لخلايا CAR-T المصفحة بـ IL-7/XCL1 المستهدفة لـ Claudin18.2 في سرطانات الجهاز الهضمي: تحليل قبل سريري وسريرِي
توجيه جهاز المناعة ضد سرطانات الجهاز الهضمي
تعد سرطانات المعدة والبنكرياس من أكثر الأورام فتكًا، جزئيًا لأنها غالبًا ما تقاوم الجراحة والعلاج الكيميائي والإشعاعي. تستكشف هذه الدراسة نهجًا جديدًا لمكافحة هذه السرطانات من خلال تعزيز خلايا المناعة لدى المريض بحيث تستطيع دخول الأورام الصلبة، والبقاء فيها، واستدعاء تعزيزات مناعية. عن طريق إعادة تصميم خلايا T المقاتلة للسرطان لإفراز إشارات مناعية مفيدة، يهدف الباحثون ليس فقط إلى مهاجمة الأورام مباشرًة بل أيضًا إلى إيقاظ بقية جهاز المناعة داخل بيئة الورم العدائية.
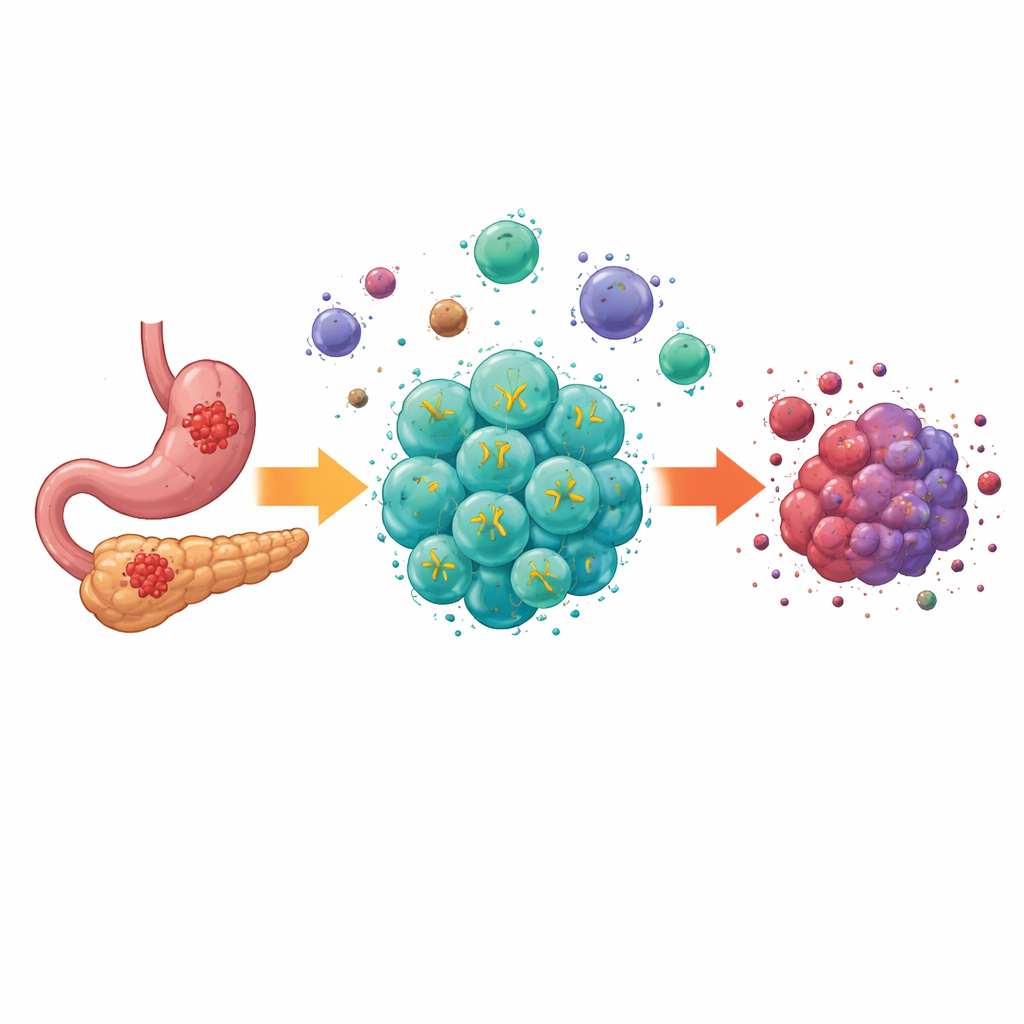
لماذا من الصعب علاج الأورام الصلبة
أنتجت علاجات الخلايا الحديثة المسماة CAR-T نتائج دراماتيكية في سرطانات الدم، شافية بعض المرضى الذين لم تكن لديهم خيارات أخرى. لكن الأورام الصلبة مثل تلك في الجهاز الهضمي تطرح عقبات إضافية. خلاياها متغايرة من مكان لآخر، ويعاني جوهر الورم نقصًا في المغذيات والأكسجين، ومزيج من الخلايا والمسارات الكابحة يضعف الهجمات المناعية. الأجيال السابقة من خلايا CAR-T كانت قادرة على التعرف على جزيئات الهدف في سرطانات الجهاز الهضمي، لكنها غالبًا ما فشلت في التوسع، والاستمرار، والقيام بوظائفها داخل هذه البيئة القاسية، مما حد من تأثيرها في العالم الحقيقي.
تصميم أذكى لخلايا T المهندسة
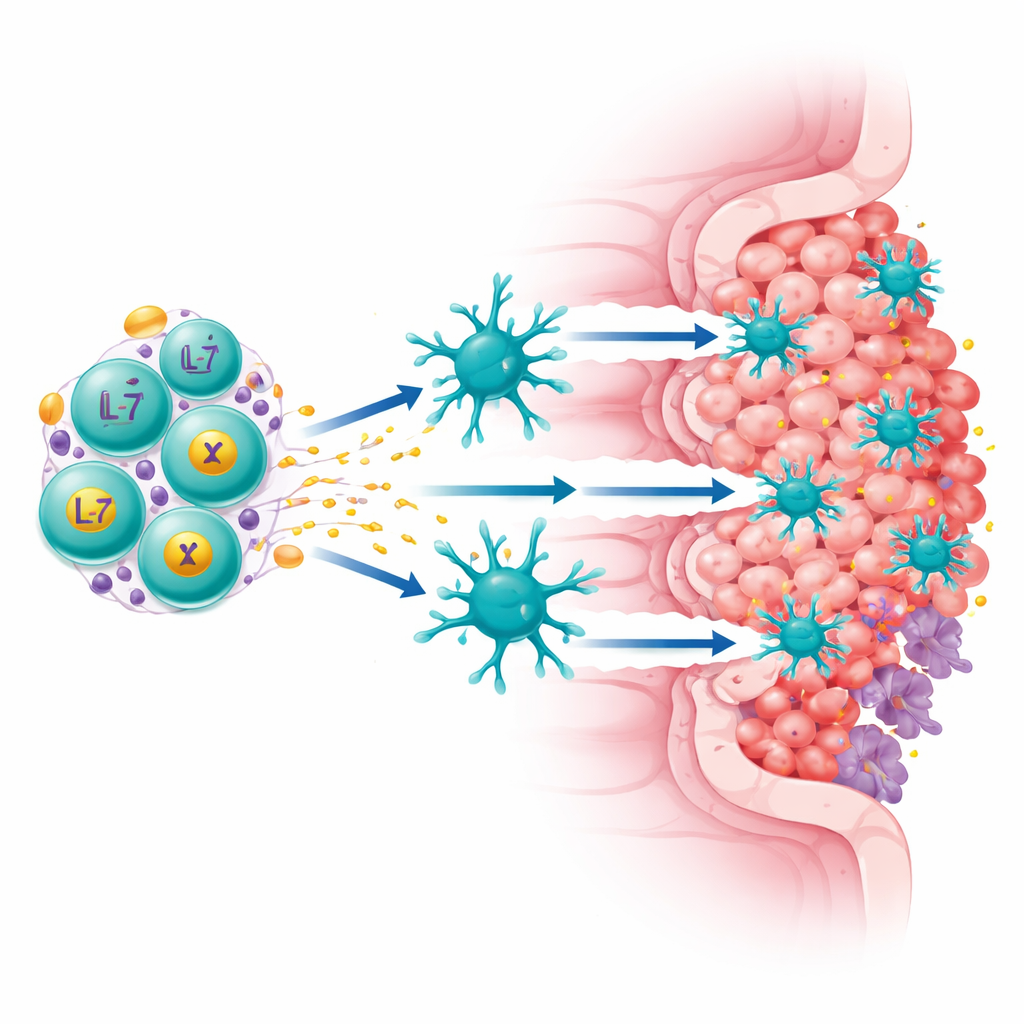
ركز الفريق على بروتين يسمى Claudin18.2، يوجد بمستويات عالية على العديد من خلايا سرطان المعدة والبنكرياس لكنه غائب إلى حد كبير عن الأنسجة الطبيعية. بنوا خلية CAR-T من "الجيل الرابع" تقوم بمهمتين في آنٍ واحد: تتعرف على Claudin18.2 على خلايا الورم وتفرز باستمرار عاملين معززين للمناعة، IL-7 وXCL1. يساعد IL-7 خلايا T على البقاء والحفاظ على حالة شبيهة بالجذعية طويلة العمر، بينما يعمل XCL1 كمنارة لجذب نوع نادر لكنه قوي من الخلايا المناعية يُدعى cDC1، وهو جيد بشكل خاص في تفعيل خلايا T القاتلة. هذه الخلايا المطورة، المسماة ExCAR-T أو RD07، صممت ليس فقط لقتل ما ترى بل لإعادة تشكيل المشهد المناعي داخل الورم.
تحكم قوي بالورم في النماذج قبل السريرية
في نماذج الفأر لسرطانات الجهاز الهضمي، تفوقت خلايا ExCAR-T على خلايا CAR-T التقليدية التي تفتقر إلى IL-7 وXCL1. في أطباق المختبر، قضت الخلايا المهندسة على مزيد من الخلايا السرطانية واحتوت على المزيد من خلايا T طويلة العمر الشبيهة بالذاكرة. في الحيوانات الحاملة لأورام موجبة لـ Claudin18.2، أدى علاج ExCAR-T إلى تقلص أعمق للأورام وإطالة البقاء مقارنة بخلايا CAR-T القياسية. توسعت الخلايا المحسنة بشكل أفضل في الدم وأطلقت نشاطًا مناعيًا أوسع، بما في ذلك إشارات تجند خلايا مناعية إضافية مع تقليل عوامل مرتبطة بانتشار الورم. اللافت أنه في الفئران التي شُفيت بواسطة ExCAR-T، رفضت تحديًا ثانويًا بخلايا سرطانية لم تعد تحمل هدف Claudin18.2، ما يشير إلى أن العلاج أثار ذاكرة مناعية طويلة الأمد على مستوى الورم بأكمله بدلاً من استجابة ضيقة لمستهدف واحد.
نتائج مبكرة من تجربة سريرية على المرضى
مشجَّعين بهذه البيانات، أطلق الباحثون تجربة أولى في الإنسان لـ RD07 شملت 12 شخصًا يعانون من سرطان متقدم في المعدة أو تقاطع المريء والمعدة، أو سرطان البنكرياس، والذين فشلوا في العلاجات القياسية. كانت الآثار الجانبية قابلة للإدارة عمومًا: معظم المشاكل الجسيمة كانت انخفاضًا في خلايا الدم ناتجًا عن العلاج الكيميائي قبل الحقن، وظهرت ردود فعل طفيفة لإطلاق السيتوكينات فقط؛ ولم تُسجل سمّية دماغية خطيرة. من بين 10 مرضى قابلين للتقييم، شهد 7 تقلصًا ملموسًا للأورام وحقق 2 استجابة جزئية. حقق المرضى الذين أظهرت أورامهم مستويات متوسطة إلى عالية من Claudin18.2 نتائج أفضل بشكل خاص، حيث شهد كل مريض منهم على الأقل استقرار المرض وبعضهم عاش شهورًا أطول بكثير من المتوقع. في هؤلاء المستجيبين، توسعت الخلايا T المعدلة بقوة أكبر في الدم، وارتفعت مستويات IL-7 وXCL1 في الدم، مما يتوافق مع تصميم العلاج.
نظرة داخل الحي المناعي للورم
لفهم كيفية عمل RD07 في البشر، فحص الفريق عينات ورمية بدقة خلوية مفردة قبل وبعد العلاج. لاحظوا أن نسبة الخلايا السرطانية الموجبة لـ Claudin18.2 انخفضت لدى المرضى المستجيبين، مما يؤكد أن العلاج استهدف الهدف المقصود. في الوقت نفسه، حدثت زيادة في تنوع نسخ خلايا T، بما في ذلك خلايا قاتلة نشطة وخلايا ذاكرة مقيمة نسيجيًا، مشيرةً إلى أن الجسم يشن هجومًا مناعيًا أوسع. أظهرت الخلايا التغصنية المتخصصة علامات نشاط متزايد وتفاعلات أقوى مع خلايا T المتكاثرة، متسقًا مع جذب XCL1 لها إلى داخل الورم. كشفت دراسات تصوير لمقطع ورم لأحد المرضى عن انخفاض في خلايا الورم والخلايا النخاعية الكابحة بعد العلاج، مع ازدياد في خلايا T وB وإعادة تنظيم النسيج إلى مناطق غنية بالمناعة، وهي سمات لبيئة دقيقة "أكثر سخونة" ومرتبطة بالالتهاب.
ما الذي قد يعنيه هذا لرعاية السرطان في المستقبل
بالجمع بين النتائج قبل السريرية والمبكرة السريرية، تشير البيانات إلى أن RD07 يفعل أكثر من مجرد إضافة دواء مستهدف آخر إلى ترسانة السرطان. بدمج تعرف على الورم مع دعم مناعي مدمج، تستطيع هذه الخلايا T المهندسة البقاء لفترة أطول، واستدعاء خلايا شريكة رئيسية، والمساعدة في تدريب جهاز المناعة لدى المريض ليحافظ على السرطان تحت السيطرة، حتى عندما يختفي الهدف الأصلي. ورغم أن التجربة كانت صغيرة ونُفذت على مرضى خضعوا لعلاجات مكثفة مسبقًا، فإن الانكماش المتكرر للأورام، والسمية المقبولة، وإعادة تشكيل مناعي عميق تبدو واعدة. إذا أكدتها دراسات أكبر، فقد يفتح هذا النهج فصلًا جديدًا في علاج سرطانات الجهاز الهضمي، حيث يصبح تمكين النظام البيئي المناعي داخل الورم أمرًا مهمًا بقدر الضربة الأولية للخلايا السرطانية نفسها.
الاستشهاد: Zhao, X., Liu, J., Zhang, Z. et al. Efficacy and immunomodulatory effect of Claudin18.2-specific IL-7/XCL1 armored CAR-T cells in digestive tract cancer: preclinical and clinical analysis. Sig Transduct Target Ther 11, 87 (2026). https://doi.org/10.1038/s41392-026-02621-8
الكلمات المفتاحية: علاج خلايا CAR-T, سرطان الجهاز الهضمي, البيئة الدقيقة للورم, Claudin18.2, المناعة العلاجية