Clear Sky Science · ar
بروتين شبيه فيزينين 1 يعطل توازن الكالسيوم ويعزز الرجفان الأذيني في نماذج بشرية وقوارض
لماذا تهم هذه القصة عن إيقاع القلب
الرجفان الأذيني هو اضطراب شائع في إيقاع القلب يزيد من خطر السكتة القلبية وفشل القلب. يعيش كثيرون معه، ومع ذلك يظل الأطباء يواجهون صعوبة في منعه أو منع عودته بعد العلاج. تكشف هذه الدراسة عن بروتين كان مهملًا سابقًا داخل خلايا القلب، يُدعى VILIP-1، يعمل كقاطع خاطئ للكالسيوم ويسهم في دفع حدوث الرجفان الأذيني لدى البشر والحيوانات. من خلال تحديد هذا القاطع وإظهار أن أدوية متوافرة يمكن أن تخفّض نشاطه، تفتح هذه الأبحاث طريقًا جديدًا نحو علاجات أكثر أمانًا واستهدافًا.
نظرة أعمق على نبض فوضوي
في قلب سليم، تنتشر الموجات الكهربائية بشكل منتظم عبر الحجرات العلوية أو الأذينين، موجهة كل نبضة قلب. يعتمد هذا الانتظام بشكل كبير على الكالسيوم، المعدن المشحون الذي يدخل ويخرج من خلايا القلب لتنسيق الانقباض والاسترخاء. في الرجفان الأذيني، يصبح تداول الكالسيوم فوضويًا: تسريبات إضافية وتقلبات في مستويات الكالسيوم تثير إشارات كهربائية شاردة قد تتصاعد إلى نظم سريع وغير منتظم. لطالما عُرف أن سوء تعامل الكالسيوم محوري في هذا الاضطراب، لكن المشغلات الأولية التي تُشعل هذه الفوضى بقيت غامضة.
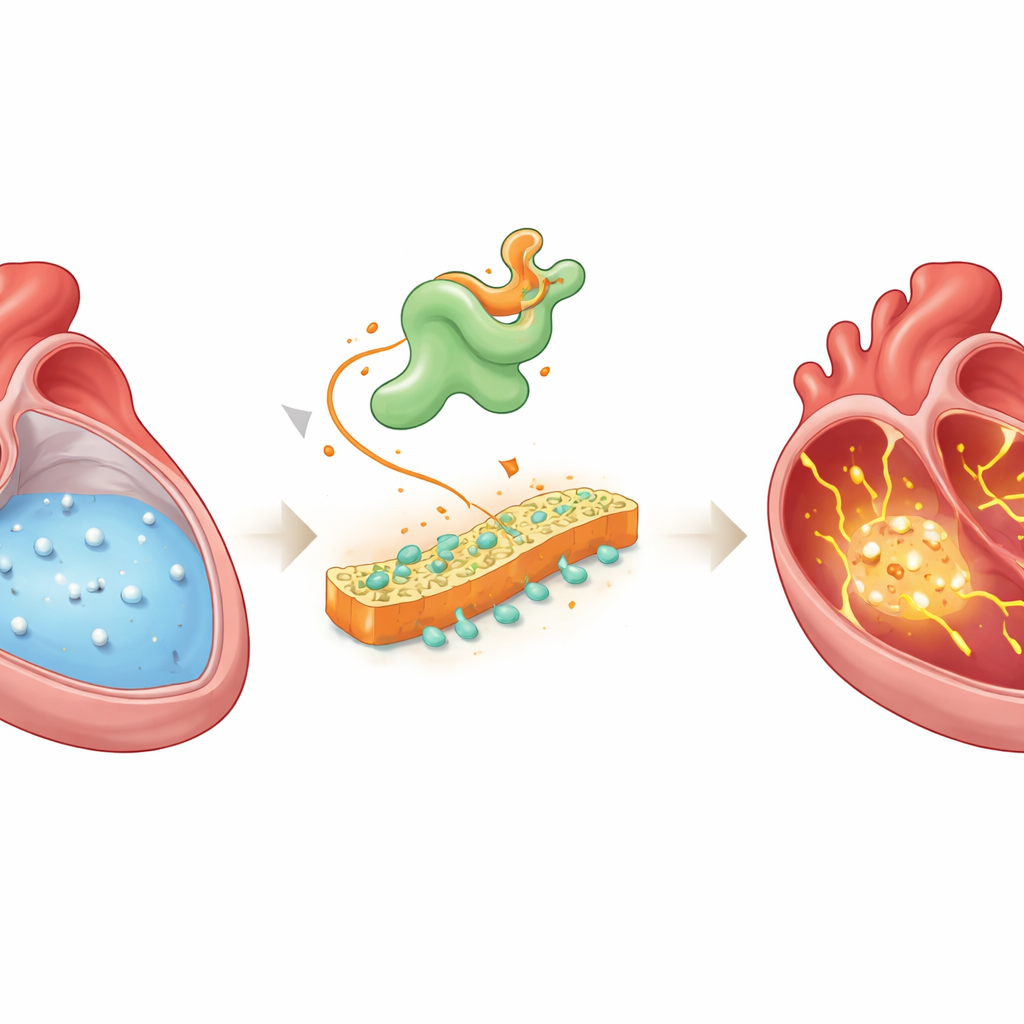
اكتشاف المسبب الخفي
جمع الباحثون عدة منهجيات متقدمة للبحث عن جزيئات تربط بين اضطراب تعامل الكالسيوم والرجفان الأذيني. سجلوا إشارات الكالسيوم من مئات الخلايا الأذينية المنفردة في جرذان شُغلت لديهم رجفان أذيني عبر التحفيز السريع، ثم سلَّلوا مجموعة الجينات النشطة بالكامل في تلك الخلايا نفسها. كما قارنوا نشاط الجينات في نسيج أذيني من مرضى بالرجفان الأذيني مع مرضى لديهم إيقاع طبيعي. عند تراكب هذه المجموعات وتتبع كيفية تحول الخلايا من الحالة السليمة إلى المريضة، برزت جين واحد مرارًا وتكرارًا: Vsnl1، الذي يُنتج بروتين VILIP-1، وهو مستشعر للكالسيوم جرى دراسته سابقًا بشكل أساسي في الدماغ والبنكرياس وليس في القلب.
كيف يخلّ VILIP-1 بتوازن الكالسيوم
في نسيج الأذين لدى كل من المرضى والنماذج الحيوانية، كانت مستويات VILIP-1 أعلى بكثير، وكان البروتين مركّزًا عند سطح الخلية. لاختبار ما إذا كان هذا التغير مجرد مرافق أم عامل مسبب، أجبر الفريق خلايا الأذين القلبية في الفئران على إنتاج كميات زائدة من VILIP-1. لم تظهر على هذه الفئران أضرار بنيوية واضحة في القلب، لكن أذينها أصبح أسهل بكثير للدفع إلى الرجفان الأذيني أثناء التحفيز الكهربائي. أظهرت تسجيلات كهربائية مفصلة زيادة في بعد الاستقطابات المتأخرة—وهي نبذات غير طبيعية بعد كل نبضة—وتناوبًا من نبضة إلى أخرى في شكل الجهد الفعّال، وهي علامات كلاسيكية لسلوك كهربائي غير مستقر مرتبط بزيادة تحميل الكالسيوم. أكدت صور الكالسيوم عالية الدقة موجات كالسيوم عفوية متكررة واستنزاف مخازن الكالسيوم الداخلية، مما يدل على تسرب شديد داخل الخلايا.
الشريك الحاسم على سطح الخلية
لفهم كيفية تسبب VILIP-1 في هذا الاضطراب، رسم العلماء خريطة البروتينات المتفاعلة معه داخل خلايا القلب. باستخدام طريقتين تكميليتين—سحب الشركاء المرتبطين من نسيج الأذين وووسم البروتينات المجاورة بحلقة بيوتن في خلايا حية—ركزوا الاهتمام على NCX-1، وهو مبادل الصوديوم-الكالسيوم الرئيسي في غشاء سطح القلب. هذا المبادل يساعد عادة على طرد الكالسيوم مقابل دخول الصوديوم، لكن في ظروف معينة يمكن أن يعمل بالعكس ويدفع الكالسيوم إلى داخل الخلية. أظهرت الدراسة أن VILIP-1 يرتبط ماديًا بـ NCX-1 ويزيد عدد جزيئات NCX-1 المتموضعة في الغشاء دون زيادة إجمالية في إنتاج NCX-1. نتيجة لذلك، أصبحت تيارات المبادل أكبر، وإيقاف NCX-1 بمثبط انتقائي قلّل موجات الكالسيوم وجعل من الأصعب إحداث الرجفان الأذيني في فئران ذات VILIP-1 زائد.
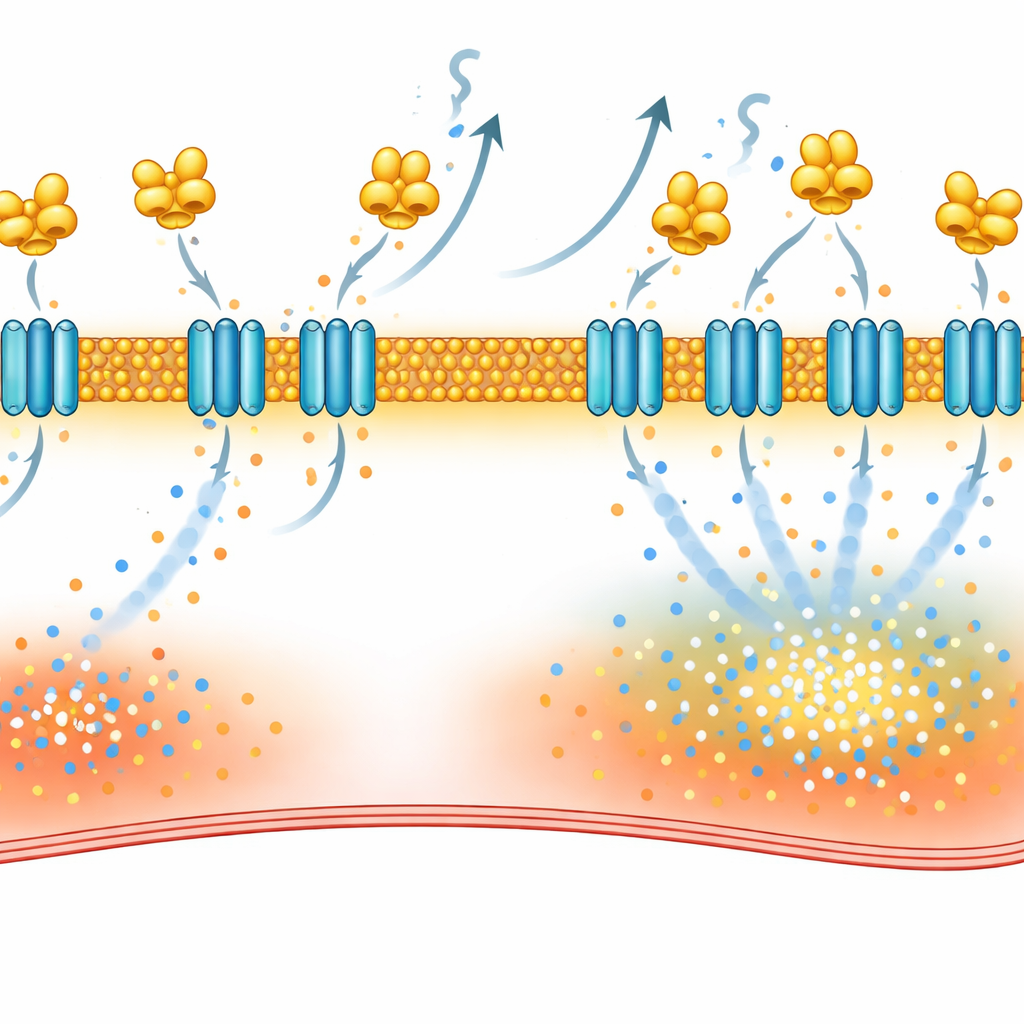
إطفاء القاطع المعطوب بأدوية متاحة
يرتبط VILIP-1 بالغشاء عبر وسم دهني يُدعى الميستويّت، والذي يتعرَض عندما يرتبط الكالسيوم بالبروتين. استخدم الفريق الديسلوراتادين، الذي أُظهر سابقًا أنه يتداخل مع خطوة وضع هذا الوسم، ووجدوا أنه خفّض مستوى NCX-1 على سطح الخلية، وطَبّع تيارات المبادل، وقلل موجات الكالسيوم، وخفّض نوبات الرجفان الأذيني في نماذج الجرذان. كما اختبروا الريباغلينايد، دواء لمرض السكري معروف بارتباطه بحساسات كالسيوم ذات صلة. أكدت تجارب بيوفيزيائية أن الريباغلينايد يرتبط مباشرةً بـ VILIP-1. في جرذان محفزة ونسيج أذيني من مرضى بالرجفان الأذيني، قلّ علاج الريباغلينايد من NCX-1 عند الغشاء، وهدأ تسرب الكالسيوم في خلايا مفردة، وخفّض بشكل كبير سهولة إثارة الرجفان الأذيني.
ماذا يعني هذا للمرضى الذين يعانون من عدم انتظام ضربات القلب
تبيّن الدراسة إجمالًا حلقة تعزيز ذاتي: ارتفاع مستويات الكالسيوم يجند VILIP-1 إلى سطح الخلية، حيث يزيد NCX-1، وهو ما يؤدي بدوره إلى مزيد من زيادة الكالسيوم ويعد الأرضية لحدوث الرجفان الأذيني. من خلال قطع هذه الحلقة على مستوى VILIP-1—إما بمنع وسمه الدهني أو بالارتباط بنواة استشعار الكالسيوم—يمكن للأدوية المتاحة أن تعيد توازن الكالسيوم بشكل أكثر استقرارًا وتقلل قابلية النسيج للاضطراب في أنسجة قلب بشرية وقوارض. وبينما هناك حاجة لمزيد من العمل لتحسين خصوصية الأدوية واختبار هذه الاستراتيجيات في نماذج حيوانية أكبر والتجارب السريرية، يظهر VILIP-1 الآن كمقبض واعد جديد للوقاية والعلاج من هذا الاضطراب الواسع والعنيد في كثير من الأحيان.
الاستشهاد: Xiong, K., Wang, G., Li, D. et al. Visinin-like protein 1 disrupts calcium homeostasis and promotes atrial fibrillation in human and rodent models. Sig Transduct Target Ther 11, 105 (2026). https://doi.org/10.1038/s41392-026-02615-6
الكلمات المفتاحية: الرجفان الأذيني, إشارة الكالسيوم, عدم انتظام ضربات القلب, مبادل الصوديوم-كالسيوم, أهداف علاجية