Clear Sky Science · ar
إشارة الفبرينوجين–Bmal1 كهدف علاجي للحد من تمزق الشريان الأورطي عن طريق الحفاظ على انقباض الخلايا العضلية الوعائية
لماذا يهم الحارس الخفي في الأبهر
يعد تمزق الأبهر من أخطر حالات الطوارئ في الطب: فقد يتمزق الشريان الرئيسي الخارج من القلب فجأة، غالبًا دون سابق إنذار، ويموت العديد من المرضى خلال ساعات. قد تنقذ الجراحة الأرواح، لكنها مخاطرة وليست متاحة دائمًا فورًا. تستكشف هذه الدراسة حليفًا غير متوقع موجودًا بالفعل في دمنا — الفبرينوجين، وهو بروتين التجلط — وتبيّن أنه إلى جانب دوره في إيقاف النزف، قد يساعد فعلاً في تثبيت الأبهر وإبطاء تقدم المرض، مما يمنح الأطباء وقتًا ثمينًا للتدخل.
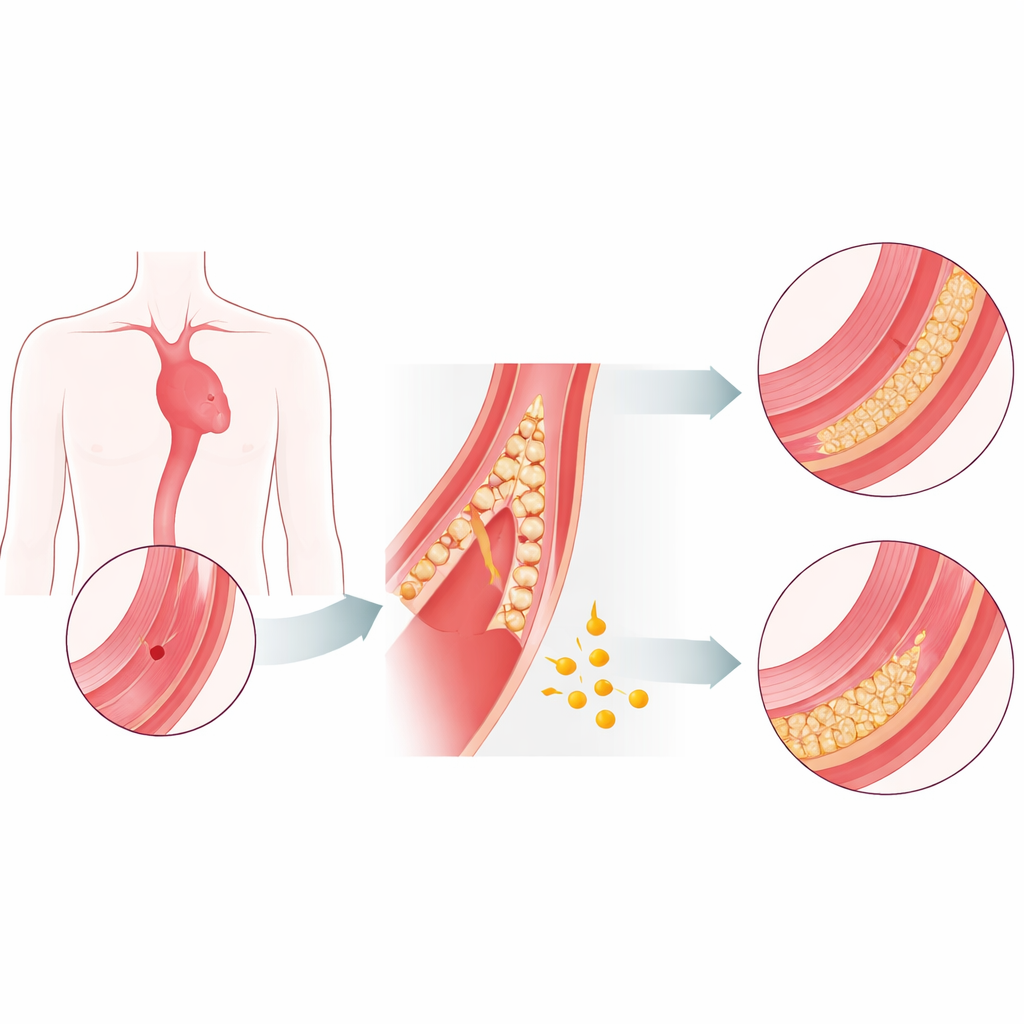
قاتل صامت بحاجة إلى خيارات جديدة
يبنى الأبهر مثل خرطوم قوي متعدد الطبقات. عندما تضعف طبقاته الداخلية وتنشق، يمكن للدم أن يتدفق داخل جدار الشريان ويفصله — هذا هو تمزق الأبهر. في المراحل المبكرة الخطرة، يزيد خطر الوفاة ساعة بساعة، وغالبًا ما تكون الجراحة الطارئة هي الخيار الوحيد. المرضى الذين يصمدون بما يكفي للوصول إلى مرحلة أكثر استقرارًا يعانون نتيجة أفضل بكثير. لا توجد اليوم أدوية مثبتة تبطئ عملية التمزق أو تقوّي جدار الأبهر بشكل موثوق. انطلق الباحثون لمعرفة ما إذا كان الفبرينوجين، البروتين الدموي الشائع المعروف بدوره في التجلط، قد يعمل أيضًا كمثبت طبيعي للأبهر.
دلائل من المرضى: المزيد من الفبرينوجين، بقاء أفضل
فحص الفريق أولاً 310 مرضى يعانون من تمزق أورطي حاد لم يتمكنوا من الخضوع للجراحة وعولجوا بالأدوية فقط. قارنوا بين الناجين أثناء إقامتهم بالمستشفى وغير الناجين. كان لدى المرضى الذين توفوا عادة مستويات فبرينوجين أقل بكثير في الدم. عندما صنف الباحثون المرضى حسب مستوى الفبرينوجين، وجدوا أن المستويات المنخفضة جدًا (أقل من 2 غرام لكل لتر) ارتبطت بمعدلات وفاة أعلى بكثير، بينما ارتبطت المستويات العالية (أكثر من 4 غرام لكل لتر) ببقاء أفضل. اقترح هذا النمط أن الفبرينوجين لم يكن مجرد مشاهد محايد بل قد يساعد فعليًا الأبهر على مقاومة المزيد من التمزق.
مراقبة تمزق وشفاء الأبهر في الفئران
للانتقال من الارتباط إلى اختبار السببية، استخدم العلماء نماذج فأرية تُحفَّز فيها جدران الأبهر على الضعف والتمزق. في هذه الحيوانات، كان الفبرينوجين عادة غائبًا عن جدار الأبهر السليم، لكن مع تطور المرض بدأ يتسرب إلى الطبقة الوسطى حيث توجد الخلايا العضلية الملساء. اللافت أن أعظم تراكم للفبرينوجين ظهر في مقاطع متضررة بشدة لكنها لم تتمزق بعد، مما يوحي بأن وجوده قد يساعد في منع انطلاق الجدار. عندما استخدم الباحثون علاجًا جينيًا لتقليل إنتاج الفبرينوجين في الكبد، ساءت حالات التمزق: تمددت الأبهرة أكثر، زاد الضرر البنيوي، ومات عدد أكبر من الفئران. إعادة إعطاء فبرينوجين منقى عكست هذه التأثيرات. أظهرت تجارب مستقلة باستخدام نموذج مختلف لتوسع الأبهر اتجاهًا وقائيًا مشابهًا، مما عزز الحجة أن الفبرينوجين يحرس جدار الوعاء بنشاط.
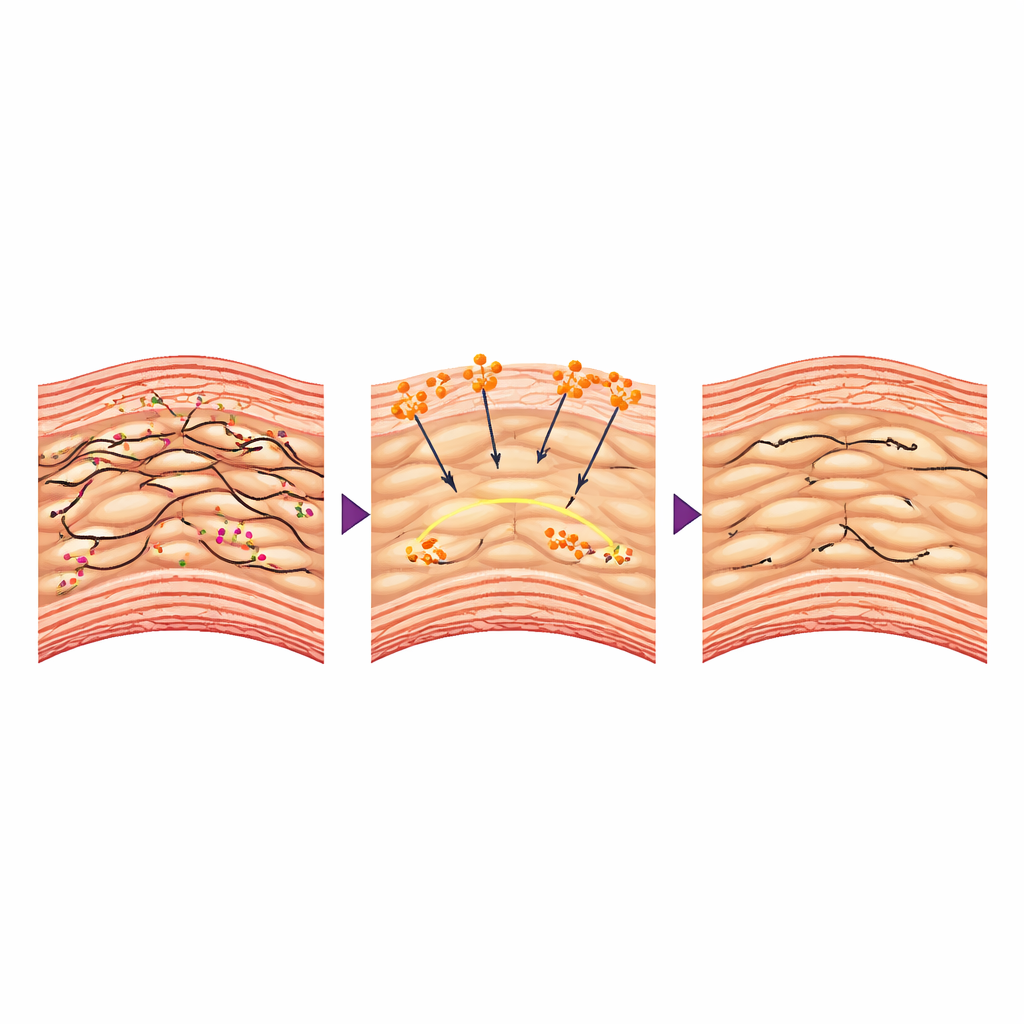
الحوار الخفي بين بروتين الدم وخلايا العضلات
كيف يمكن لبروتين التجلط أن يحمي الأبهر من الداخل؟ ركز المؤلفون على الخلايا العضلية الملساء الوعائية، الخلايا القابضة التي تشكل الطبقة الوسطى من الأبهر وتعمل كـ«حلقات تقوية» حية. في المرض، غالبًا ما تفقد هذه الخلايا حالتها الضيقة والقابضة وتتحول إلى شكل أكثر رخاوة وتصنيعية يفسد النسيج المحيط. وجدت الدراسة أنه عندما دخل الفبرينوجين جدار الأبهر، تفاعل مع مستقبلات محددة على هذه الخلايا وساعد في الحفاظ على السقالة الداخلية من خيوط الأكتين. كانت الخلايا العضلية الملساء من الحيوانات المعالجة أكثر صلابة، تنقبض بقوة أكبر في الاختبارات، وعبرت عن مزيد من علامات «الانقباض» وأقل من البروتينات التي تهدم المصفوفة الداعمة. على مستوى الجينات، خفّض الفبرينوجين نشاط Bmal1، المنظم الرئيسي المرتبط بساعة الجسم، والذي في هذا السياق دفع تغييرات ضارة في سلوك الخلايا العضلية. إعادة رفع مستوى Bmal1 ألغت فوائد الفبرينوجين، ما أظهر أن هذا المسار الإشاري كان محورياً للتأثير الوقائي.
من الآلية إلى العلاج المحتمل
نظرًا لأن الفبرينوجين يقود أيضًا التجلط، تساءل الفريق عما إذا كانت فائدته مجرد نتيجة لتشكيل جلطات أقوى. باستخدام مميع دم قوي لحجب الثرومبين — الإنزيم الذي يحول الفبرينوجين إلى جلطة صلبة — أظهروا أن الفبرينوجين لا يزال يحمي الأبهر حتى عندما تعطلت عملية التجلط إلى حد كبير. أخيرًا، اختبروا جرعات مختلفة ووجدوا أن كميات كافية فقط من الفبرينوجين المضافة أبطأت المرض، خفضت حالات التمزق، وحافظت على بنية النسيج. معًا، تصوّر هذه النتائج الفبرينوجين كمُركب ذي غرض مزدوج: عند مستويات أعلى، يمكن للفبرينوجين الكامل أن يدخل جدار الأبهر الضعيف، يهدئ مسار إشاري ضار في الخلايا العضلية الملساء، ويساعدها على البقاء قوية وقابضة. بالنسبة للمرضى، يفتح هذا الاحتمال أن تُصبح تسريعات الفبرينوجين المحسوبة يومًا ما علاجًا شبيهاً بالدواء لإبطاء تمزق الأبهر وتمديد نافذة الوقت الآمنة للجراحة المخططة المنقذة للحياة.
الاستشهاد: Zhong, X., Li, D., Zhao, Y. et al. Fibrinogen–Bmal1 signaling as a therapeutic target to limit aortic dissection by preserving VSMC contractility. Sig Transduct Target Ther 11, 103 (2026). https://doi.org/10.1038/s41392-026-02610-x
الكلمات المفتاحية: تمزق الشريان الأورطي, فبرينوجين, الخلايا العضلية الملساء الوعائية, إشارة Bmal1, توسع الشريان الأورطي