Clear Sky Science · ar
التآزر الكيماوي‑الضوئي يشعل مناعة مضادة للأورام عبر الفيروبتوز
تحويل حرارة الجسم والضوء إلى محارب للسرطان
يمكن لعقاقير العلاج الكيميائي أن تقلص الأورام، لكنها غالباً ما تصاحبها آثار جانبية شديدة ولا تضمن دائماً منع عودة السرطان. تستكشف هذه الدراسة طريقة جديدة لجعل دواء قائم بالفعل، دوكيتاكسيل، يعمل بذكاء أكبر وبقوة أعلى عبر تعبئته في جسيمات دقيقة تستجيب للحرارة وتشغيلها بضوء قريب من تحت الأحمر. الهدف ليس فقط قتل خلايا الورم بشكل أكثر دقة، بل أيضاً إيقاظ الجهاز المناعي ليتمكن من التعرف على السرطان ومطاردته في أنحاء الجسم ومنع الانتكاسات المستقبلية. 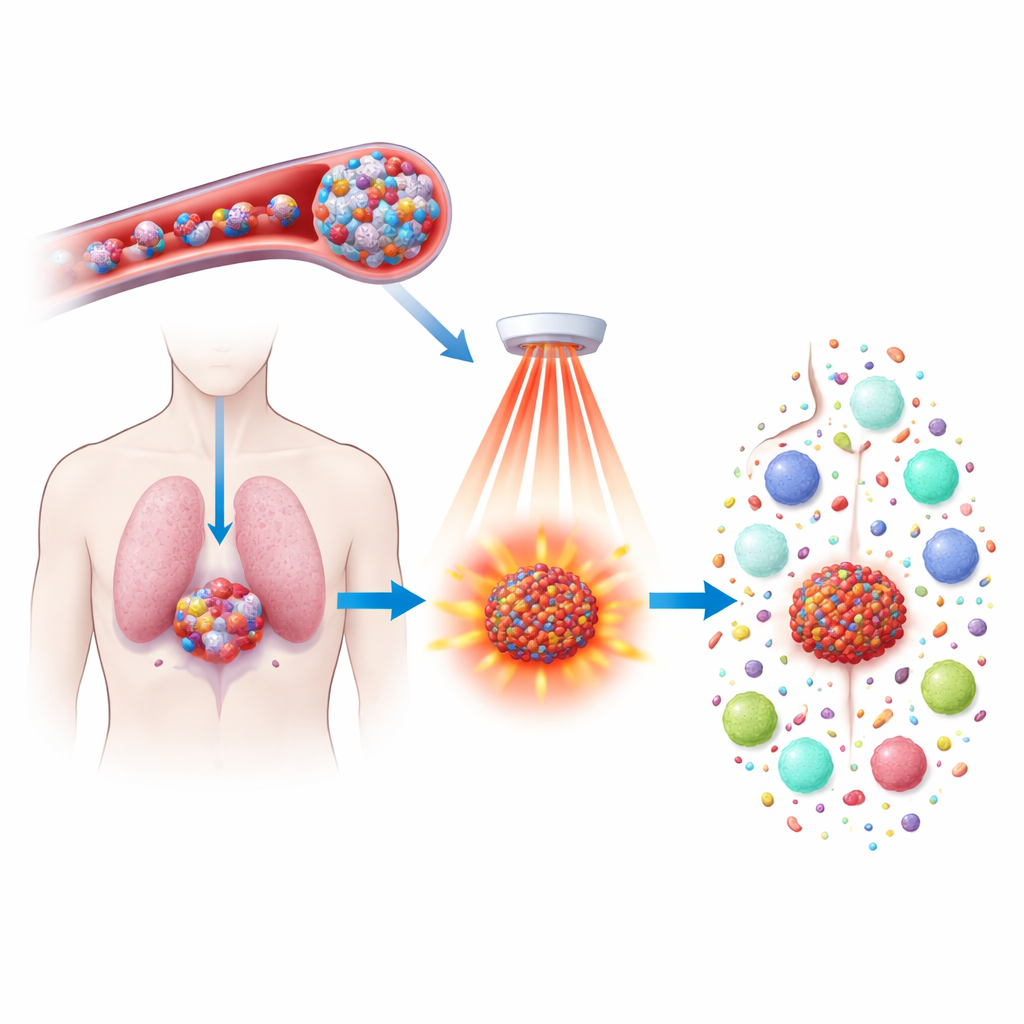
سعاة صغار يعرفون إلى أين يذهبون
بنى الباحثون نوعاً جديداً من الجسيمات النانوية من بوليمر يحتوي على فيروسين، وهو جزيء حامِل للحديد يتفاعل بقوة مع بيروكسيد الهيدروجين—المؤكسد الموجود بكميات أعلى داخل الأورام مقارنة بالأنسجة السليمة. هذه البوليمرات تتجمع ذاتياً إلى كريات محبة للماء قادرة على حمل كل من الدوكيتاكسيل وصبغة ماصة للضوء تسمى IR808. بعد الحقن في مجرى الدم، تكون الجسيمات صغيرة ومستقرة بما يكفي للدوران والتسرب إلى الأورام، حيث تبدأ الأوعية الدموية المسربة ومستويات بيروكسيد الهيدروجين المرتفعة في إضعاف الجسيمات وإطلاق حمولتها تدريجياً. هذا التصميم يركّز العلاج داخل الأورام مع تقليل الضرر للأعضاء السليمة.
استخدام الضوء لتعزيز التلف الموضعي
يُسلط ضوء قريب من تحت الأحمر، القادر بأمان على اختراق الأنسجة، نحو منطقة الورم. يمتص IR808 داخل الجسيمات هذا الضوء ويحوّله إلى حرارة بينما يولّد أيضاً أنواعاً تفاعلية من الأكسجين. يؤدي توافر بيروكسيد الهيدروجين المنتج داخل الورم ومؤكسدات مدفوعة بالضوء إلى تفكك الجسيمات بسرعة أكبر وإفراز الدواء في المكان المطلوب بالضبط. في الوقت ذاته، يساعد الحديد داخل جزء الفيروسين على تحويل هذه المؤكسدات إلى أشكال شديدة العدوانية تهاجم المكونات الدهنية لغشاء الخلايا. هذا الهجوم الكيميائي والحراري المستهدف يزيد بشكل حاد من قدرة القتل مقارنةً بالدوكيتاكسيل أو العلاج الضوئي بمفردهما. 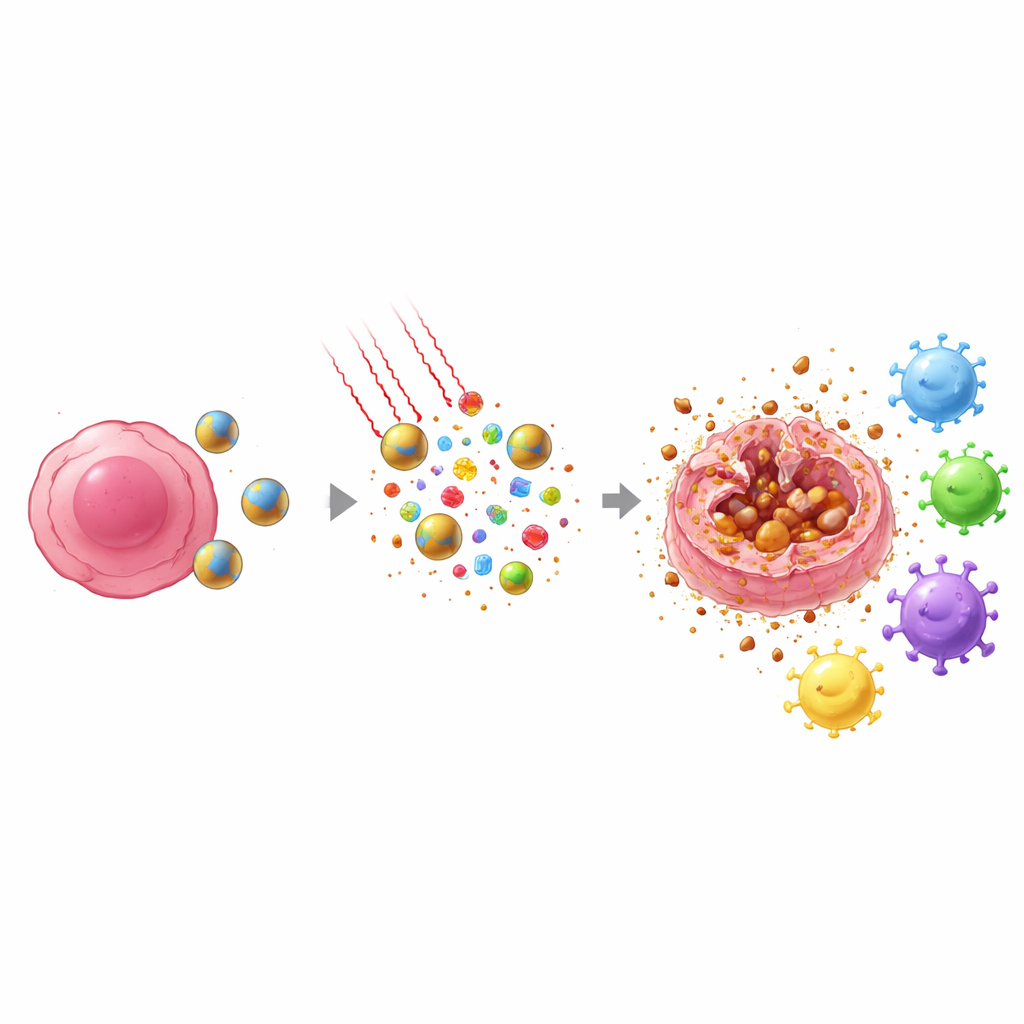
حرق مسيطر عليه يبعث إشارات إلى الجهاز المناعي
والأهم أن طريقة موت خلايا الورم تحت هذا العلاج تختلف عن العلاج الكيميائي التقليدي. بدلاً من التحلل بهدوء إلى شظايا مرتبة، تمر العديد من الخلايا بعملية تُسمى الفيروبتوز، وهي شكل من الموت المعتمد على الحديد ويُلحق ضرراً بالدهون يؤدي إلى تمزق الغشاء الخارجي. عندما يحدث ذلك، تُفرِغ الخلايا إشارات إنذار داخلية وشظايا خاصة بالورم إلى المحيط. في الوقت نفسه، يدفع الدوكيتاكسيل بروتيناً نووياً رئيساً، HMGB1، نحو حافة الخلية، مهيئاً إياه للإفراز. معاً، تخلق الحرارة والمؤكسدات وأثر الدواء دفعة من إشارات الخطر والمستضدات التي تستطيع خلايا الحراسة المناعية القريبة—الخلايا الشجيرية—كشفها ونقلها إلى العقد اللمفاوية.
من هجوم موضعي إلى دفاع على مستوى الجسم بأكمله
في نماذج أورام الفئران، لم يقتصر تأثير هذا العلاج الكيماوي‑الضوئي المركب على تصغير الأورام المعالجة بالحرارة المباشرة بفعالية أكبر من أي مكوّن منفرد، بل غيّر أيضاً المشهد المناعي. أظهرت الأورام مزيداً من خلايا شجرية ناضجة وأعداداً أكبر من خلايا T القاتلة، سواء داخل الورم نفسه أو في العقد اللمفاوية المصروفة. في بعض الفئران التي تملك جهازاً مناعياً سليماً، اختفت الأورام الأولية بعد دورتين علاجيتين فقط. عندما زرع العلماء لاحقاً أوراماً جديدة في مواقع بعيدة أو في الجانب المقابل، تباطأت هذه النتوءات الثانوية أو كُبِحت، مما يشير إلى أن الحيوانات طورت شكلاً من الذاكرة المناعية الخاصة بالسرطان. إضافة جسم مضاد يعيق نقاط التفتيش التي تمنع استنفاد خلايا T خفضت كذلك انبثاثات الرئة وامتدت البقاء، ما يوحي بأن هذا العلاج الموضعي يمكن دمجه مع العلاجات المناعية الحديثة.
لماذا هذا مهم لرعاية السرطان في المستقبل
للشخص غير المتخصص، الخلاصة هي أن هذه الاستراتيجية تحوّل الدوكيتاكسيل من سم نظامي عشوائي إلى جزء من استراتيجية مضادة للسرطان متعددة المراحل وذكية. عبر تعبئة الدواء في جسيمات نانوية تحتوي على الحديد وتُفعل بالضوء وتستجيب لكيمياء الورم نفسها، يُوَجَّه العلاج لإحداث مزيد من الضرر داخل الأورام مع حماية الأنسجة السليمة. نمط موت الخلايا الذي يثيره يعمل كنوع من التطعيم داخل الورم، يعلم الجهاز المناعي التعرف على السرطان وتذكره. إذا تُرجمت هذه النتائج إلى البشر، فقد تساعد أنظمة الكيماوي‑الضوئي هذه على تحويل الأورام المقاومة "الباردة" إلى أورام "ساخنة" تستجيب أفضل بكثير للعلاجات المناعية، مما يقلل احتمالية الانتكاس ويحسّن السيطرة طويلة الأمد.
الاستشهاد: Lin, J., Yang, H., Zou, Z. et al. Chemo-photothermal synergy ignites antitumor immunity via ferroptosis. Sig Transduct Target Ther 11, 98 (2026). https://doi.org/10.1038/s41392-026-02608-5
الكلمات المفتاحية: طب نانوي للسرطان, العلاج بالحرارة الضوئية, الفيروبتوز, المناعة ضد السرطان, توصيل دوكيتاكسيل