Clear Sky Science · ar
برو دراغ من نانوزيم تنسيقي موصل يطلق البيروبتوز وال كوبروبتوز وال فيروبتوز بدقة لتحصين السرطان في الموقع
تحويل الأورام إلى لقاحات ضد نفسها
عادة ما يهدف علاج السرطان إلى قتل خلايا الورم مباشرة، لكن ماذا لو أمكن تحويل الورم إلى لقاح ضد نفسه؟ تصف هذه الدراسة «برو دراغ» نانوي ذكي يسافر بأمان في الجسم، وينشط فقط داخل الأورام، ثم يجبر خلايا السرطان على الموت بطريقة تنبه الجهاز المناعي بقوة. النتيجة ليست فقط تقلص الأورام الأولية، بل تدريب الجسم على ملاحقة الأورام والانبثاثات البعيدة.
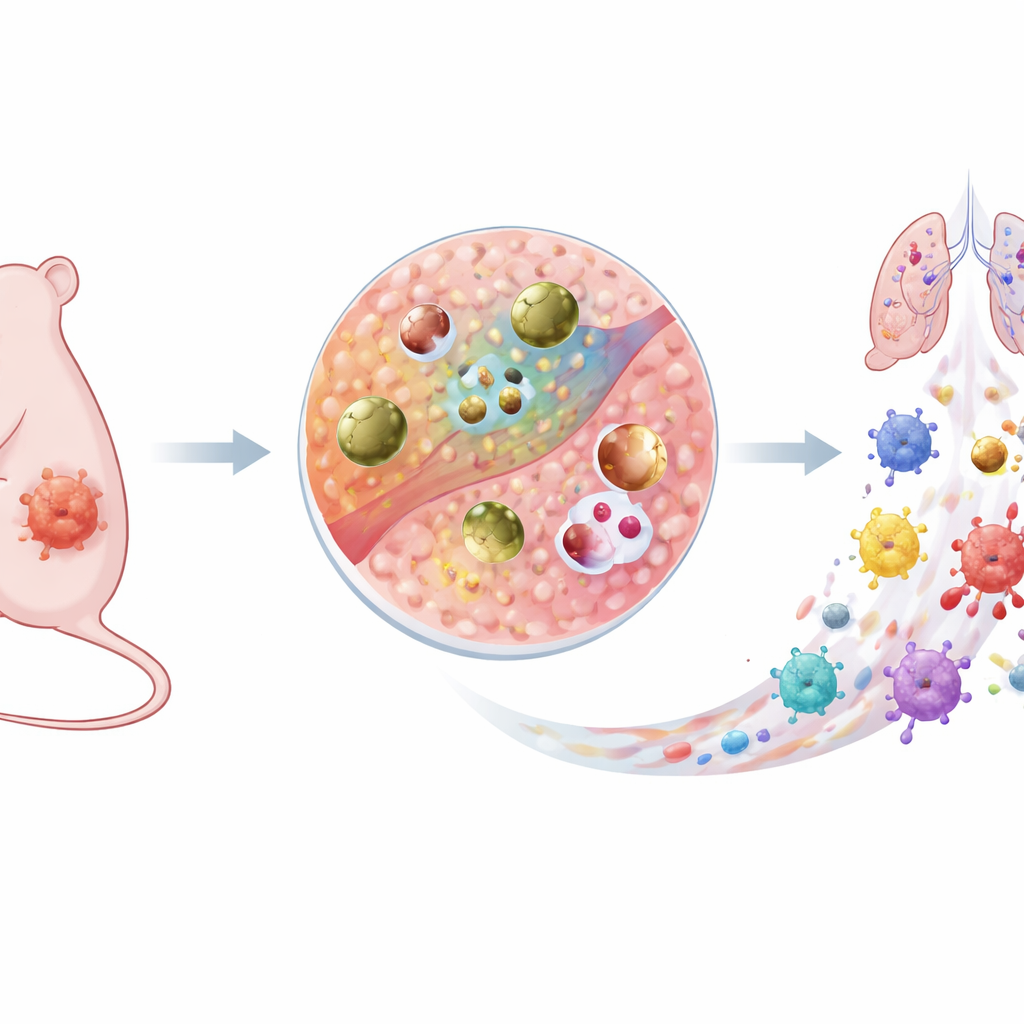
نوع جديد من السلاح الذكي ضد السرطان
بنَى الباحثون جسيمًا نحيفًا قائمًا على النحاس يسمى Cu–DHN يتصرف كدواء خامد أثناء التداول ويصبح مقاتلًا قويًا للسرطان بمجرد وصوله إلى الورم. يتكون من أيونات نحاس، وجزيء سلفي غير ضار (1،5-ديهيدروكسي نافثالين، أو DHN)، والحمض الأميني سيستئين. معًا يشكلون شبكة تنسيقية موصلة، مما يعني أن الإلكترونات يمكنها التحرك بسهولة عبر الجسيم. يسمح هذا «الطريق السريع للإلكترونات» الداخلي للنانوجسيم كله، وليس سطحه فقط، بالمشاركة في التفاعلات الكيميائية. والأهم أن Cu–DHN مصمم للاستجابة فقط لكيمياء البيئة الميكروية غير الاعتيادية للورم، حيث تكون مستويات الجلوتاثيون ومؤكسيد الهيدروجين مرتفعة بشكل غير طبيعي.
كيف تقلب كيمياء الورم مفتاح التشغيل
داخل الأورام، يعمل Cu–DHN كإنزيم اصطناعي. في وجود الجلوتاثيون ومؤكسد الهيدروجين معًا، يستخدم أولاً الجلوتاثيون لإعادة ضبط أيونات النحاس إلى حالة شديدة التفاعل ثم يستخدم مؤكسد الهيدروجين لتوليد دفعة مستمرة من المؤكسدات العدوانية للغاية (جذور الهيدروكسيل). تؤدي هذه المؤكسدات عملًا مزدوجًا: فهي تتلف مكونات الخلايا وتحول DHN غير الضار المحبوس داخل الجسيم إلى جوغلون، وهو مركب مضاد للسرطان قوي. يقوم الجوغلون بدوره بكبح دفاعات الورم المضادة للأكسدة ويزيد مستويات مؤكسد الهيدروجين، مكوّنًا حلقة تضخيم ذاتي للإجهاد التأكسدي تبقى محصورة داخل الورم، لأن الأورام وحدها توفر المدخلات الكيميائية المناسبة لبدء هذه الدورة.
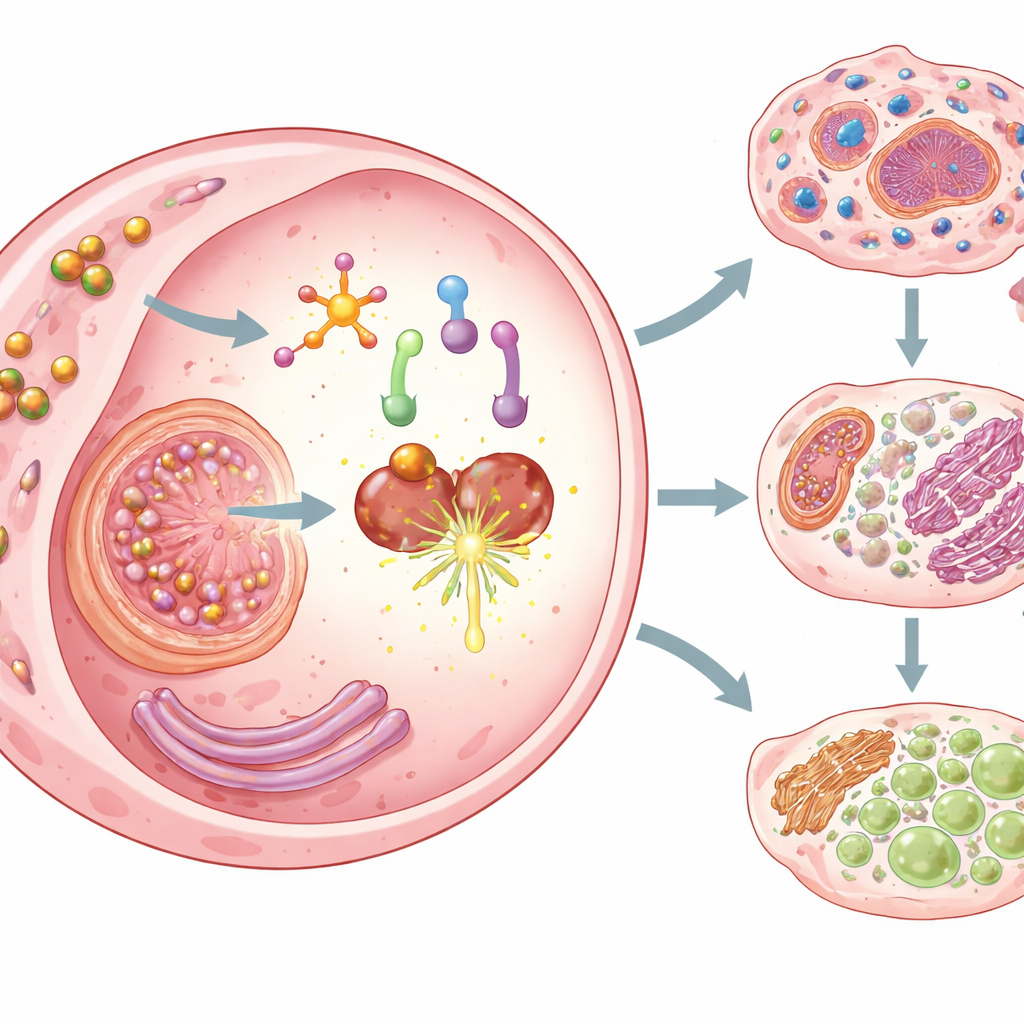
إطلاق ثلاث أشكال من موت خلية السرطان
بمجرد تنشيطه، يفعل Cu–DHN أكثر من مجرد تسميم خلايا السرطان. إنه يطلق ثلاث أشكال منظمة من موت الخلايا تظهر بوضوح أمام الجهاز المناعي. أولًا، يعكس الجوغلون الكبت اللاجيني لبروتين مُنشئ للمسام يُدعى غاسدرمين D وينشط مركب استشعار التهابية، مما يجعل الخلايا تخضع للبيروبتوز — شكل متهور وملتهب من الموت يؤدي إلى انتفاخ الغشاء وتمزقه وانسكاب المحتويات الداخلية. ثانيًا، يدفع النحاس المحمّل داخل الجسيمات، والذي تستوعبه خلايا السرطان بكفاءة، إلى الكوبروبتوز، وهو شكل موت مرتبط بتراكم سام للنحاس في آليات التمثيل الغذائي الرئيسية. ثالثًا، من خلال استنزاف الجلوتاثيون وتعطيل إنزيم واقٍ (GPX4)، يعزز Cu–DHN الفيروبتوز، وهو موت يقوده تأكسد الدهون. معًا، تضمن هذه الآليات أن خلايا السرطان لا تُقتَل بكفاءة فحسب، بل تموت بطريقة شديدة التحفيز للمناعة.
من هجوم محلي إلى دفاع جهازي
يسبب البيروبتوز والأضرار التأكسدية المصاحبة له إطلاق خلايا الورم لطوفان من إشارات الإنذار: مستضدات مرتبطة بالورم، وجزيئات خطر مثل ATP وHMGB1، وعلامات إجهاد على سطحها. في نماذج فأرية لسرطان ثدي عدواني، أدى حقن واحد من Cu–DHN في الأورام الأولية إلى تنشيط قوي للخلايا التغصنية في العقد اللمفاوية القريبة وتزايد خلايا CD8 القاتلة للأورام. سافرت هذه الخلايا المناعية بعد ذلك إلى الأورام غير المعالجة في الجانب المقابل من الجسم وإلى الرئتين، حيث أبطأت أو منعت تقريبًا نمو أورام جديدة وعقد نقيلية. أسفرت حجب خلايا CD8 عن إزالة هذه الحماية إلى حد كبير، مما يؤكد أن Cu–DHN يحول الورم الأولي إلى لقاح في الموقع يعلّم الجهاز المناعي التعرف على السرطان وتدميره في أماكن أخرى.
تأثيرات قوية مع ملف سلامة أفضل
أحد المخاوف المهمة من العلاجات القائمة على البيروبتوز هو مخاطر إيذاء الأنسجة الطبيعية، التي تحمل أيضًا نفس البروتينات المكونة للمسام. عندما يُعطى الجوغلون مباشرة في شكله النشط، تتعرض الفئران لتسمم كبير في الكبد والكلى والدم. بالمقابل، يبقى Cu–DHN خاملًا في الأنسجة السليمة، لأنها تفتقر إلى مزيج المحفزات الكيميائية اللازمة لتنشيط الجسيم. في الفئران، حقق Cu–DHN قوة قتل الورم والوقاية من النقائل مشابهة للجوغلون النشط مع تجنب تلف الأعضاء، والاضطرابات الدموية، وفقدان الوزن. ببساطة، يظهر هذا العمل كيف يمكن لجسيم نانوي موصل كهربائيًا وذكي أن يظل هادئًا في الجسم، ويستيقظ فقط داخل الأورام، ويجبر خلايا السرطان على الموت بطريقة تحفز المناعة، ومن ثم يعمل كمنصة لقاح سرطانية دقيقة ومغلقة ذاتيًا.
الاستشهاد: Wang, Y., Zhao, H., Sun, K. et al. Conductive coordination nanozyme prodrugs precisely trigger pyroptosis, cuproptosis and ferroptosis for in situ cancer vaccination. Sig Transduct Target Ther 11, 96 (2026). https://doi.org/10.1038/s41392-026-02607-6
الكلمات المفتاحية: المناعة ضد السرطان, الطب النانوي, البيروبتوز, لقاحات السرطان, البيئة الميكروية للورم