Clear Sky Science · ar
تثبيت KDM5B بواسطة يوبكويتين يدفع لمقاومة العلاج الكيميائي عبر قمع فوسفاتا إزالة التثبيت ثنائية الخصوصية 4 في سرطان المبيض
لماذا تتوقف بعض حالات سرطان المبيض عن الاستجابة للعلاج الكيميائي
تستجيب العديد من النساء المصابات بسرطان المبيض في البداية جيدًا لعلاجات تعتمد على السلع النبيلة مثل السيسبلاتين، لكنهن يواجهن لاحقًا عودة مدمرة للأورام التي لم تعد تتجاوب مع العلاج. تكشف هذه الدراسة عن دائرة جزيئية خفية داخل الخلايا السرطانية تساعدها على اكتساب المقاومة الدوائية. من خلال كشف كيفية تشغيل وإيقاف «مفتاح فوق جيني» محدد، يشير الباحثون إلى طرق جديدة للتنبؤ بأي الأورام ستقاوم العلاج وكيفية إعادة حساسيتها للأدوية الموجودة.
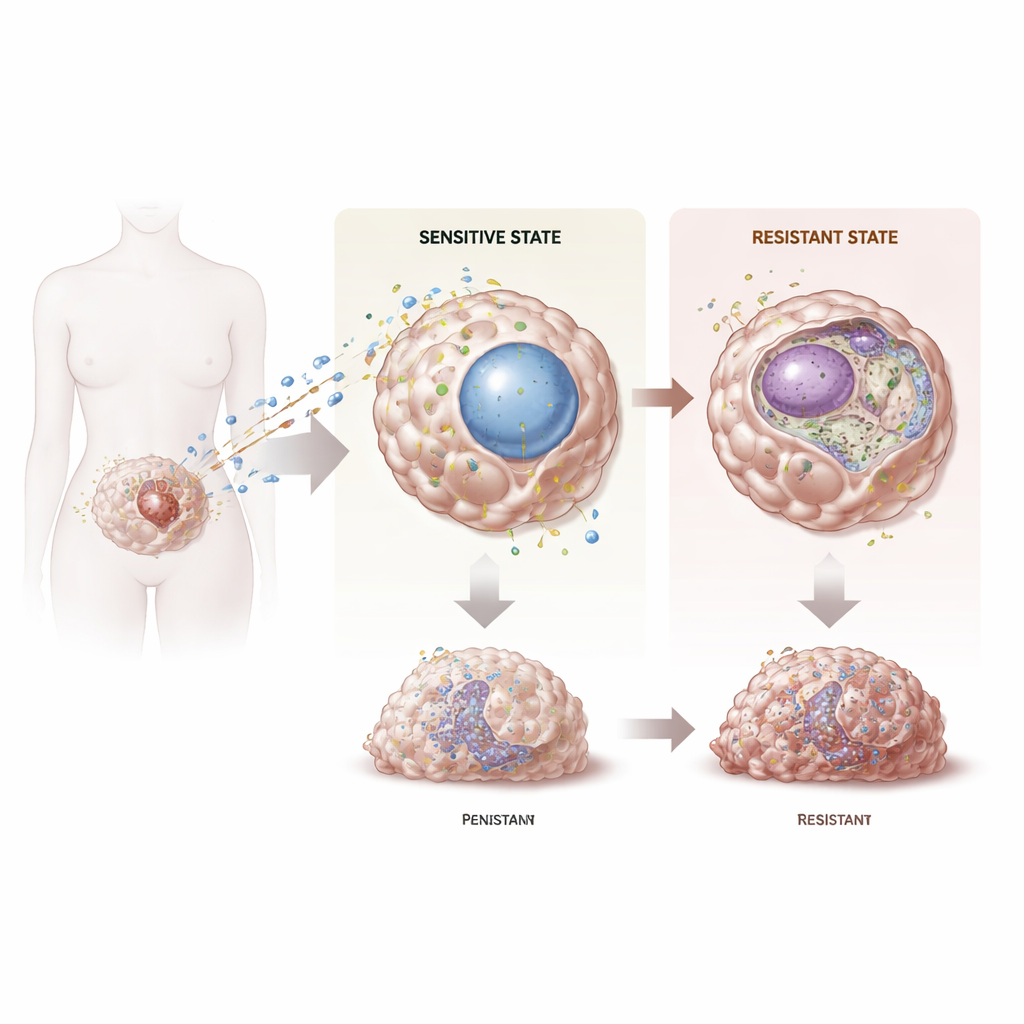
عودة عنيدة لسرطان قاتل
يُعد سرطان المبيض واحدًا من أكثر سرطانات الجهاز التناسلي الأنثوي فتكًا جزئيًا لأنه يُشخَّص عادة متأخرًا ولأن المقاومة للعلاج الكيميائي شائعة. على الرغم من أن ما يصل إلى 80% من المرضى يستفيدون مبدئيًا من العلاج الكيميائي القائم على البلاتين، إلا أن الغالبية تعاودها الطفرة بأورام لم تعد تستجيب، ما يترك خيارات قليلة وبقاءً ضعيفًا. أظهرت أعمال حديثة أن التغيرات في كيفية تنظيم وقراءة الحمض النووي—التغيرات فوق الجينية—يمكن أن تساعد الخلايا السرطانية على التكيف مع العلاج. ركز المؤلفون على عائلة من الإنزيمات تُدعى KDM5، التي تعدل نشاط الجينات عبر إزالة علامات كيميائية من بروتينات الهستون التي تنظم الحمض النووي. تساءلوا عما إذا كانت أعضاء محددة من هذه العائلة قد تكون مفتاحًا لمقاومة البلاتين في سرطان المبيض.
إنزيم واحد يميل الميزان نحو المقاومة
من خلال التنقيب في قواعد بيانات جينومية للسرطان واسعة النطاق ثم اختبار عدة خطوط خلوية لسرطان المبيض، اكتشف الفريق أن أحد أعضاء عائلة KDM5، وهو KDM5B، يبرز في الأورام المقاومة. مستوياته أعلى في سرطانات المبيض المتكررة والآفات النقيليّة والخطوط الخلوية التي لم تعد تستجيب للسيسبلاتين، بينما قرينته القريبة KDM5A لا تُظهر نفس النمط. عندما أزال الباحثون KDM5B انتقائيًا من الخلايا المقاومة، أصبحت تلك الخلايا مرة أخرى عرضة للسيسبلاتين وخضعت لمزيد من موت الخلايا المبرمج. إضافة KDM5B إضافي إلى خلايا كانت حساسة في الأصل أعطت التأثير المعاكس، مما جعلها أصعب في القتل بالعلاج الكيميائي. ثبُتت هذه النتائج عبر عدة نماذج خلوية مستقلة وفي فئران تحمل أورامًا بشرية للمبيض، ما يورط KDM5B بثبات كسائق للمقاومة الدوائية.
فرملة مهمَّلة لإشارات النمو
بتعمق أكبر، سأل المؤلفون أي الجينات يقوم KDM5B بإسكاتها لمساعدة خلايا الورم على النجاة. باستخدام تسلسل RNA ورسم خرائط الكروماتين، وجدوا أن KDM5B يقمع مباشرة جينًا يُدعى DUSP4، الذي يعمل عادة كفرملة على مسار رئيسي للنمو والاستجابة للضغط يُعرف بمسار MAPK. يرتبط KDM5B بمروج DUSP4 ويمحو علامات التشغيل، ما يقلل مستويات DUSP4 ويحرر فعليًا الفرملة على إشارة MAPK. عندما تكون مستويات DUSP4 منخفضة، ترتفع نشاطات MAPK، مما يعزز نمو الخلايا ويساعدها على تحمل تلف الحمض النووي الناتج عن السيسبلاتين. استعادة DUSP4 يعكس هذه المقاومة، بينما حذف DUSP4 يُلغي فوائد إزالة KDM5B، سواء في أطباق الخلايا أو في أورام الفئران. تتردد هذه النتائج في بيانات المرضى: فالأورام ذات المستويات العالية من KDM5B والمنخفضة من DUSP4 ترتبط ببقاء أسوأ.
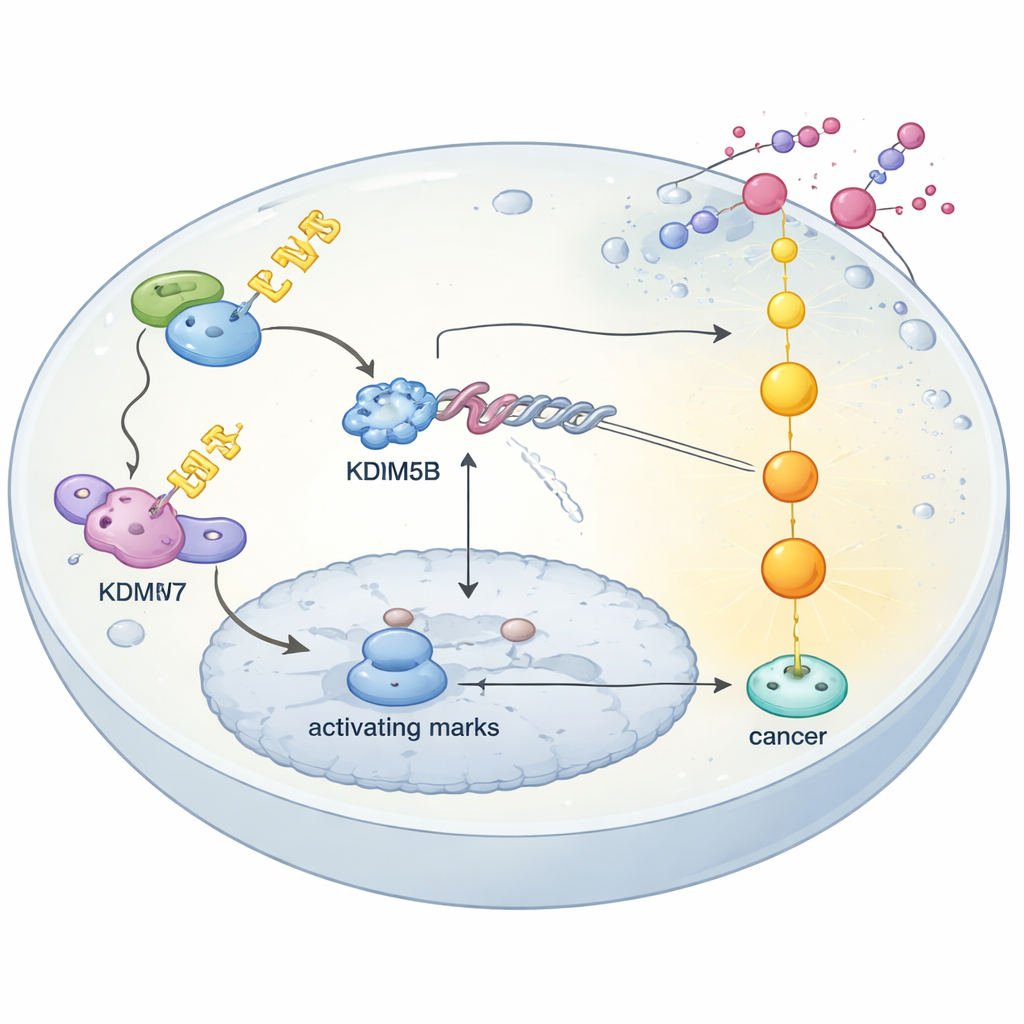
جودة البروتين تشكّل الاستجابة للدواء
تكشف الدراسة أيضًا كيف تُثَبَّت مستويات KDM5B في المقام الأول داخل الخلايا. داخل الخلايا، تُعلَّم العديد من البروتينات باستمرار للتدمير أو تُحفظ بواسطة نظام مراقبة جودة يعتمد على سلاسل اليوبيكويتين. يظهر الباحثون أن إنزيمًا يُدعى USP7 يحمي KDM5B عن طريق إزالة هذه الوسوم، مانعًا تحلله. عندما يُقفل USP7 وراثيًا أو بمثبط جزيئي صغير، تنخفض مستويات KDM5B وتستعيد خلايا سرطان المبيض المقاومة حساسيتها للسيسبلاتين. على النقيض، يتعرف مركب ناقل الببتيد E3 المبني حول بروتين يُسمى FBXW7 على KDM5B فقط بعد أن يضيف إنزيم آخر، HIPK1، فسفرة في موقع محدد، معلمًا إياه للتدمير. تعطيل هذا المسار FBXW7–HIPK1 يجعل KDM5B أكثر استقرارًا. عمومًا، تنشأ المقاومة عندما يفوق دور USP7 الوقائي دور FBXW7 المعالِج، مما يسمح بتراكم KDM5B وإبقاء DUSP4 مطفأ.
طرق جديدة للتحايل على الأورام العنيدة
من خلال رسم محور USP7–KDM5B–DUSP4–MAPK، يقدم المؤلفون تفسيرًا متماسكًا لكيفية تطور خلايا سرطان المبيض إلى مقاومة للسيسبلاتين. للقراء غير المتخصصين، الرسالة الأساسية هي أن المشكلة ليست مجرد وجود طفرات أكثر، بل أيضًا إعادة توصيل تحكم الجينات ودوران البروتينات. تشير الدراسة إلى عدة استراتيجيات قابلة للاختبار: استخدام مستويات KDM5B وUSP7 وDUSP4 كمؤشرات حيوية للتنبؤ بمن سيستجيبون بشكل سيء للعلاج بالبلاتين، ودمج السيسبلاتين مع أدوية تثبط KDM5B أو USP7، أو تعزز تحلل KDM5B، لاستعادة حساسية الدواء. بينما تحتاج هذه المقاربات إلى تحقق سريري، فهي تقدم مخططًا واعدًا لجعل بعض سرطانات المبيض المقاومة قابلة للعلاج مرة أخرى.
الاستشهاد: Yoo, J., Kim, G.W., Jeon, Y.H. et al. Ubiquitin-mediated stabilization of KDM5B drives chemoresistance via repression of dual-specificity phosphatase 4 in ovarian cancer. Sig Transduct Target Ther 11, 89 (2026). https://doi.org/10.1038/s41392-026-02601-y
الكلمات المفتاحية: سرطان المبيض, مقاومة السيسبلاتين, التنظيم فوق الجيني, KDM5B, إشارة MAPK