Clear Sky Science · ar
إزالة DUSP6 تعيد كفاءة خَلايا CAR T المتضررة بفقدان CD58 في الورم عبر تنشيط إشارة AP-1
لماذا يهم تعزيز خلايا مكافحة السرطان
غيّرت الخلايا المناعية المهندَسة المعروفة باسم خَلايا CAR T علاج بعض سرطانات الدم، إلا أن العديد من المرضى يعودون للانتكاس لأن أورامهم تتعلّم كيف تتفادى الهجوم. تكشف هذه الدراسة عن نقطة ضعف مخفية في بعض الأورام تعطل خَلايا CAR T من الداخل — وتبيّن كيف أن تعديلًا جينيًا دقيقًا يمكن أن يستعيد قدرة هذه الخلايا على الصمود، وتوفير الطاقة، وقوة القتل. للقراء، إنها لمحة عن الكيفية التي قد تجعل بها علاجات الخلايا من الجيل القادم أكثر دوامًا وفاعلية لشريحة أوسع من المرضى.
مقبض مفقود على خلايا الورم
تحتاج خَلايا CAR T إلى «مصافحة» قوية مع الهدف لتعمل جيدًا. تعرض العديد من خلايا الورم جزيئًا سطحيًا يسمى CD58 يعمل كمِقبَض للخلايا المناعية، يساعدها على الالتصاق وتكوين منطقة اتصال محكمة. أظهرت أعمال سابقة أنه عندما تفقد السرطانات CD58، يصعب على خَلايا CAR T تشكيل هذا الاتصال وتضعف فعاليتها. في هذه الدراسة، طرح الباحثون سؤالًا أعمق: إلى جانب مشكلة المصافحة الميكانيكية، كيف يعيد فقدان CD58 برمجة البيولوجيا الداخلية لخَلايا CAR T ليقلل من أدائها مع مرور الوقت؟
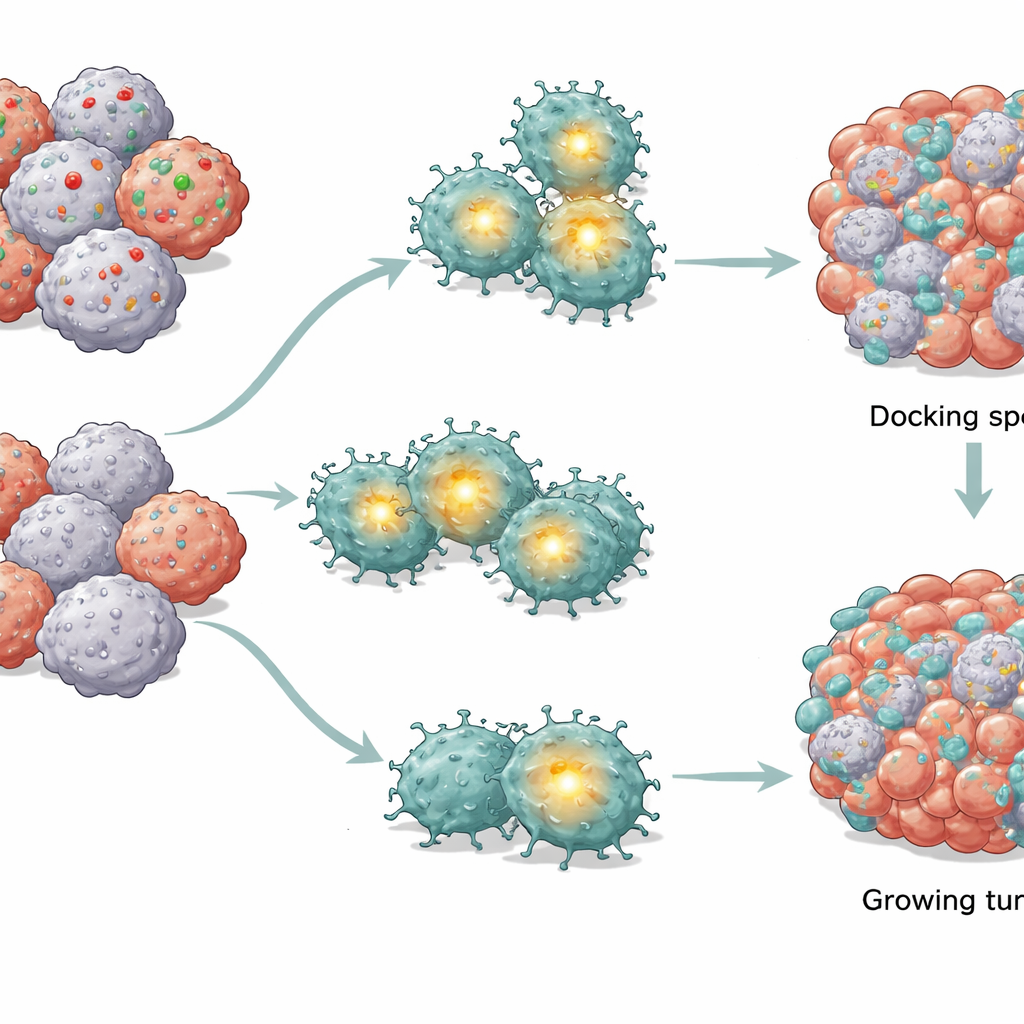
أسلاك قصيرة داخل خَلايا CAR T
بمقارنة خَلايا CAR T المعرضة لأورام طبيعية بتلك المواجهة لأورام ناقصة CD58، وجد الفريق أن محور تحكّم رئيسي داخل الخلايا التائية — يسمى AP-1 — أصبح أضعف انتقائيًا، بينما ظلت مسارات إشارات رئيسية أخرى إلى حد كبير سليمة. AP-1 مجموعة بروتينات تُشغّل جينات مرتبطة بالتنشيط والبقاء. عندما انخفض نشاط AP-1، أظهرت خَلايا CAR T علامات أزمة طاقة داخلية واضحة: عدد ومحجم أقل للميتوكندريا (محطات الطاقة)، قدرة أقل على استهلاك الأكسجين واستخدام السكر، وفقدان الشحنة الكهربائية عبر أغشية الميتوكندريا. في الوقت نفسه، تراكمت جزيئات أكسجينية ضارة. مجتمعة، دفعت هذه التغيرات خَلايا CAR T نحو برنامج انتحاري ذاتي قائم على تلف الميتوكندريا الداخلية، حتى دون إشارات موت خارجية.
إيقاف مكبح داخلي
لفهم سبب خمود AP-1، بحث الباحثون صعودًا عن «مكابح» جزيئية قد تكون مفرطة النشاط. وجدوا أن خَلايا CAR T المواجهة لأورام ناقصة CD58 رفعت من مستوى عدة فسفاتازات — إنزيمات تُطفئ مسارات الإشارة — وخصوصًا إنزيمًا يسمى DUSP6. باستخدام أدوية ثم تعديل جيني دقيق لحجب هذه الإنزيمات، اكتشفوا أن إزالة DUSP6 أعادت نشاط AP-1 بشكل أقوى من غيرها. خَلايا CAR T المحرّرة من DUSP6 توسعت بشكل أفضل، كوّنت ميتوكندريا أكثر، أحرقت الوقود بكفاءة أعلى، أنتجت المزيد من الجزيئات القاتلة للسرطان، وكانت أقل عرضة للموت المبرمج، لا سيما عند تحديها مرارًا بواسطة خلايا ورمية ناقصة CD58.
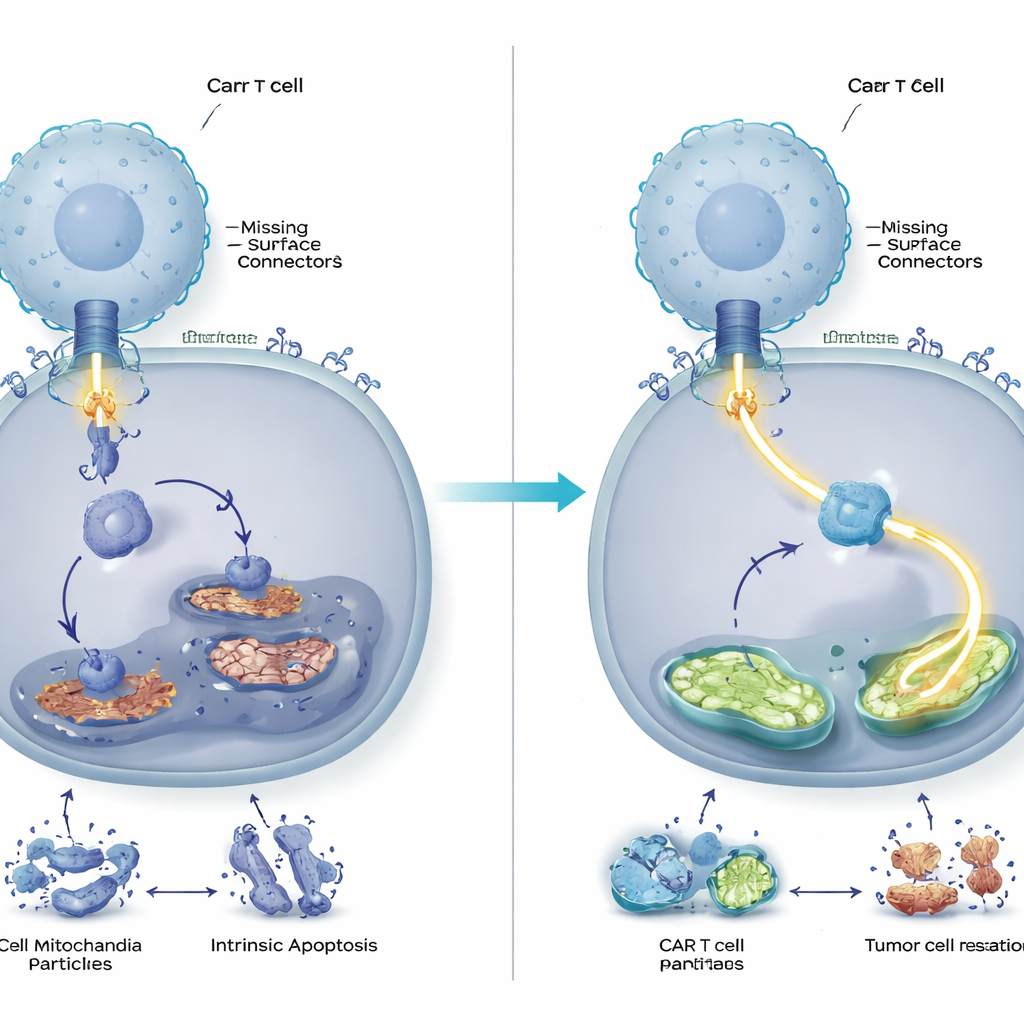
تحكم أقوى وأطول بالورم في الحيوانات
اختبر الفريق بعد ذلك ما إذا كان هذا الضبط الجزيئي مهمًا في أنظمة حية. في فئران تحمل خلايا سرطان دم بشرية ذات CD58 أو ناقصة له، قضت خَلايا CAR T الخالية من DUSP6 على الأورام بفاعلية أكبر وأبقت عليها لفترة أطول مقارنة بخَلايا CAR T التقليدية. تكاثرت الخلايا المهندَسة بقوة أكبر، أظهرت علامات تعب أقل، وأفرازت مستويات أعلى من الرسل المناعيين الرئيسيين. والأهم أن فوائد إزالة DUSP6 لم تُرَ فقط عند الأورام الناقصة CD58 بل أيضًا عند تلك التي احتفظت به، مما يوحي بأن هذا التعديل قد يعزز علاجات خَلايا CAR T بشكل عام بدلاً من كونه تصحيحًا ضيقًا لنوع نادر من الأورام.
دلائل من بيانات المرضى
لفحص الصلة في البشر، درس الباحثون بيانات التعبير الجيني من أشخاص عولجوا بخَلايا CAR T أو بأدوية تثبيط نقاط التفتيش المناعية. في مرضى مصابين بورم ليمفاوي خلايا ب كبيرة منتشر يتلقون علاج CAR T ثنائي الهدف، ارتبطت مستويات أقل من DUSP6 في الخلايا التائية CD8 قبل أو بعد الحقن مباشرة بمعدلات استجابة كاملة أعلى. في مجموعة منفصلة من سرطانات الجلد المعالجة بمضادات PD-1، كانت الخلايا التائية CD8 المستنفدة من غير المستجيبين تميل إلى التعبير عن DUSP6 أكثر من تلك لدى المستجيبين. تقترح هذه الملاحظات معًا أن DUSP6 يعمل كعلامة سلبية للياقة الخلوية عبر علاجات مناعية مختلفة وأن خفضه قد يحسّن النتائج.
ماذا يعني هذا لعلاجات السرطان المستقبلية
للقارئ العام، الرسالة أن بعض الأورام تهرب من هجوم خَلايا CAR T ليس فقط عبر الاختباء عن التعرف بل عبر تخريب محركات الخلايا الداخلية. فقدان «مقبض» CD58 على خلايا الورم يخفض بهدوء إشارة AP-1 في خَلايا CAR T، يستنزف ميتوكندرياها، يزيد النواتج السامة، ويدفعها نحو موت مبكر. بإزالة مكبح DUSP6، يمكن للعلماء استعادة هذه الإشارات المفقودة، إصلاح صحة الميتوكندريا، ومنح خَلايا CAR T قدرة تحمل وقوة قتل أكبر، حتى ضد الأورام المقاومة. ومع أن هناك حاجة لمزيد من اختبارات السلامة والسريرية، تبرز إزالة DUSP6 كاستراتيجية هندسية واعدة لجعل عقاقير السرطان الحية أكثر قوة وطولًا وربما فعالية لشريحة أوسع من المرضى.
الاستشهاد: Ma, X., Zhang, Y., Wang, Y. et al. DUSP6 ablation restores CAR T-cell fitness impaired by tumor CD58 loss through invigoration of AP-1 signaling. Sig Transduct Target Ther 11, 100 (2026). https://doi.org/10.1038/s41392-026-02597-5
الكلمات المفتاحية: خَلايا CAR T, CD58, DUSP6, المناعة المناعية ضد السرطان, استقلاب الخلايا التائية