Clear Sky Science · ar
إطلاق العنان لإمكانات قنبلة نانومترية ثنائية المعدن لتنشيط مسار STING لتعزيز معالج التيل الخلوي ثنائي الخصوصية ضد العلاج الضوئي-المناعي لسرطان القولون والمستقيم
إعادة الجهاز المناعي لمحاربة سرطان القولون
سرطانات القولون والمستقيم شائعة وغالبًا ما تكون مميتة، ويرجع ذلك جزئياً إلى قدرة الأورام على التخفّي من جهاز المناعة. تستكشف هذه الدراسة استراتيجية جديدة تَجمَع عدة آليات مضادة للسرطان في «قنبلة نانوية» صغيرة لإيقاظ دفاعات الجسم، ومساعدة خلايا المناعة على العثور على الورم، ومنع عودة السرطان أو انتشاره.
لماذا تحتاج أدوية المناعة الحالية إلى ترقية
فئة واعدة من أدوية السرطان، تُسمى معالجات التيل الخلوي ثنائية الخصوصية، تعمل كوسطاء حيويون: طرف يلتقط خلية تيل (مقاتل مناعي رئيسي) والطرف الآخر يتصل بعلامة على خلية الورم، مما يجبرهما على الاتحاد حتى تقتل خلية التيل الورم. وعلى الرغم من فعاليتها في سرطانات الدم، إلا أن هذه الأدوية تكافح في الأورام الصلبة مثل سرطان القولون والمستقيم. تُزال بسرعة من الجسم، وقد تهاجم أنسجة سليمة تشترك في نفس العلامة، وغالبًا ما تواجه أورامًا «باردة» تفتقر إلى ما يكفي من الخلايا المناعية لجعل العلاج فعالًا. لذلك يبحث الأطباء والعلماء عن طرق لتوصيل هذه الأدوية بأمان أكبر ولتحويل الأورام الباردة إلى أورام «ساخنة» غنية بالخلايا المناعية المفعّلة.
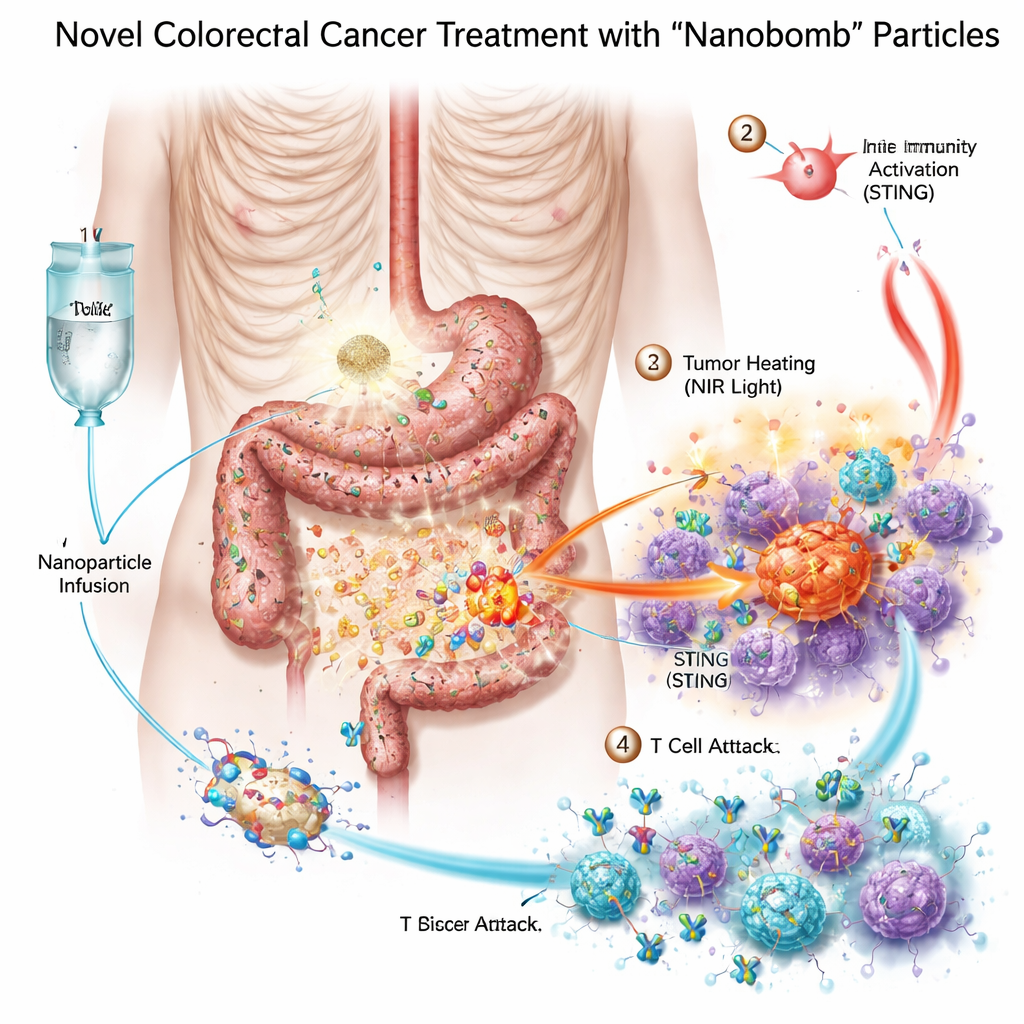
حزم ثلاث أسلحة داخل «قنبلة نانوية» واحدة
صمّم الباحثون قنبلة نانوية ثنائية المعدن — مسماة علميًا MnO2/Co‑DA@BiTE/HPT — تدمج ثلاث طرق علاجية في جسيم واحد. أولاً، يحتوي النواة على المنغنيز والكوبالت، وهما معادن يمكنها تنشيط نظام إنذار خلوي يُسمى مسار STING، الذي يساعد الجسم على استشعار الخطر واستدعاء خلايا المناعة. ثانيًا، طُليت سطحية الجسيم بمعالج التيل الخلوي ثنائي الخصوصية الذي يربط خلايا التيل بخلايا السرطان. ثالثًا، يمتص المادّة الضوء القريب من الأشعة تحت الحمراء، مما يمكَّن الأطباء من تسخين الورم من الخارج كنوع من العلاج بالحرارة الضوئية. ولضمان استهداف القنابل النانوية لخلايا سرطان القولون والمستقيم، أضاف الفريق قطعة قصيرة من الحمض النووي، أبتيامر، تتعرف على PD‑L1، وهو جزيء غالبًا ما يتواجد كثيرًا على هذه الأورام. بمجرد وصول هذه الجسيمات إلى الورم، تساعد الإنزيمات الطبيعية في نسيج الورم على تفكيكها وإطلاق حمولتها في المكان الذي تُحتاج إليه بالضبط.
التسخين، الإنذار، وتجنيد جيش المناعة
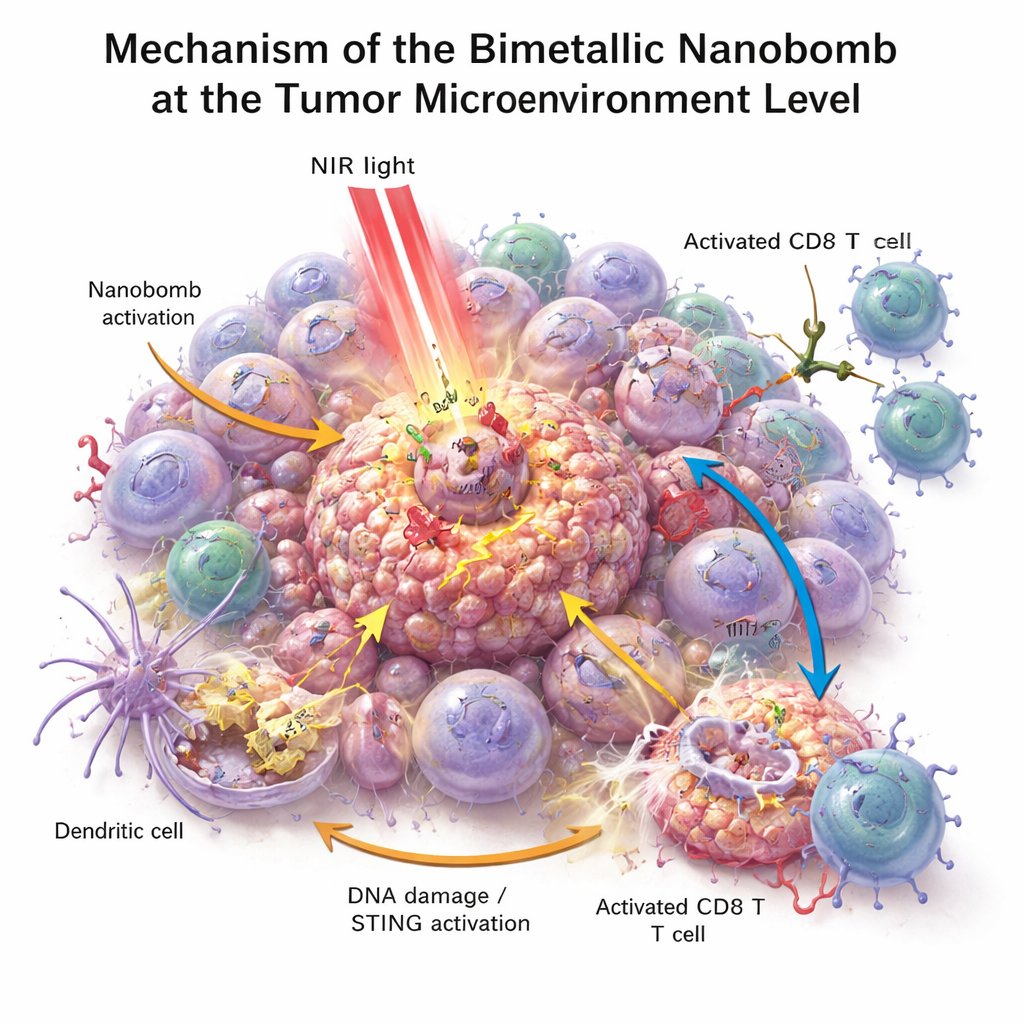
في الأطباق المخبرية، قتلت القنابل النانوية خلايا سرطان القولون والمستقيم بفعالية أكبر من أي مكوّن منفرد. عند تسليط الضوء القريب من الأشعة تحت الحمراء، احتُمرت الجسيمات، وأحدثت ضغطًا وأضرارًا في خلايا السرطان، وساهمت في توليد أنواع أكسجين تفاعلية — جزيئات عالية التفاعل تُلحق مزيدًا من الضرر بخلايا الورم. سبّب هذا الإجهاد تلفًا في حمض نووي الخلايا ودفعها نحو شكل وفاة ظاهر يطلق إشارات «خطر». التهمت خلايا المناعة القريبة، وخصوصًا الخلايا التغصنية، المواد الورمية المحتضرة وفعلت مسار STING بمساعدة المنغنيز والكوبالت المُطلقَين. ثم أنتجت الإنترفيرونات وغيرها من الرسل الالتهابية التي تنضج وتستقطب خلايا التيل. في الوقت نفسه، ربط المعالج ثنائي الخصوصية الموجود على القنبلة النانوية خلايا التيل فعليًا بخلايا الورم الإيجابية لـ PD‑L1، مما حسّن تنشيط خلايا التيل وقتل الورم حتى في الأورام الباردة سابقًا.
من تقلص الورم إلى ذاكرة مناعية دائمة
في عدة نماذج فأرية — بما في ذلك أورام قولون تحت الجلد، وأورام على جانبي الجسم، ونقائل رئوية، ونموذج عودة بعد الجراحة — أبطأت القنابل النانوية مع الضوء نمو الورم بشدة أو أوقفته تقريبًا. احتوت الأورام المعالجة على عدد أكبر بكثير من خلايا التيل CD8 القاتلة للسرطان وأقل من الخلايا التائية المنظمة التي تكبح الاستجابات المناعية عادة. أظهرت الخلايا التغصنية داخل الأورام وفي العقد الليمفاوية علامات النضج، وكشفت فحوصات الدم عن مستويات مرتفعة من السيتوكينات المحفّزة للمناعة. والأهم أن الفئران التي تخلصت من أورامها بعد علاج القنبلة النانوية كانت محمية بشكل أفضل عند إعادة إدخال السرطان، وظهرت عليها نقائل رئوية أقل، مما يدل على أن العلاج ساعد في بناء ذاكرة مناعية طويلة الأمد بدلًا من مجرد تقلص مؤقت للورم.
ماذا قد يعني هذا لرعاية السرطان المستقبلية
تقدم هذه الدراسة دواءً نانويًا «ثلاثي الضربات» يسخّن الأورام، ويشغّل إنذار الخطر الداخلي، ويرشد خلايا التيل مباشرة إلى الخلايا السرطانية، كل ذلك داخل جسيم مستهدف واحد. في الفئران، لم يقتصر دور هذا النهج على تحويل أورام القولون والمستقيم الباردة إلى أورام ساخنة ومُلتهبة فحسب، بل ساعد أيضًا في منع التكرار والانتشار. وبينما لا تزال التقنية بعيدة عن الاستخدام السريري — فالتوسيع الصناعي، والسلامة على المدى الطويل، والاختبارات البشرية تبقى تحديات كبيرة — فإنها تقدم نموذجًا للعلاجات المستقبلية التي تمزج مواد ذكية مع أدوية مناعية لمنح المرضى استجابة مضادة للسرطان أقوى وأكثر ديمومة.
الاستشهاد: Mu, M., Li, H., Chen, B. et al. Unleashing the potential of bimetallic nanobomb-mediated STING pathway to enhance bispecific T-cell engager against colorectal cancer photo-immunotherapy. Sig Transduct Target Ther 11, 80 (2026). https://doi.org/10.1038/s41392-026-02596-6
الكلمات المفتاحية: سرطان القولون والمستقيم, العلاج المناعي, الجسيمات النانوية, مسار STING, معالج التيل الخلوي ثنائي الخصوصية