Clear Sky Science · ar
علاج موجه مخصّص موجه بالفارماكوكيتيك والفارماكودينامي عبر منصة متعددة العضويات مشتقة من الخلايا الجذعية المحفَّزة في سرطان الثدي الطافح لطافح NF1
لماذا يهم هذا البحث للمرضى
يتلقى العديد من مرضى السرطان أدوية تعمل بشكل جيد لدى بعض المرضى ولا تؤتي ثمارها لدى آخرين، وغالبًا ما تسبب آثارًا جانبية شديدة. تصف هذه الدراسة طريقة جديدة لاختبار علاجات السرطان خارج الجسم باستخدام أعضاء مصغرة مزروعة مخبريًا مُصنَّعة من خلايا المريض نفسه. يركز العمل على شكل صعب العلاج من سرطان الثدي يقوده تغير في جين يُدعى NF1، ويُظهر كيف أن الجمع بين استراتيجية تصحيح جيني ودواء موجه قد يؤدي إلى علاج أكثر أمانًا وفعالية وشخصنة حقيقية.
بناء نسخة مصغرة من جسد المريض
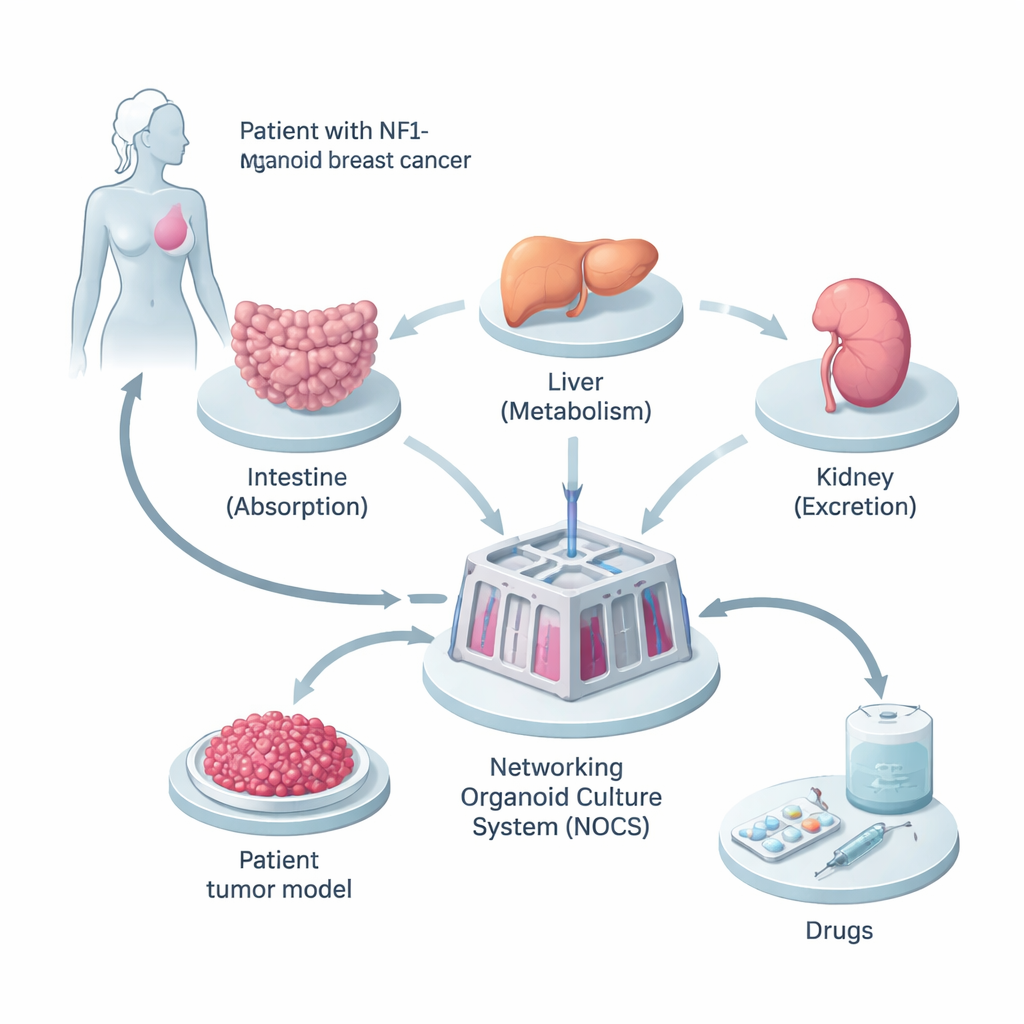
بدأ الباحثون بنسيج من امرأة كان سرطان ثديها يحمل طفرة موروثة في جين NF1. أعادوا برمجة خلايا تشبه الجلد السليمة لديها إلى خلايا جذعية محرضة متعددة القدرات، قادرة على التحوّل إلى أي نوع تقريبًا من خلايا الجسم. ومن هذه الخلايا نَمَوْا ثلاثة أنواع من الأعضاء المصغرة—الأمعاء الدقيقة والكبد والكلى—لأن هذه المواقع هي المحاور الأساسية التي يُمتَص عبرها الدواء ويُعالج ويُطرد. وبالتوازي، أنشأوا كرة ثلاثية الأبعاد منورّاة للورم من خلايا سرطانها، محافظةً على مزيج أنواع الخلايا والتغيرات الجينية الموجودة في الورم الأصلي.
دائرة حيّة لاختبار الأدوية
لجعل هذه الأعضاء المصغرة تتصرف أكثر مثل الجسم الحقيقي، ربط الفريق بينها في جهاز مملوء بالسائل يُسمى نظام زراعة الأورغانويدات المترابطة، أو NOCS. في هذا الإعداد يتدفق الوسط السائل بين حجرات الأمعاء والكبد والكلى والورم، مقلدًا دوران الدم. يمكن إضافة الأدوية بطريقة تشبه ابتلاع قرص أو تلقي حقنة، وتتحكم حساسات ومضخات في سرعة تحرك «الدم» وتواتر تجديده. سمح هذا للعلماء بتتبع مقدار الدواء الممتص، وسرعة تفككه، وقوة فعاليته على الورم—كل ذلك في نموذج بشري مخصص للمريض.
تصحيح جين معطّل عبر تخطي الإكسون
كان ورم المريضة يحمل طفرة ضارة في NF1 تبقي مسارات النمو مفعَّلة وتُفشل العديد من الأدوية القياسية. صمّم الفريق قطعًا قصيرة من المادة الوراثية تُعرف بالأوليغونوكليوتيدات المضادة للاستطالة (antisense oligonucleotides) لتدفع آلية معالجة الرنا داخل الخلايا إلى تخطي الجزء المعطوب (الإكسون 2) من جين NF1. باستخدام نظام توصيل فيروسي يحافظ على الفعالية لأيام، أحدثوا «تخطيًا» مستقراً للإكسون في خلايا سرطان المريضة. نتج عن ذلك بروتين NF1 أقصر لكنه وظيفي، حدَّ من إشارات النمو المفرطة، وجعل خلايا الورم أكثر حساسية للعلاج.
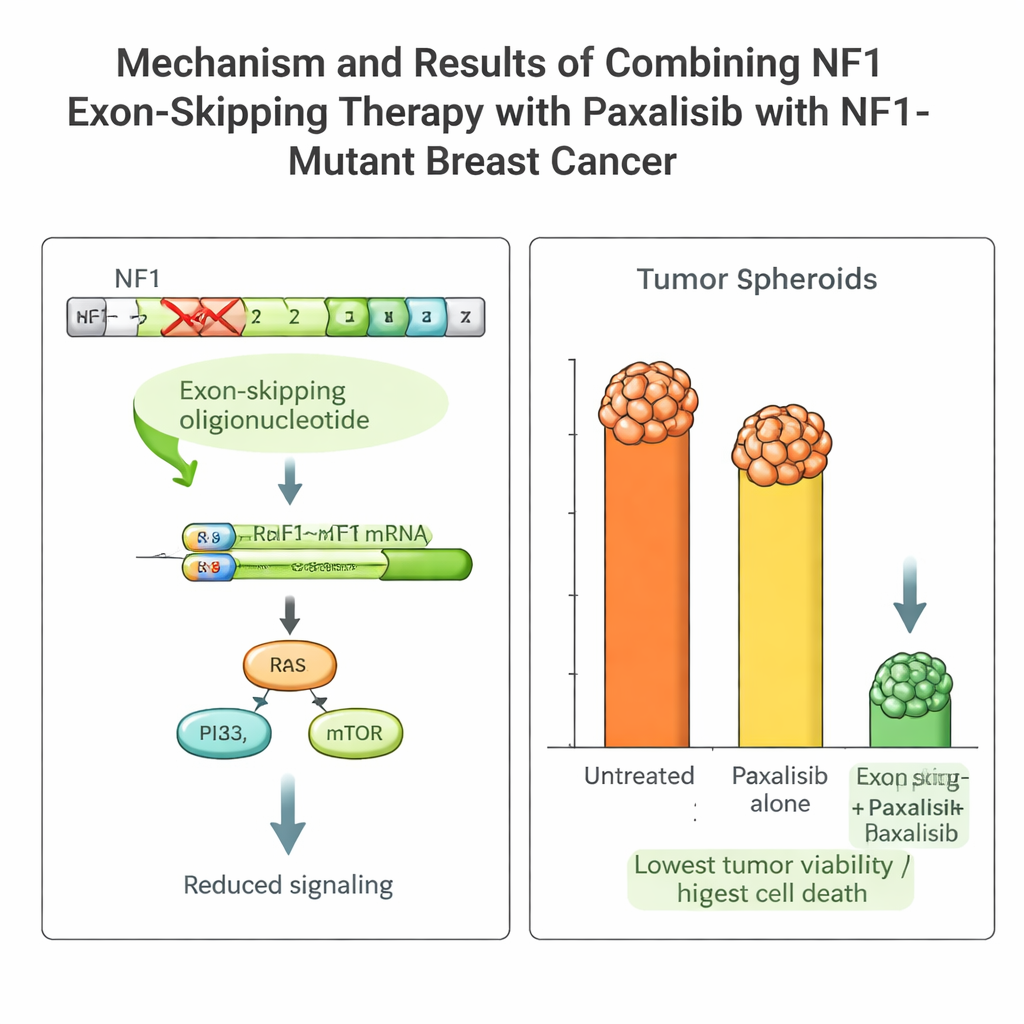
اختيار الدواء الموجه المناسب بتوجيهات PK/PD
مزوّدين بهذه المنصة، قارن الفريق عدة أدوية متقدمة تمنع مسار PI3K–mTOR، الذي يقع أسفل NF1. قاسوا الفارماكوكيتيك (كيف يتعامل الجسم مع الدواء) والفارماكوديناميكا (كيف يؤثر الدواء على الورم) في كل من الفئران ونظام NOCS. برز دواء واحد، باكساليسيب (Paxalisib): إذ اُمتص جيدًا في الأمعاء، وبقي في النظام بمستويات مفيدة، وأظهر سلوكًا مماثلًا في الحيوانات وفي جهاز الأورغانويدات. عند الجمع بين تخطي إكسون NF1 وباكساليسيب، ازدادت قدرة الدواء على قتل خلايا ورم المريضة بشكل كبير، مع تراجعات قوية في النمو وعلامات واضحة للموت المبرمج للخلايا، سواء في NOCS أو في الفئران الحاملة لورم المريضة.
موازنة الفائدة والمخاطر عبر الأعضاء
لأن نماذج الأمعاء والكبد والكلى كانت جزءًا من الدائرة نفسها، تمكن الباحثون أيضًا من مراقبة علامات مبكرة لضرر أعضاء. تسبب باكساليسيب في استجابات إجهاد وإضعاف طفيف للحاجز في نماذج الأمعاء والكلى وعلامات إجهاد في الكبد، لكن من دون فقدان كبير في حيوية الخلايا عند الجرعة المختبرة. هذا النوع من النظرة الشاملة للجسم، باستخدام نسيج بشري، يوفر وسيلة لمقارنة خيارات العلاج ليس فقط على أساس مدى تقلّص الأورام، بل أيضًا على كيفية تأثيرها المحتمل على الأعضاء السليمة قبل أن يصل الدواء إلى المريض.
ما الذي قد يعنيه هذا لرعاية السرطان في المستقبل
بكل وضوح، تُظهر هذه الدراسة أنه أصبح بالإمكان الآن زراعة «جسد مصغّر على رقاقة» مبسَّط ومخصص للمريض يمكنه اختبار كيف سيتصرف ويتفاعل كل من الأدوية—وحتى طرق تصحيح الجينات—. بالنسبة لمريضة سرطان الثدي الحاملة لطفرة NF1، كانت الاستراتيجية المثلى مزيجًا من علاج تخطي إكسون NF1 والدواء الفموي باكساليسيب، حيث أبطأ الاثنان نمو الورم أكثر بكثير مما حققه أي منهما وحده. إذا طُوِّرت هذه المنصات أكثر واختُبرت في مرضى إضافيين، فقد ترشد الأطباء نحو خطط علاجية مخصّصة لجينات وبيولوجيا كل شخص، مما يزيد فرص النجاح ويقلل السمية غير الضرورية.
الاستشهاد: Lim, J.H., Mun, S.J., Kang, H.M. et al. Personalized pharmacokinetic–pharmacodynamic guided therapy via an induced pluripotent stem cell–derived multi-organoid platform in NF1-mutant breast cancer. Sig Transduct Target Ther 11, 79 (2026). https://doi.org/10.1038/s41392-026-02595-7
الكلمات المفتاحية: طب الأورام المخصص, سرطان الثدي, الأورغانويدات, طفرة NF1, العلاج الموجَّه