Clear Sky Science · ar
الجذور الحرة للأكسجين (ROS) في السرطان: من الآلية إلى الدلالات العلاجية
عندما تتحول جزيئات مفيدة إلى خطرة
داخل كل خلية، تتولد شرارات كيميائية دقيقة تُسمى الجذور الحرة للأكسجين، أو ROS، باستمرار كجزء من الحياة الطبيعية. عند مستويات مناسبة تساعد هذه الجزيئات الخلايا على النمو والتواصل والدفاع عن نفسها ضد الجراثيم. لكن هذه المراجعة تشرح كيف يمكن لنفس الجزيئات أن تضر الحمض النووي، وتعرّض شبكات الخلايا للخلل، وتدفع السرطان إلى النمو والانتشار والمقاومة للعلاج. فهم هذه «الحياة المزدوجة» للجذور الحرة يساعد العلماء على تصميم علاجات سرطانية جديدة إما لتهدئة الإجهاد التأكسدي الضار أو لدفعه عمدًا إلى حد قاتل لقتل الخلايا الورمية.
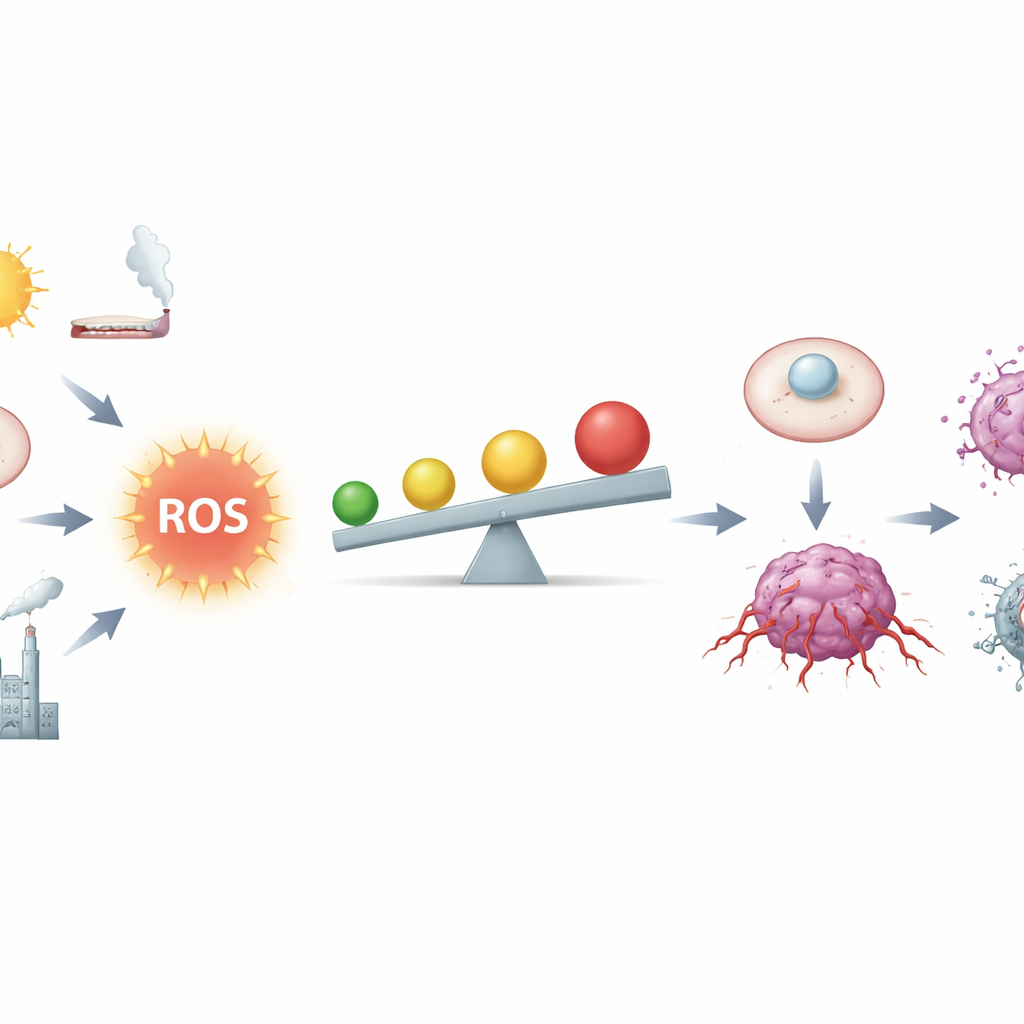
الحد الفاصل بين الوقود والنار
يصف المؤلفون ROS كنواتج كيميائية للتنفس والتمثيل الغذائي، لكنها أيضاً رسول قوي. في الأنسجة السليمة، تساعد كميات منخفضة من ROS على ضبط دورة الخلية، وإصلاح الأضرار، وضبط الاستجابة المناعية. تحافظ الخلايا على هذه الإشارات تحت السيطرة باستخدام شبكة مضادات أكسدة معقدة، تشمل جزيئات مثل الجلوتاثيون وإنزيمات يخضع نشاطها لمفتاح رئيسي يسمى Nrf2. أما خلايا السرطان فتعيش أقرب إلى منطقة الخطر: الجينات المعطوبة، الميتوكوندريا المرهقة، الالتهاب المزمن، دخان التبغ، الإشعاع، وبعض المعادن ترفع مستويات ROS. عند مستويات مرتفعة متوسطة، يمكن لـROS أن تُحدث شقوقًا في الحمض النووي، وتزعزع استقرار الكروموسومات، وتفعّل باستمرار دوائر النمو والبقاء، مما يجعل تحول الخلية الطبيعية إلى خلية سرطانية أسهل.
كيف يشكل الإجهاد التأكسدي سلوك الورم
بمجرد أن يتأسس الورم، تواصل ROS تشكيل بيولوجيته. الإجهاد التأكسدي المتوسط ينشط العديد من مسارات النمو التي تشجع الخلايا على الانقسام، وتكوين أوعية دموية، وغزو الأنسجة المجاورة، ومقاومة العلاج الكيميائي. يمكن لـROS إعادة برمجة كيفية استخدام خلايا السرطان للسكريات والدهون والأحماض الأمينية، موجهة الوقود إلى مسارات تصنع طاقة مضادة للأكسدة ومكونات بناء إضافية للخلايا الجديدة. كما تؤثر على قرارات مصير الخلية: بحسب الشدة والسياق، قد تميل ROS إلى تعزيز إشارات البقاء أو إلى دفع الخلية نحو أشكال متعددة من الموت المبرمج، بما في ذلك الاستماتة التقليدية (apoptosis) وأشكال أحدث مثل الفيروبتوزيس، النخر المبرمج (necroptosis) والكوبروبتوزيس. هذا يجعل ROS رفقاء في تقدم الورم ومثيرين محتملين لتدميره الذاتي.
إعادة برمجة المناعة واستجابة الأدوية
تُبرز المراجعة أن تأثيرات ROS لا تقتصر على خلايا السرطان نفسها — بل تعيد تشكيل حيّز الورم. يمكن للإجهاد التأكسدي العالي أن يُجهد أو يقتل خلايا T القاتلة والخلايا القاتلة الطبيعية، بينما يفضّل الخلايا القمعية التي تحمي الورم من الهجوم. كما تساعد ROS الأورام على زيادة إشارات «لا تقتلني» مثل بروتينات نقاط التفتيش، مما يضعف تأثيرات العلاج المناعي. وفي الوقت نفسه، يمكن لـROS المتوسطة أن تدفع مقاومة الدواء عبر تعزيز مضخات طرد الدواء واستجابات الإجهاد، ما يسمح لخلايا السرطان بطرد العلاج الكيميائي أو إصلاح الأضرار التي يسببها. ومع ذلك، في ظروف أخرى، فإن دفع ROS فوق عتبة حاسمة يمكن أن يفكك هذه الدفاعات ويعيد حساسية الأورام للعلاج.
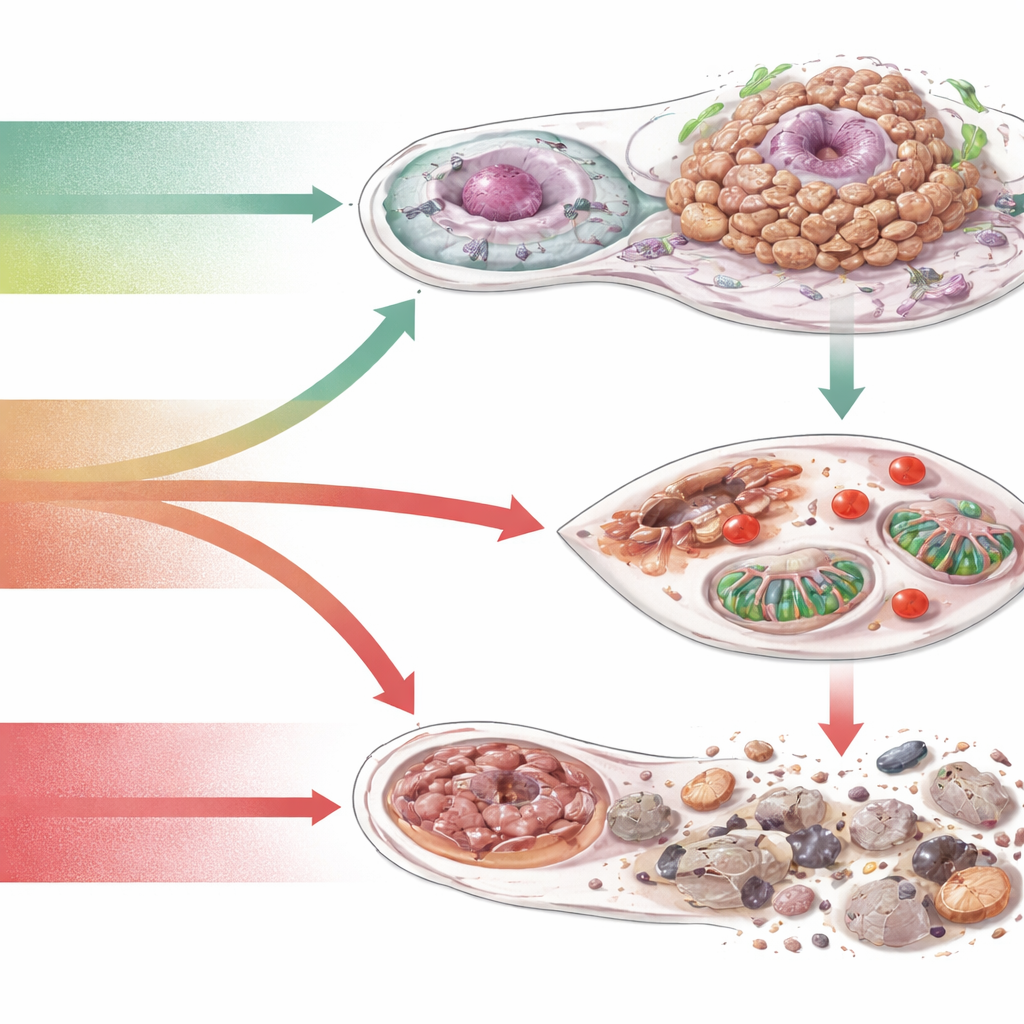
تحويل هشاشة التوازن الأحمر إلى استراتيجية علاجية
لأن خلايا السرطان تمشي على حبل مشدود بين استخدام ROS والتسمم بها، يرى المؤلفون أن توازن ROS يشكل رافعة علاجية. إحدى الاستراتيجيات العامة هي خفض ROS الضار أو تقوية أنظمة مضادات الأكسدة، وذلك أساسًا للوقاية أو لحماية الأنسجة السليمة أثناء العلاج. أما الأخرى فهي العكس داخل الأورام: تعطيل أنظمة مضادات الأكسدة أو زيادة إنتاج ROS حتى تتجاوز خلايا السرطان عتبة قاتلة، خصوصًا عند الجمع مع الإشعاع أو الأدوية المستهدفة أو العلاج المناعي. نهج ثالث هو ترك مستويات ROS كما هي لكن حجب المفاتيح الحساسة للـROS — بروتينات الإشارة، الإنزيمات الأيضية، أو مسارات الموت — التي يعتمد عليها الورم. ويخيط هذه الأفكار موضوع التخصيص: كل سرطانات تحمل «بصمات حمرية» مختلفة، لذا قد تحتاج العلاجات المستقبلية إلى اختبارات دم أو نسيج لقياس الضرر التأكسدي، قدرة مضادات الأكسدة، والجينات المرتبطة بـROS لاختيار العلاج المستهدف المناسب لكل مريض.
ماذا يعني هذا للمرضى
بعبارات بسيطة، يجادل هذا المقال بأن ROS ليست سيئة تمامًا ولا جيدة تمامًا؛ إنها أدوات قوية تستخدمها الخلايا والسرطانات. تميل خلايا السرطان إلى العمل أقرب إلى نقطة الانقلاب في الإجهاد التأكسدي مقارنة بالخلايا السليمة، ما قد يخلق نافذة علاجية. ومع ذلك، ولأن مضادات الأكسدة والمحفزات التأكسدية يمكن أن تفيد أو تضر اعتمادًا على الجرعة والتوقيت ونوع الورم، فإن الاستخدام الواسع للمكملات أو الأدوية المعززة للـROS يحمل مخاطر. ويخلص المؤلفون إلى أن المستقبل يكمن في علاجات وتشخيصات مصممة بعناية تقرأ حالة التوازن الأحمر لكل ورم ثم تحفز ROS وأنظمة مضادات الأكسدة بما يكفي — إما خفضها لحماية الأنسجة الطبيعية، أو رفعها لدفع خلايا السرطان إلى ما بعد نقطة الانهيار.
الاستشهاد: Akter, S., Madhuvilakku, R., Kar, A.K. et al. Reactive oxygen species (ROS) in cancer: from mechanism to therapeutic implications. Sig Transduct Target Ther 11, 111 (2026). https://doi.org/10.1038/s41392-026-02583-x
الكلمات المفتاحية: الجذور الحرة للأكسجين, الإجهاد التأكسدي, استقلاب السرطان, العلاج بالأكسدة/المعادلة الحمرية, البيئة الدقيقة للورم