Clear Sky Science · ar
التحلل المفرط للجلوتامين يحفّز الشيخوخة والهرم عبر تنشيط محور الأرجينين–mTORC1
لماذا يهم هذا البحث لصحة التقدم في العمر
الشيخوخة ليست مجرد تجاعيد وشيب—بل هي فقدان خلايا الجسم تدريجياً لقدرتها على الإصلاح والتجدد. يطرح هذا البحث سؤالاً بسيطاً ظاهرياً له تداعيات كبيرة: هل الطريقة التي تحرق بها خلايانا الحمض الأميني جلوتامين تساهم فعلاً في دفعها نحو الكِبر؟ يكشف المؤلفون سلسلة استقلابية كانت مخفية سابقاً تربط معالجة الخلايا للجلوتامين بمفتاح نمو قوي يُدعى mTORC1، ويظهرون أن تشغيل هذا المسار بشكل زائد يمكن أن يسرّع الشيخوخة الخلوية بنشاط في ذباب الفاكهة والفئران.
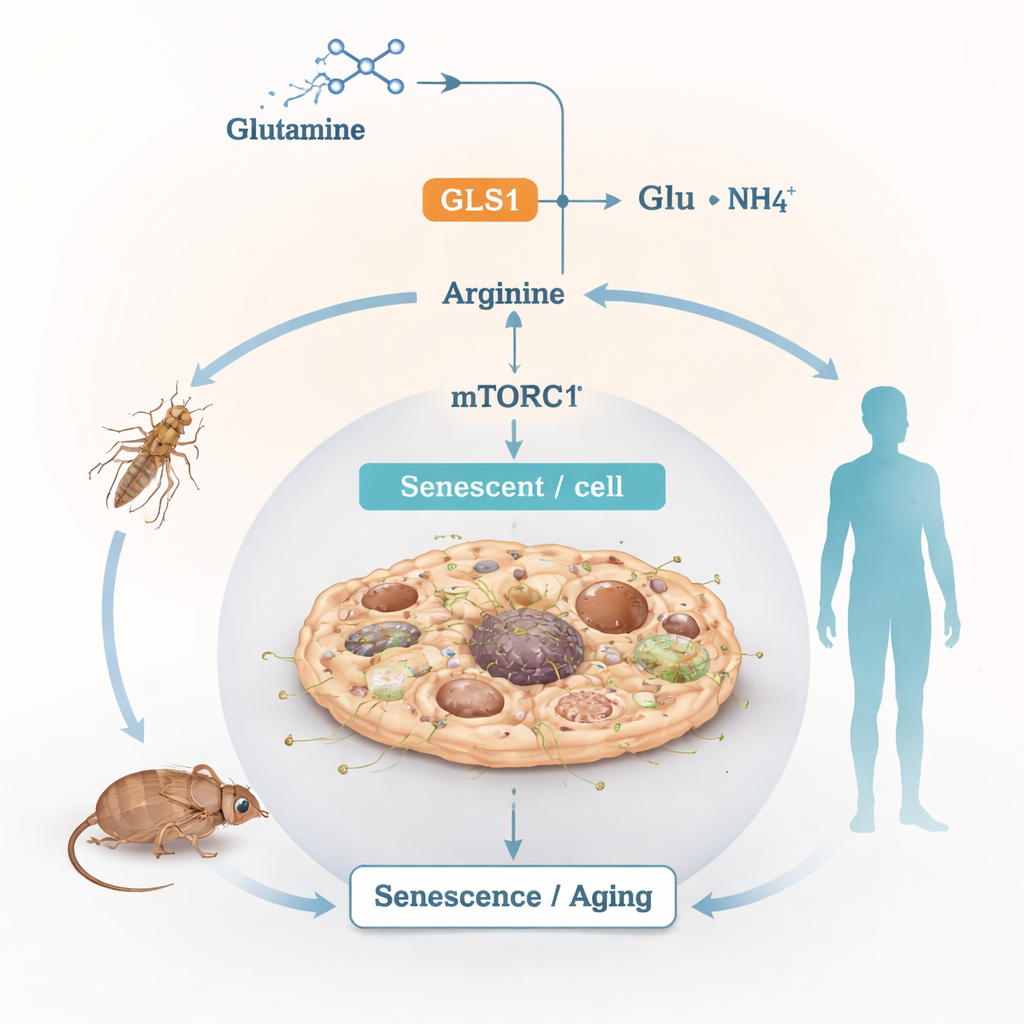
خط وقود يسري بدرجة حرارة مرتفعة للغاية
الجلوتامين هو أكثر الأحماض الأمينية الحرة وفرة في الدم والأنسجة. تستخدمه الخلايا كوقود متعدد الأدوار وكحجر بناء، فتكسّره عبر عملية تُسمى التحلل بالجلوتامين (glutaminolysis). تتولّى إنزيم يُدعى GLS1 الخطوة الأولى، حيث يحول الجلوتامين إلى جلوتامات وأمونيا؛ ومن هناك تغذي النواتج إنتاج الطاقة، والدفاعات المضادة للأكسدة، وصنع أحماض أمينية أخرى. بينما يكون هذا التحلل حيوياً للحياة الطبيعية، تساءل الباحثون ماذا يحدث عندما يصبح نشيطاً بشكل مزمن في سياق الشيخوخة والإجهاد.
اكتشاف «التحلل المفرط للجلوتامين» في خلايا وحيوانات مسنة
باستخدام تقنيات متقدمة لتوصيف المستقلبات، قارن الفريق بين خلايا شابة منقسمة وخلايا شيخوخة—الخلايا الأقدم التي توقفت عن الانقسام وتفرز عوامل التهابية. وجدوا أن مستويات العديد من الأحماض الأمينية زادت، وكان الجلوتامين في مركز الشبكة المعاد توصيلها. استهلكت الخلايا الشاخِخة المزيد من الجلوتامين، وظهر فيها مستوى ونشاط أعلى لـ GLS1، وتراكمت مستويات أعلى من الجلوتامات والأمونيا. ظهرت تغييرات مشابهة في الكائنات كاملة: أظهر ذباب الفاكهة المسن والفئران الكبيرة نشاط GLS مرتفعاً في أنسجة متعددة. سمّى الباحثون هذه الحالة المشتركة من زيادة تحلل الجلوتامين «التحلل المفرط للجلوتامين»، مشيرين إلى أنها سمة محفوظة للشيخوخة وليست مجرد أثر جانبي طفيف.
تخفيض تحلل الجلوتامين يبطئ علامات الشيخوخة
إذا كان التحلل المفرط للجلوتامين يصاحب الشيخوخة، فهل يساهم فعلاً في دفعها؟ لاختبار ذلك، عطل الباحثون تحلل الجلوتامين بعدة طرق: خفضوا الجلوتامين في وسط الزرع، وقموا بتثبيط GLS بأدوية، أو قللوا وراثياً من GLS1. في الخلايا المتعرضة للإجهاد أو المسنة تكرارياً، قطعت هذه التدخّلات علامات الشيخوخة الكلاسيكية مثل تلوين SA-β-gal، ومثبط دورة الخلية p16، وإشارات «SASP» الالتهابية. في ذباب الفاكهة، أدت إما تثبيط GLS وراثياً أو أدوية مثبطة منخفضة الجرعة إلى إطالة العمر الافتراضي، وتحسين قدرة التسلق (اختبار الحيوية)، وتقليل تسرب الأمعاء المرتبط بالسن. والأهم، عندما تم تقييد تحلل الجلوتامين منذ بداية التعرض للإجهاد، لم يكن التأثير ناجماً بالأساس عن قتل الخلايا القديمة، بل عن منعها من الوصول إلى حالة الشيخوخة أصلاً.
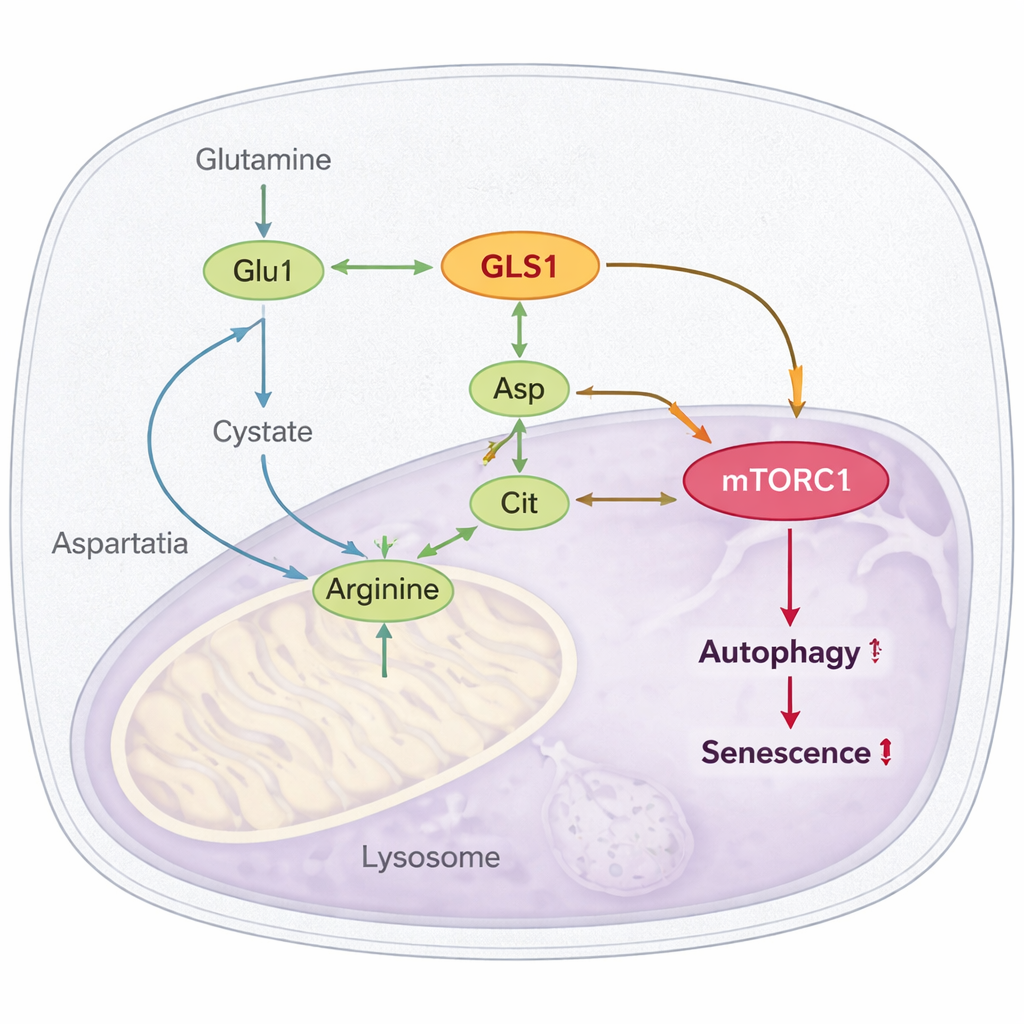
دائرة مخفية: من الجلوتامين إلى الأرجينين إلى mTORC1
أكثر النتائج بروزاً هي كيف يتصل هذا المسار المفرط النشاط بـ mTORC1، المنظم الرئيسي الذي يُعرف أنه يعزز الشيخوخة ويمنع إعادة تدوير الخلايا (الالتهام الذاتي) عندما يبقى مفعّلاً باستمرار. يظهر المؤلفون أن التحلل المفرط للجلوتامين يعزّز إنتاج الأرجينين، حمض أميني آخر ينشط mTORC1 مباشرة. تغذي الجلوتامات والأمونيا الناتجة من الجلوتامين صنع الأسبارتات والسترتولين، والتي تُدمج بعد ذلك لتكوين الأرجينين. في الخلايا والذباب المسنين، ترتفع مستويات الأرجينين وسابقيه؛ وكبح GLS أو إنقاص إنزيم رئيسي في تخليق الأرجينين (ASL) يخفض الأرجينين ويقلل نشاط mTORC1. ويظهرون أيضاً أن بروتين مستشعر الأرجينين CASTOR1 مطلوب لهذا التأثير: عندما يُعطل CASTOR1، لا يؤدي كبح تحلل الجلوتامين إلى تهدئة mTORC1 أو تحسين الالتهام الذاتي، وتختفي فوائد التخفيف من الشيخوخة الخلوية.
عندما يسرّع الإفراط في شيء مفيد الشيخوخة
ليروا إن كان مجرد دفع هذا المسار بقوة أكبر يمكن أن يجعل الخلايا تتقدم في العمر أسرع، أغرق الفريق خلايا صحية نسبياً بالجلوتامين أو الأرجينين أو مجموعات من المستقلبات الوسيطة لأسابيع. كانت النتيجة ارتفاعاً واضحاً في علامات الشيخوخة والجينات الالتهابية. في الذباب، أدت المكملات الطويلة الأمد بالجلوتامين أو الأرجينين إلى تقصير العمر الوسيط والحد الأقصى. مجتمعة، ترسم الدراسة سلسلة كاملة: التحلل المفرط للجلوتامين يضخّم إنتاج الأرجينين، الذي تكشفه CASTOR1، فيبقي mTORC1 مفعّلاً بشكل شاذ، يقمع تنظيف الخلايا، ويعزّز الشيخوخة الخلوية وشيخوخة الكائن الحي.
ما الذي يعنيه هذا لاستراتيجيات مكافحة الشيخوخة المستقبلية
لغير المتخصصين، تعيد هذه الدراسة تأطير استقلاب الجلوتامين كسيف ذو حدين: ضروري للصحة، لكنه قد يكون ضاراً عندما يصبح مفرط النشاط بشكل مزمن في منتصف العمر وما بعده. عبر رسم مسار ملموس من تكسير الجلوتامين إلى فرط تنشيط mTORC1، يبرز المؤلفون نقاط تدخل جديدة—مثل إنزيمي GLS1 وASL أو خطوة استشعار الأرجينين—والتي قد تُعدّل لتبطئ التراجع المرتبط بالعمر دون إيقاف الاستقلاب الحيوي تماماً. ورغم أنه من المبكر جداً تحويل هذه النتائج إلى نصائح غذائية أو علاجات، تضيف الدراسة قطعة مهمة إلى لغز كيف أن معالجة المغذيات اليومية يمكن أن تميل بخلايانا إما نحو المرونة أو نحو تسريع الشيخوخة.
الاستشهاد: Chen, H., Huang, N., Xu, W. et al. Hyperglutaminolysis drives senescence and aging through arginine-mTORC1 axis activation. Sig Transduct Target Ther 11, 64 (2026). https://doi.org/10.1038/s41392-026-02576-w
الكلمات المفتاحية: استقلاب الجلوتامين, الشيخوخة الخلوية, إشارة mTORC1, تخليق الأرجينين, تدخلات مضادة للشيخوخة