Clear Sky Science · ar
مستضد نووي خارجي من فيروس إبشتاين–بار يثير مقاومة الأورام للعلاج المناعي بواسطة ADAR1
لماذا يهم فيروس شائع لعلاج السرطان
العديد من السرطانات تُعالج الآن بأدوية مناعية تطلق العنان لجهاز المناعة في الجسم. ومع ذلك، لا يستفيد معظم المرضى لأن أورامهم تتعلم كيف تختبئ من الهجوم المناعي. تكشف هذه الدراسة كيف يساعد فيروس شائع جداً، فيروس إبشتاين–بار (EBV)، الأورام على إيقاف الدفاعات المناعية ومقاومة هذه الأدوية القوية—وكيف قد تعيد جزيئات مصممة جديدة تنشيط تلك الدفاعات.
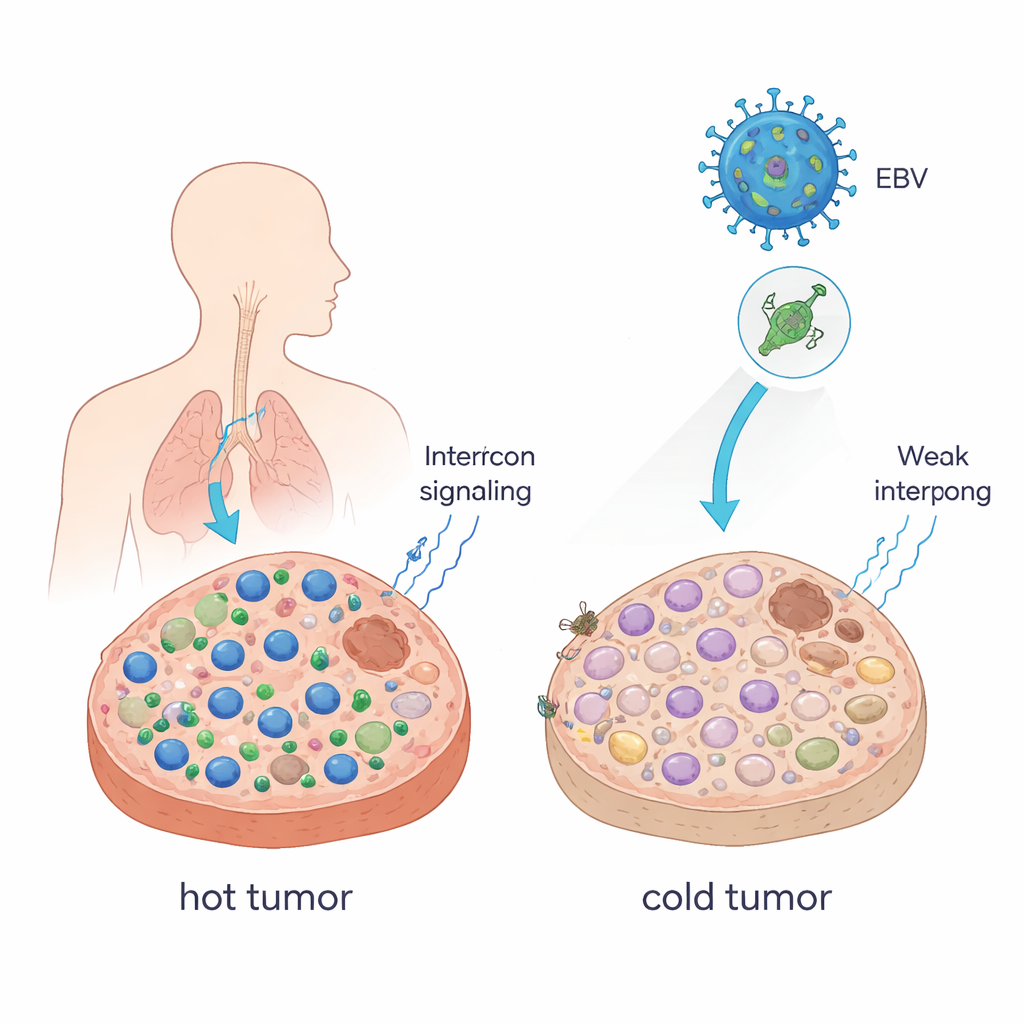
تحويل الأورام الساخنة إلى باردة
غالباً ما يصف الأطباء الأورام بأنها «ساخنة» عندما تكون مملوءة بخلايا T القاتلة للسرطان، و«باردة» عندما تكون تلك الخلايا نادرة. الأورام الحارة عادةً تستجيب جيداً لأدوية كبح نقاط التفتيش المناعية (ICB) مثل الأجسام المضادة لمستقبل PD-1؛ أما الأورام الباردة فعادةً لا تستجيب. أظهر المؤلفون أن بروتين EBV واحداً، يسمى EBNA1، يمكنه دفع الأورام نحو حالة أكثر برودة وتملصاً. عند إجبار خلايا ورم الفأر على إنتاج EBNA1 وزراعتها في فئران ذات جهاز مناعي سليم، كبرت الأورام، واحتوت على خلايا CD8+ وخلايا القاتل الطبيعي أقل، وازداد وجود البلعميات المثبطة للمناعة. كما انخفضت بشكل كبير إشارات الإنترفيرون—المرسلات الأساسية التي تساعد في حشد الخلايا المناعية. في عينات مرضى سرطان البلعوم الأنفي، وهو سرطان مرتبط بشدة بـEBV، أظهرت الأورام التي عبّرت عن EBNA1 نقصاً مماثلاً في خلايا CD8+ مقارنة بالنسيج الطبيعي.
اختصار فيروسي إلى آلية التحكم في RNA داخل الخلية
لفهم كيف يعيد EBNA1 تشكيل بيئة الورم، بحث الباحثون عن بروتينات بشرية تتفاعل جسدياً معه. ركزوا على بروتين يسمى IGF2BP3، الذي يقرأ علامات كيميائية صغيرة (m6A) على الرنا المرسال ويمكنه تعزيز ثباتها أو ترجمتها إلى بروتين. ارتبط EBNA1 بشدة بـIGF2BP3 في عدة أنواع خلوية، بما في ذلك خلايا السرطان الإيجابية لـEBV. أظهرت بيانات من أورام المرضى أن المستويات العالية من IGF2BP3 كانت مصحوبة بنشاط ضعيف لجينات متعلقة بالإنترفيرون وتسلل أقل لخلايا CD8+، مما يوحي بأن هذا التحالف الفيروسي-المضيف قد يخمد المناعة المضادة للورم.
تعزيز مُحرّر RNA الذي يسكت إشارات الخطر
ألقت تحليلات أعمق الضوء على هدف رئيسي لهذا التفاعل: ADAR1، إنزيم يحرر الحمض النووي الريبي مزدوج السلسلة عن طريق تحويل أحرف "A" معينة إلى "I". يمكن لهذا التحرير أن يجعل RNA الشبيه بالڤيروس داخل الخلايا يبدو أقل خطورة للمستشعرات الداخلية، مما يقلل من استجابات الإنترفيرون. وجد المؤلفون أن EBNA1 وIGF2BP3 وعامل الترجمة EIF4G1 يشكلون مركباً ثلاثي الأجزاء على mRNA الخاص بـADAR1. يزيد هذا المركب من تعليمات m6A، ويجند آلية الترجمة، ويعزز إنتاج بروتين ADAR1 بشكل انتقائي دون رفع مستويات الرنا الخاصة به. كنتيجة لذلك، تقوم خلايا الورم بمزيد من تحرير RNA في عناصر جينية متكررة تقع بالقرب من جينات متعلقة بالإنترفيرون. هذه التعديلات تقلل من كمية RNA مزدوج السلسلة غير المحرر الذي كان سيُنبه مستشعرات مثل MDA5 وPKR، مما يضعف إنتاج الإنترفيرون ويساعد الأورام على الاختباء من الهجوم المناعي.
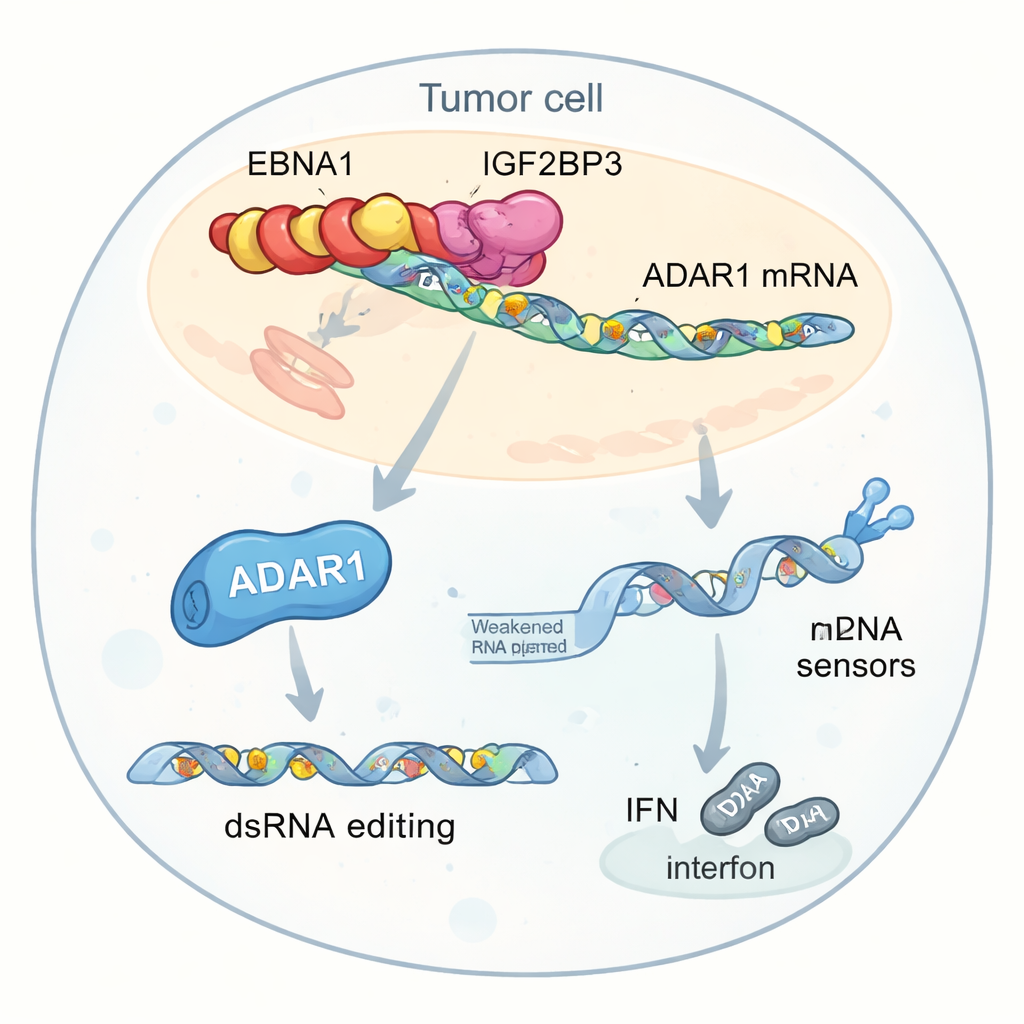
انخفاض الإنترفيرون، ضعف الاستجابة للعلاج المناعي
عندما تعرّضت خلايا الورم المعبرة عن EBNA1 للخلايا T والأجسام المضادة المضادة لـPD-1 في المختبر، كانت أصعب على القتل من الخلايا الضابطة وأطلقت كمية أقل من الإنترفيرون. حتى عند معالجتها مباشرة بالإنترفيرون، كانت الخلايا الحاملة لـEBNA1 أقل حساسية، وكانت مستشعرات RNA الداخلية لديها أقل نشاطاً. أدت خفض مستويات ADAR1 إلى عكس جزئي لهذه التأثيرات، واستعادة نشاط المستشعرات وإشارة الإنترفيرون. أكدت تجارب جينية وتسلسلية أن الخلايا المعبرة عن EBNA1 أظهرت أحداث تحويل A إلى I أكثر في مناطق RNA محددة، خاصة بعد تحفيز بالإنترفيرون، مما يدعم الفكرة بأن تعزيز الفيروس لـADAR1 يساعد في تحييد إشارات الخطر التي كانت ستطلق استجابات مناعية قوية.
مُحلّل مصمم يعيد إيقاظ الهجوم المناعي
سأل الفريق بعد ذلك ما إذا كان تجريد الأورام من EBNA1 يمكن أن يستعيد قابليتها للعلاج المناعي. صمموا جزيء PROTAC، EP-1215، يلصق بـEBNA1 ليعلم بتدميره عبر نظام التخلص داخل الخلية. بجرعات منخفضة، قام EP-1215 بتحلل EBNA1 بكفاءة وخفض مستويات بروتين ADAR1. في تجارب على الفئران، كان لـEP-1215 وحده تأثير محدود على الأورام الإيجابية لـEBNA1، وكان مضاد PD-1 وحده ضعيفاً أيضاً. لكن عند الجمع بين العلاجين، تقلصت الأورام بشكل حاد، وزاد تسلل خلايا CD8+، وارتفعت خلايا T المنتجة للإنترفيرون. في نماذج فأرية مؤنسنة تحمل خلايا مناعية بشرية وأورام مرتبطة بـEBV، تفوق المزيج مرة أخرى على العلاجات المنفردة، من دون سمية ظاهرة للكبد أو الكلى.
ماذا يعني هذا لرعاية السرطان في المستقبل
للأشخاص غير المتخصصين، الرسالة أن فيروساً شائعاً يمكنه إعادة برمجة خلايا السرطان بصمت ليقمع أنظمة الإنذار الداخلية، مطفئاً الإشارات الكيميائية التي كانت ستجذب وتفعّل الخلايا المناعية. يفعل EBNA1 ذلك عن طريق الاستيلاء على قارئ RNA مضيف (IGF2BP3) وعامل ترجمة (EIF4G1) لإنتاج كميات زائدة من محرر الـRNA ADAR1، الذي يحرر هياكل الـRNA نفسها التي وُضعت مستشعرات المناعة للتعرف عليها. من خلال تحلل EBNA1 بواسطة PROTAC مُصمم مثل EP-1215، تمكن المؤلفون من استعادة هذه إشارات الخطر وجعل الأورام المقاومة تستجيب مجدداً لأدوية كبح النقاط التفتيشية الموجودة. إذا ثبت أن استراتيجيات مماثلة آمنة وفعالة لدى البشر، فقد يوفر استهداف مساعدين فيروسيين مثل EBNA1 طريقاً جديداً لتحويل الأورام الباردة المرتبطة بـEBV إلى أهداف ساخنة يمكن للعلاجات المناعية الحديثة القضاء عليها أخيراً.
الاستشهاد: Liu, C., Sun, Z., Li, C. et al. Exogenous Epstein–Barr virus nuclear antigen 1 induces ADAR1-driven tumor resistance against immunotherapy. Sig Transduct Target Ther 11, 63 (2026). https://doi.org/10.1038/s41392-026-02574-y
الكلمات المفتاحية: فيروس إبشتاين-بار, مقاومة العلاج المناعي, ADAR1, تعديل RNA, سرطان البلعوم الأنفي