Clear Sky Science · ar
PKC-إيتا يعزز نقائل سرطان الثدي عن طريق تنظيم مسار هيبو–YAP
لماذا يهم هذا البحث
يعد سرطان الثدي ثلاثي السلبي (TNBC) أحد أخطر أشكال سرطان الثدي لأنه ينتشر مبكرًا ويفتقد إلى علاجات مستهدفة. يكشف هذا العمل كيف تعمل إنزيم داخل الخلايا السرطانية، يُدعى PKC-إيتا (PKCη)، كمفتاح رئيسي يساعد الأورام على الانفصال والتحرك عبر الجسم وتكوين أورام جديدة. ومن خلال فهم هذا المفتاح، يحدد الباحثون أيضًا ببتيدًا طبيعيًا صغيرًا يستطيع تعطيله، ما يشير إلى احتمال طريق علاجي جديد لهذا المرض العدواني.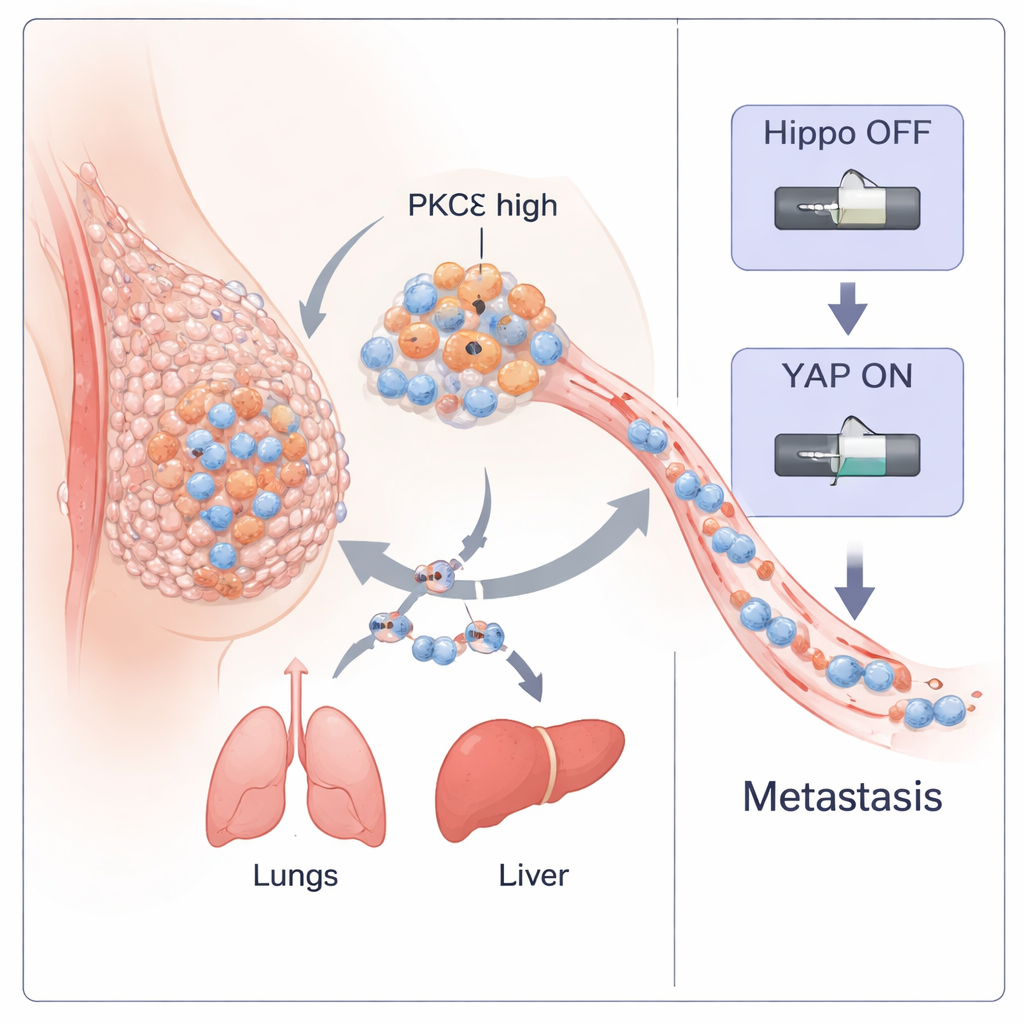
دافع خفي في الأورام العدوانية للثدي
بدأ الفريق بتحليل مجموعات كبيرة من بيانات مرضى سرطان الثدي. وجدوا أن الجين المشفر لـ PKCη (PRKCH) مرتفع بشكل خاص في نوع من الأورام يعرف باسم «انخفاض كلودين» (claudin-low)، الذي يتداخل بقوة مع TNBC ويحتوي على خلايا شبيهة بالخلايا الجذعية وبذات قابلية حركية عالية. عبر تجمعات مرضى متعددة، أظهرت الأورام ذات التعبير العالي لـ PRKCH توقيعات قوية لعملية التحول الظهاري-اللحمي (EMT)—وهي عملية تفقد فيها الخلايا المرتبة تلاصقها، وتغير شكلها، وتصبح أكثر غزوًا. كانت مستويات PRKCH أيضًا أعلى في عينات نقيلية مقارنة بالأورام الابتدائية الأصلية، وأظهر تلوين البروتين في أنسجة TNBC البشرية وجود PKCη نشطًا بالقرب من النواة في الأورام ذات الدرجة الأعلى والمتقدمة. تقترح هذه النتائج مجتمعة أن PKCη مرتبط ارتباطًا وثيقًا بعدوانية الورم وانتشاره.
من طبق المختبر إلى الفأر: إظهار أن PKCη يغذي الانتشار
لاختبار السببية، استخدم الباحثون تحرير الجينات بتقنية CRISPR لإزالة PKCη من سطرين خلويين لـ TNBC شديدَي الانبثاث، أحدهما فأري (4T1) والآخر بشري (MDA‑MB‑231). بدون PKCη، انتقلت الخلايا نحو حالة أكثر «ظهارية»: زاد التعبير عن بروتينات التصاق مثل E‑cadherin وEpCAM، وقَلَّت العلامات التقليدية للحالة اللحامية مثل فيمنتين وN‑cadherin. شكَّلت هذه الخلايا الخالية من PKCη مستعمرات أقل وحجمًا أصغر، وهاجرت وغَزَت بكفاءة أقل، وكانت أكثر حساسية للموت الخلوي عند الانفصال، وأظهرت انخفاضًا حادًا في سمات الخلايا الجذعية السرطانية، بما في ذلك قلة الخلايا CD44high/CD24low وخلايا موجبة لـ ALDH وسعة أقل لتشكيل الكريات. عند حقنها في فئران، أنتجت الخلايا الناقصة PKCη أورامًا أولية أصغر ونقائل أقل بكثير إلى الرئتين والكبد والدماغ وأعضاء أخرى؛ كما عاشت الفئران لفترة أطول. عكس إعادة التعبير عن PKCη هذه التغيرات، مما يؤكد أن الإنزيم يعزز تقدم وانتشار TNBC بشكل فعال.
كيف يختطف PKCη مسار ضبط النمو
ركزت الدراسة لاحقًا على كيفية ممارسته لهذه القوة المحفزة للانبثاث. كشفت بيانات المرضى أن مستويات PKCη ترتفع وتنخفض بالتوازي مع YAP، وهو بروتين مُحَوِّل قوي تتحكم به شجرة إشارات هيبو—وهو «فرامل أمان» خلوية عادةً ما تكبح النمو. تنبأت المستويات العالية من PRKCH أو YAP1 بنتائج أسوأ للمرضى، وكانت المستويات المرتفعة معًا مرتبطة ببقاء خالٍ من النقائل البعيدة أسوأ بشكل خاص. في خلايا TNBC، أدى حذف PKCη إلى خفض إجمالي مستوى YAP وتحويله من النواة إلى السيتوبلازم حيث يكون غير نشط. أظهرت تجارب كيميائية حيوية أن PKCη يرتبط فعليًا بـ YAP ويُضيف له علامة فوسفورية تحديدًا عند الموقع Ser128. تعمل هذه التعديل على تثبيت YAP وتساعده على دخول النواة لتشغيل جينات تدفع EMT والصفات الشبيهة بالجذعية والانبثاث. عند غياب PKCη، يُوسَم YAP بدلاً من ذلك عند مواقع مختلفة (Ser127 وSer397) تؤدي إلى ارتباطه ببروتينات 14‑3‑3 واحتجازه في السيتوبلازم وفي النهاية تحلله. كما يعزز PKCη مستوى PTEN—وهو كابح طبيعي لإنزيم AKT—وبهذا يحافظ على نشاط AKT منخفضًا ويُقمع كينازات هيبو الصاعدة التي كانت ستعطل YAP. بهذه الطريقة، يُفعّل PKCη YAP مباشرة ويمنع ضمنيًا فرملة هيبو من العمل.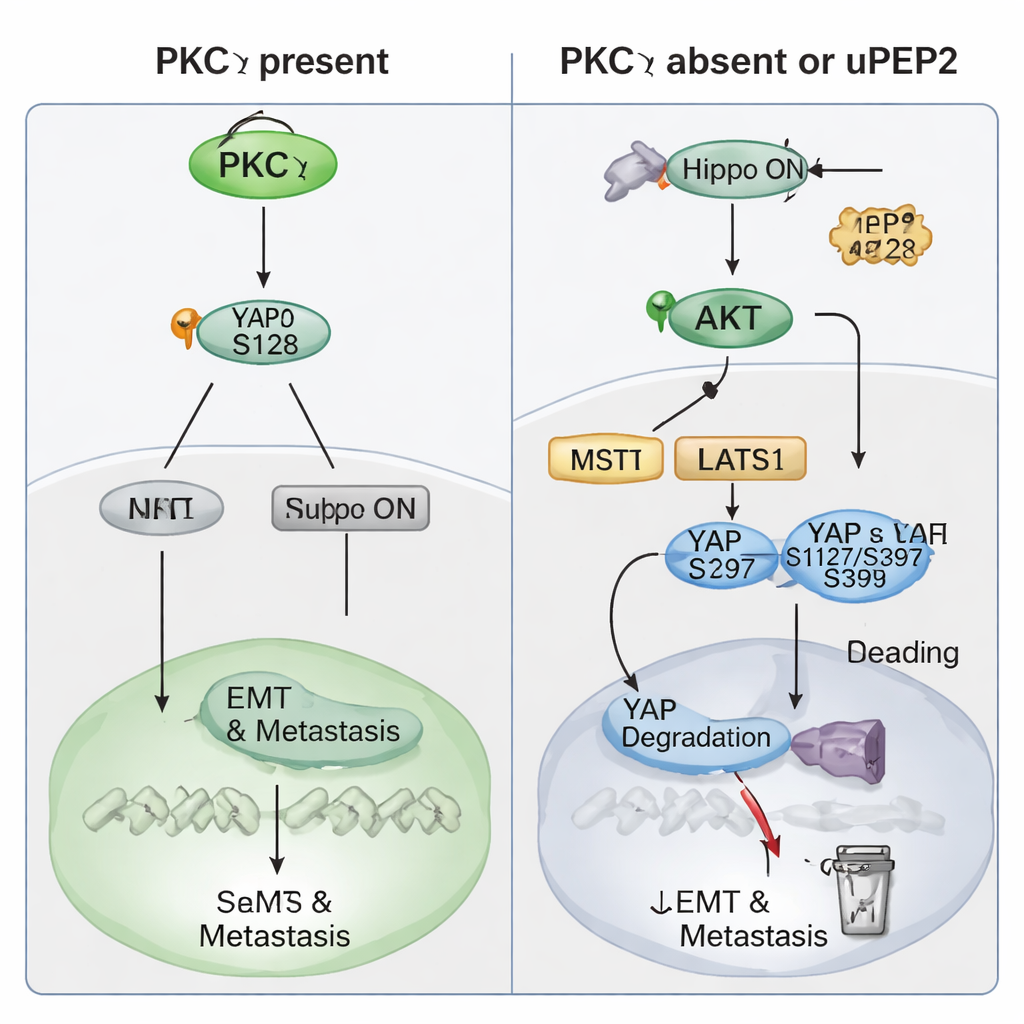
ببتيد صغير يفك تعشيق مفتاح السرطان
ومن المثير أن جين PKCη يحمل إطار قراءة مفتوح قصيرًا سابقًا (uORF) يُشفِّر ميكروببتيدًا يُسمى uPEP2. أظهرت أعمال سابقة أن uPEP2 يمكنه الارتباط بـ PKCη وإعاقة إنزيمات مرتبطة به. هنا، أدى معالجة خلايا TNBC بـ uPEP2 صناعي إلى محاكاة آثار حذف PKCη: انخفضت الهجرة والغزو والسلوك الشبيه بالجذعية، وتحولت علامات EMT نحو ملف أقل عدوانية، وتراجعت مستويات YAP بينما زادت علامات الفسفرة التي تطفئه. في أورام الفئران، خَفَّض uPEP2 من PKCη وYAP في الأورام الأولية، وزاد من تعطيل YAP، وكان مرتبطًا بعدد أقل من النُّقَيْلات الصغيرة في الكبد والرئتين. من الناحية الميكانيكية، يُعزز uPEP2 تحليل PKCη، معيدًا تشغيل مسار هيبو ودافعًا YAP نحو الاحتجاز السيتوبلازمي والتحلل.
ما معناه لعلاجات المستقبل
للقارئ العام، الرسالة الأساسية هي أن الباحثين حددوا PKCη كعنصر محوري يساعد أكثر سرطانات الثدي عدوانيةً على الانفكاك والتحرك واستعمار أعضاء بعيدة عن طريق تعطيل نظام ضبط النمو الطبيعي وتفعيل دواسة الغاز YAP. من خلال إزالة PKCη أو استخدام الببتيد الطبيعي الصغير uPEP2 لتحليله، تمكنوا من إعادة تشغيل فرملة الأمان هيبو، وإسكات YAP، وتقليل النقائل بشكل كبير في نماذج قبل سريرية. وبينما لا يزال هذا العمل في مرحلة تجريبية وأُجري في خطوط خلوية وفئران ذات مناعة ناقصة، فإنه يبرز PKCη وتفاعله مع YAP كأهداف واعدة لعلاجات جديدة لـ TNBC، ويقترح أن عقاقير شبيهة بـ uPEP2 قد تساعد يومًا ما في منع أو الحد من انتشار هذا السرطان الذي يصعب علاجه.
الاستشهاد: Liju, V.B., Waidha, K., Muraleedharan, A. et al. PKC-eta promotes breast cancer metastasis by regulating the Hippo–YAP signaling pathway. Sig Transduct Target Ther 11, 58 (2026). https://doi.org/10.1038/s41392-026-02572-0
الكلمات المفتاحية: سرطان الثدي ثلاثي السلبية, PKC-إيتا, مسار هيبو-YAP, التحول الظهاري-اللحمي, انبثاث السرطان