Clear Sky Science · ar
تحمي Serpina3c من مرض الكبد الدهني المرتبط بخلل التمثّل الغذائي لدى النسل الناتج عن التعرض لبريدنيزون قبل الولادة
لماذا يهم هذا البحث أطفال المستقبل
تحتاج العديد من النساء إلى تناول بريدنيزون أثناء الحمل للتحكم في أمراض مناعية ذاتية والتهابية خطيرة. يعلم الأطباء أنه قد ينقذ حياة الأم، لكن أقل فهماً كيف يؤثر على صحة أطفالهم على المدى الطويل. تطرح هذه الدراسة سؤالاً ملحاً: هل يمكن لتناول بريدنيزون أثناء الحمل أن يمهّد بصمت لكبد الطفل لتطوير مرض الكبد الدهني لاحقاً في الحياة، خصوصاً عند التعرّض لنمط غذائي غير صحي؟ وإذا كان الأمر كذلك، هل توجد طريقة لعكس هذا الخطر؟
مشكلة كبدية متزايدة عالمياً
مرض الكبد الدهني المرتبط بخلل التمثّل الغذائي، أو MASLD، أصبح الآن واحداً من أكثر الأمراض الكبدية المزمنة شيوعاً، ويصيب نحو ثلث سكان العالم مع توقعات بارتفاع النسبة. ويشمل تراكم الدهون البسيط في الكبد، والتهاب دهني «تشمعي»، والتندب، وتليف الكبد، وحتى سرطان الكبد. يرتبط MASLD ارتباطاً قوياً بالسمنة وارتفاع ضغط الدم وداء السكري من النوع الثاني. وكثيراً ما أدرك العلماء أن بذور هذا المرض قد تُزرع قبل الولادة، عندما يتعرض الجنين النامي لضغوط مثل سوء التغذية أو التلوث أو الأدوية. تُعرف هذه الفكرة — بأن بيئات الحياة المبكرة تُشكّل مخاطر الأمراض مدى الحياة — باسم «أصول التطور للصحة والمرض». 
بريدنيزون قبل الولادة كالضربة الأولى
لمعرفة كيف يؤثر بريدنيزون قبل الولادة على الكبد، عالج الباحثون إناث الجرذان والفئران الحوامل بجرعات اختيرت لمحاكاة الجرعات السريرية المنخفضة المستخدمة لدى البشر. ثم تابعوا النسل قبل الولادة وحتى سن البلوغ المبكر. وحدها، كانت الحيوانات الصغيرة المعرضة لبريدنيزون داخل الرحم أصغر حجماً وأظهرت بالفعل علامات على اضطراب في التعامل مع الدهون في الكبد: قطرات دهنية أكثر، وثلاثيات الجليسريد الكبدية أعلى، وكفاءة أقل في استخدام الدهون كمصدر للطاقة. ومع نمو النسل، ظل كبدهم مخزناً للدهون أكثر من المعتاد، حتى مع النظام الغذائي العادي. وعندما تعرّضت الحيوانات لاحقاً لنظام غذائي عالي الدهون — ما يعادل نمط الوجبات السريعة الغربية — أصبحت الاختلافات درامية. طوّر النسل المعرض لبريدنيزون كبد دهني أشدّ، والتهاباً، وفي الذكور ظهرت علامات واضحة على التندب. كما ساءت لديهم السيطرة على سكر الدم، مما يشير إلى اضطراب أيضي أوسع.
بروتين كبدي وقائي يختفي
تعمق الفريق أكثر باستخدام تحليلات جينية واسعة النطاق للبحث عن تغييرات جزيئية مشتركة في أكباد النسل من كلا الجنسين. برزت جينة واحدة: Serpina3c، التي تُنتج بروتيناً مفرزاً ينتمي إلى عائلة مثبطات الإنزيمات الطبيعية. في الجنسين، قلّلت التعرضات قبل الولادة للبريدنيزون Serpina3c في الكبد وفي مجرى الدم بشكل حاد ومستمر، من الحياة الجنينية المتأخرة وحتى البلوغ. وعندما خفض العلماء Serpina3c عمدًا فقط في كبد فئران سليمة، أصبحت تلك الحيوانات أيضاً عُرضة للكبد الدهني وسوء التحكم في السكر، خصوصاً على نظام غذائي عالي الدهون. وبالمقابل، أدّت زيادة Serpina3c في أكباد النسل المعرض لبريدنيزون بعد الولادة إلى إنقاذهم إلى حد كبير: خزّن كبدهم دهوناً أقل، وتعامل مع الجلوكوز بشكل أفضل، وظهر به التهاب وتندب أقل.
كيف يعيد بريدنيزون برمجة مفاتيح التحكم الكبدية
سأل الباحثون بعد ذلك كيف يخفض بريدنيزون Serpina3c. وجدوا أن الشكل النشط لبريدنيزون، بريدنيزولون، يفرط في تنشيط مستقبل الجلوكوكورتيكويد — وهو بروتين يستشعر الدواء موجود في خلايا الكبد. يتعاون هذا المستقبل بعد ذلك مع بروتين آخر، HDAC3، الذي يشدّ تغليف الحمض النووي عبر إزالة شُرَف «أستيل» صغيرة من بروتينات الهستون. في أكباد الحيوانات وخلايا الكبد المزروعة، زاد بريدنيزولون من نشاط مستقبل الجلوكوكورتيكويد وHDAC3 مباشرةً عند جينة Serpina3c، فإزالت علامات الأستيل عند موقع رئيسي يُسمى H3K27. مع إزالة هذه العلامات، انخفض نشاط الجينة وتراجعت مستويات بروتين Serpina3c. أدى حجب المستقبل أو HDAC3، أو تثبيط إزالة الأستيل، إلى استعادة هذه العلامات الأستيلية، ورفع Serpina3c، وتحسين تعامل خلايا الكبد مع الدهون والسكر.
تفاعل سلسلة ضار داخل الكبد
أطلق نقص Serpina3c سلسلة ثانية ضارة. تحت الظروف الطبيعية، يساعد Serpina3c في كبح إنزيمات مثل الكيماز التي تولّد هرمون الأنجيوتنسين II مباشرة داخل الأنسجة. عندما كان Serpina3c نادراً، ارتفعت مستويات ونشاط الكيماز، فانتجت المزيد من الأنجيوتنسين II في الكبد وفُعل مستقبلُه AT1R على خلايا الكبد بشكل مفرط. ومن المعروف أن هذا الارتفاع المحلي في الهرمون يحفز الإجهاد التأكسدي، ومقاومة الأنسولين، وتراكم الدهون، والالتهاب، وتكوّن الندبات. في كلٍ من الحيوانات المعرضة لبريدنيزون والفئران التي خُفض فيها Serpina3c خصيصاً في الكبد، كان مسار الكيماز–الأنجيوتنسين II–AT1R مفَعَّلاً، وكُبِحت جينات رئيسية تدعم حرق الدهون وامتصاص الجلوكوز. أدّت استعادة Serpina3c بعد الولادة إلى تهدئة هذا المسار وإحياء أيض أكثر صحة. 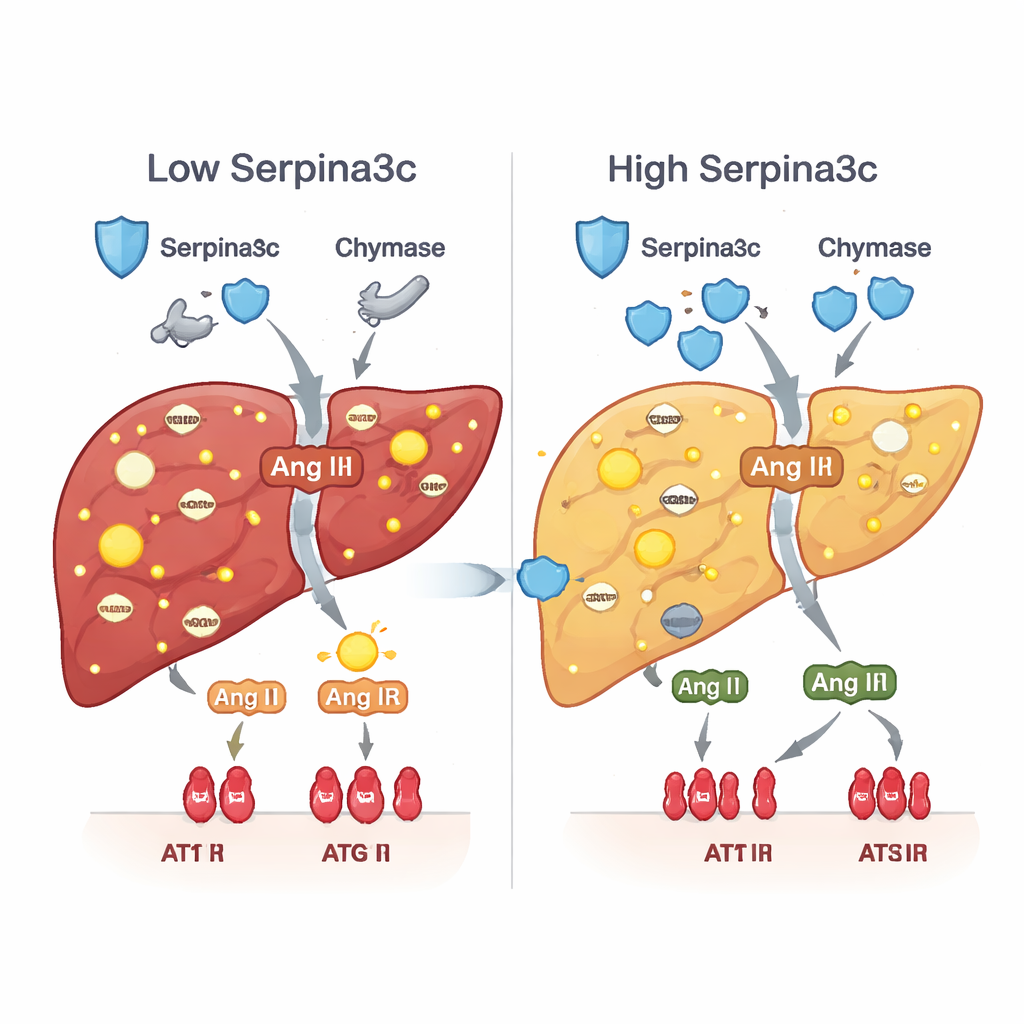
ماذا يعني ذلك للمرضى والأسر
لغير المتخصصين، الرسالة الرئيسية هي أن الأدوية المتناولة أثناء الحمل يمكن أن تترك بصمة جزيئية على الكبد النامي تستمر حتى البلوغ. في هذه الدراسة، عمل بريدنيزون كـ«الضربة الأولى»، خافِضاً بروتيناً وقائياً (Serpina3c) عبر تغييرات إيبيجينية — علامات كيميائية على بروتينات تغليف الحمض النووي — بحيث يسهّل «الضربة الثانية» لاحقاً مثل النظام الغذائي العالي الدهون ظهور مرض الكبد الدهني. والجانب المشجع هو أن هذا الخطر لم يكن ثابتاً: فقد أدت إعادة رفع Serpina3c في الكبد بعد الولادة إلى تقليل تلف الكبد بشكل ملحوظ. ومع أن هذه النتائج مأخوذة من القوارض، فإنها تثير أسئلة مهمة حول كيفية مراقبة ودعم الأطفال الذين احتاجت أمهاتهم بريدنيزون أثناء الحمل، وتشير إلى Serpina3c ونظام الكيماز–الأنجيوتنسين II كمستهدفات واعدة مستقبلاً للوقاية أو علاج مرض الكبد الدهني الذي يبدأ قبل الولادة.
الاستشهاد: Dai, Y., Lu, Z., Peng, Y. et al. Serpina3c protects against metabolic dysfunction-associated steatotic liver disease in offspring induced by prenatal prednisone exposure. Sig Transduct Target Ther 11, 71 (2026). https://doi.org/10.1038/s41392-025-02569-1
الكلمات المفتاحية: بريدنيزون قبل الولادة, مرض الكبد الدهني, علم الوراثة فوق الجزيئي (الإيبيجينيتيكس), Serpina3c, أصول التطور