Clear Sky Science · ar
الفصال العظمي: الآليات الجزيئية المسببة وخيارات علاجية محتملة
عندما يصبح ألم المفاصل اليومي قصة تشمل الجسم كله
غالبًا ما تُعتبر الركب المؤلمة أو الأصابع المتصلبة جزءًا لا مفر منه من التقدّم في العمر. ومع ذلك فالفصال العظمي—أكثر أمراض المفاصل شيوعًا في العالم—ليس مجرد «تآكل واحتكاك». تكشف هذه المقالة الاستعراضية ما يحدث فعلاً داخل المفاصل المؤلمة، من أعصاب الألم التي تعمل بشكل خاطئ إلى آلات الخلية المتعبة، وتستعرض جيلًا جديدًا من العلاجات التي تتجاوز مسكنات الألم البسيطة.
مرض شائع بتكاليف شخصية كبيرة
يصيب الفصال العظمي ما يقرب من 8% من سكان العالم، مع مئات الملايين الذين يعيشون بألم مزمن وقلة في الحركة. يضرب المرض النساء أكثر، والأشخاص فوق 55 عامًا، ومن يعانون زيادة في الوزن أو الذين تضعهم أعمالهم أو رياضتهم تحت ضغط متكرر على المفاصل. الرعاية القياسية الحالية—التمارين، فقدان الوزن، الدعامات، أقراص مضادة للالتهاب، حقن المفصل، وفي الحالات الشديدة استبدال المفصل—يمكن أن تخفف الأعراض لكنها نادرًا ما توقف المرض عن التقدم. هذه الفجوة بين الحاجة والعلاج المتاح دفعت العلماء إلى البحث بعمق أكبر في كيفية بدء الفصال العظمي ولماذا يسبب كل هذا الألم.
لماذا يؤلم المفصل: أسلاك وكيميائيات وإشارات
لا يفسر التصوير بالأشعة وحده ألم الفصال العظمي: فبعض الأشخاص الذين لديهم أضرار طفيفة يؤلمهم الألم بشدة، بينما آخرون مع تغيّرات شديدة يبلغون عن ألم قليل. تتعقب المقالة مسار الألم من مفصل الركبة صعودًا عبر الحبل الشوكي إلى الدماغ. تنتهي الألياف العصبية في المفصل—وخاصة الألياف الرقيقة Aδ وC—مغمورة في خليط من المواد الكيميائية الالتهابية، بما في ذلك الإنترلوكينات وعامل النخر الورمي، وكذلك عامل نمو العصب. هذه المواد تشغّل قنوات خاصة في نهايات الأعصاب تمرر الصوديوم والكالسيوم، مما يجعل الأعصاب تطلق إشارات بسهولة وتيرة أعلى. مع مرور الوقت، يمكن أن تصبح مسارات الألم في الحبل الشوكي والدماغ مفرطة الاستجابة، بحيث يبدو أن الحركة العادية أو برودة طفيفة تسبب إحساسًا قاسيًا وحارقًا.
العبء الخفي داخل خلايا المفصل
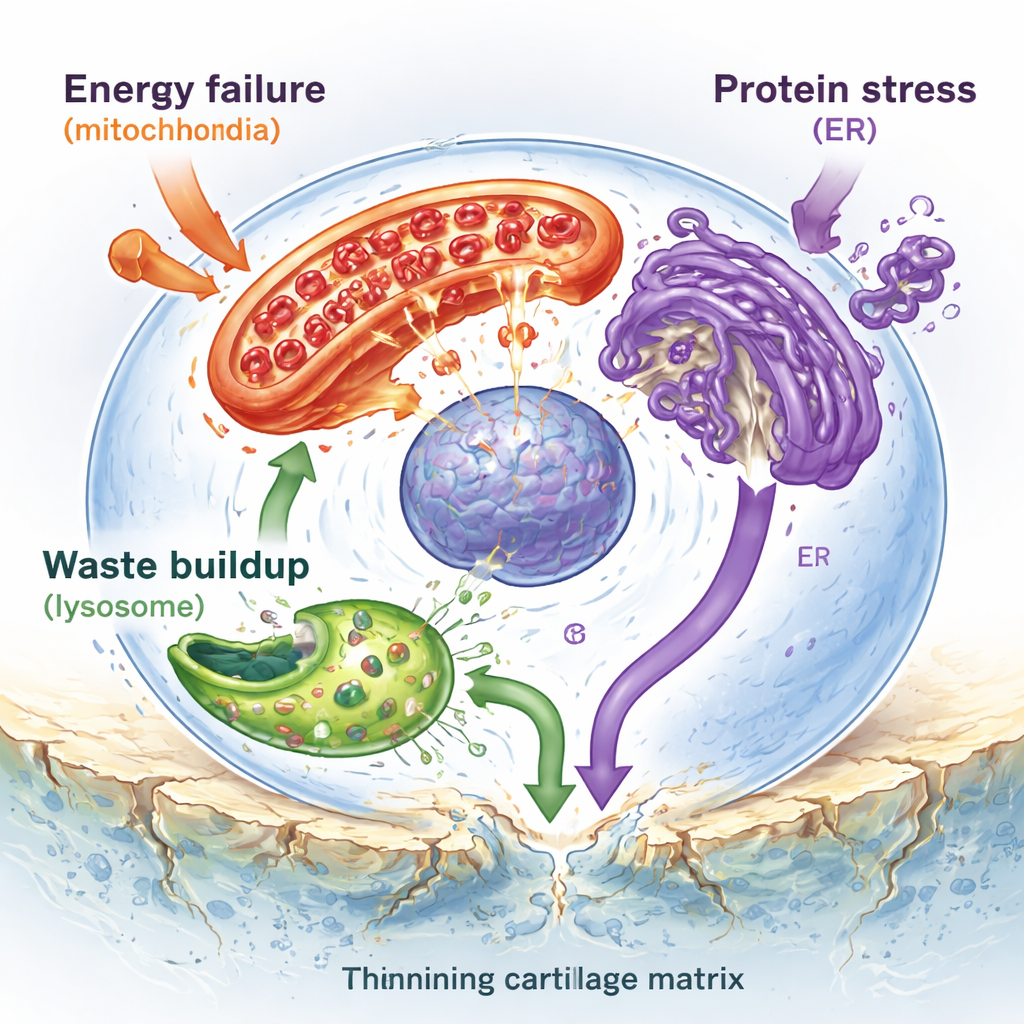
في عمق الغضروف، تحاول الخلايا المقيمة الوحيدة—الخلايا الغضروفية—الحفاظ على مصفوفة ناعمة ومرنة تسمح للعظام بالانزلاق. يبين المؤلفون أن هذه الخلايا تتعرض لهجوم من عدة جهات. تتعرض الميتوكوندريا، محطات الطاقة الصغيرة في الخلية، للضرر وتصبح أقل كفاءة، فتنتج طاقة غير كافية وجزيئات أكسدة تفاعلية زائدة تلحق الضرر بالحمض النووي والبروتينات. تُطغى الليسوزومات، مراكز إعادة التدوير في الخلية، ببلورات معدنية صلبة، ما يضعف أغشيتها بحيث تتسرب إنزيمات مدمرة إلى داخل الخلية وتطلق موت الخلية. يصبح الشبكة الإندوبلازمية، المتاهة الغشائية حيث تُطوى البروتينات الجديدة، مزدحمة بجزيئات مطوية بشكل خاطئ، مما يطلق «استجابة إجهاد» مزمنة تدفع الخلايا في النهاية نحو الانتحار الخلوي. معًا، تغذي هذه العضيات المتعبة الالتهاب وتسارع فقدان الغضروف وتكلسه.
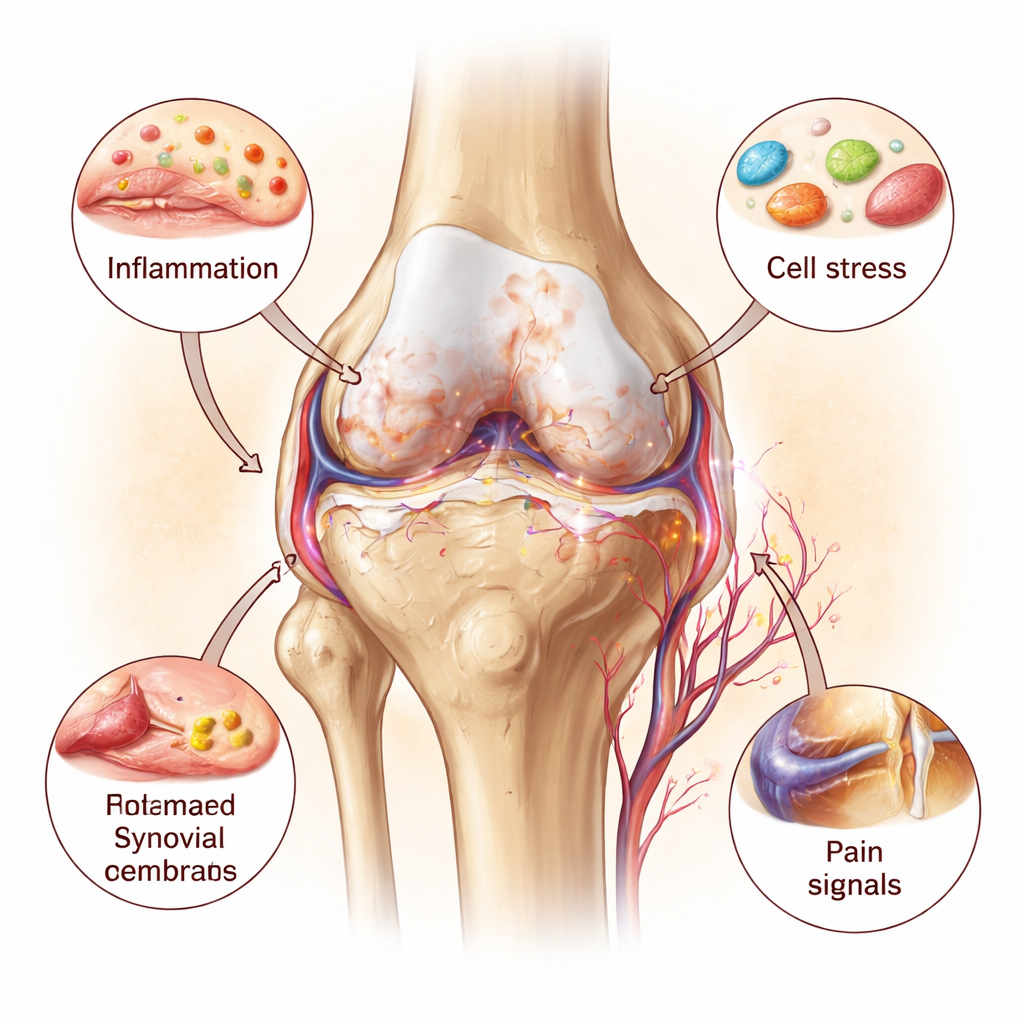
الالتهاب: وقود للنار
جزيئات الرسائل الالتهابية هي مكبرات الصوت لهذه العملية. ثلاث منها على وجه الخصوص—الإنترلوكين‑1، الإنترلوكين‑6، وعامل النخر الورمي‑ألفا—تشكل حلقة شريرة مع تلف العضيات. تحفّز الخلايا الغضروفية على إنتاج إنزيمات تفسد الغضروف وتشجع نموًا عظميًا غير طبيعي تحت سطح المفصل. في الوقت نفسه، تطلق الميتوكوندريا المصابة والليسوزومات المتسربة إشارات استغاثة خاصة بها، والتي تنشط أجهزة الاستشعار المناعية داخل المفصل أكثر. تنمو الأوعية الدموية وألياف الألم داخل مناطق من الغضروف كانت هادئة وخالية عادة من الأعصاب، مما يزيد حساسية الألم. تصور هذه النظرة للمفصل بأكمله الفصال العظمي كمرض التهابي بطيء الحركة ولكنه معزز ذاتيًا، وليس مجرد تآكل ميكانيكي سلبي للغضروف.
أفكار علاجية جديدة: من قنوات الأيونات إلى مصانع الطاقة الخلوية
مسلحين بهذه الخريطة الميكانيكية، يختبر الباحثون عقاقير وأنظمة توصيل جديدة. في جانب الألم، تحجب أدوية تجريبية أو تخفف حساسية قنوات الأعصاب مثل TRPV1 (مستقبل الكابسيسين)، TRPA1، TRPM3/8، وبعض قنوات الصوديوم المحددة (Nav1.7 وNav1.8)، أو تحيد عامل نمو العصب لمنع فرط حساسية الأعصاب. في جانب تعديل المرض، تستهدف الأجسام المضادة المحددة خفض السيتوكينات الالتهابية الأساسية، بينما تحاول الجزيئات الصغيرة وعوامل «سِنو ليتك» استعادة سلوك خلوي أكثر صحة. حدٌّ مثير بشكل خاص هو العلاج الموجّه إلى العضيات: مركبات تحفز تنظيف الميتوكوندريا (الالتهاب الميتوكوندري)، وتثبت حموضة وغشاء الليسوزومات، أو تقلل من إجهاد الشبكة الإندوبلازمية. تُصمم جسيمات نانوية متقدمة، ليبوزومات، وإكسوزومات مهندسة لاستهداف خلايا الغضروف وحتى عضيات محددة، لتوصيل الأدوية بدقة إلى المواضع التي تحتاجها.
ما يعنيه هذا للأشخاص المصابين بالفصال العظمي
تخلص المقالة إلى أن الفصال العظمي يجب أن يُنظر إليه ويُعالَج كاضطراب بيولوجي معقّد يشمل اضطرابًا في استقلاب الخلايا، والتهابًا مزمنًا منخفض الدرجة، ودوائر ألم تكيفية خاطئة. بينما الكثير من الأدوية ونظم التوصيل المقترحة لا تزال في الاختبار المخبري المبكر أو تجارب على الحيوان، فإنها تشير إلى مستقبل يكون فيه العلاج متعدد الأوجه وشخصيًا: تخفيف الألم بهدوء الأعصاب المفرطة النشاط، وفي نفس الوقت حماية أو تجديد خلايا المفصل وآلاتها الداخلية. بالنسبة للمرضى، قد يعني هذا في نهاية المطاف علاجات لا تقلل الألم فحسب، بل تبطئ أو ربما تعكس التلف البُنيوي الذي يُعتبر اليوم غالبًا أمراً حتميًا.
الاستشهاد: Zhang, Y., Han, Y., Sun, Y. et al. Osteoarthritis: molecular pathogenesis and potential therapeutic options. Sig Transduct Target Ther 11, 81 (2026). https://doi.org/10.1038/s41392-025-02556-6
الكلمات المفتاحية: الفصال العظمي, ألم المفاصل, الغضروف, الالتهاب, الميتوكوندريا