Clear Sky Science · ar
اكتشاف وتطوير الأدوية المضادة للفيروسات: التحديات والاتجاهات المستقبلية
لماذا ما زلنا بحاجة إلى أدوية أفضل لمكافحة الفيروسات
أظهرت جائحة كوفيد-19 مدى سرعـة قدرة فيروس جديد على قلب حياة الناس اليومية—وكم نعتمد على أدوية فعالة عندما لا تكفي اللقاحات وحدها. يستعرض هذا المقال تاريخ ستين عاماً من تطوير الأدوية المضادة للفيروسات ويتساءل: كيف يمكننا بناء دفاعات أسرع وأكثر ذكاءً وأوسع ضد التهديدات الفيروسية المستقبلية؟ ويشرح، بلغة يسهل على الجمهور العام فهمها، كيف يكتشف العلماء ويصممون ويوصلون الأدوية المضادة للفيروسات، وماذا تعلموا من كوفيد-19، وكيف قد تغير أدوات مثل الذكاء الاصطناعي وتقنية النانو قواعد اللعبة.
من أول مضادات الفيروسات إلى ترسانة اليوم
يعد طب المضادات الفيروسية مجالاً شاباً نسبياً. أظهر الدواء الأول الموافق عليه، إيدوكسيوريدين في الستينيات، أن تعديل لبنات بناء الحمض النووي يمكن أن يبطئ تكاثر الفيروس، لكنه كان يضر أيضاً بالخلايا السليمة وله استخدام محدود على سطح العين. ثم ظهر الأسكلوفير، دواء بارز للهربس يُفعَّل بشكل أساسي داخل الخلايا المصابة، مما جعله فعالاً وآمناً في الوقت نفسه. في ثمانينيات القرن الماضي أصبح الزيدوفودين أول علاج لفيروس العوز المناعي البشري، فاتحاً الباب للعلاجات المركبة الحديثة التي حولت الإيدز إلى حالة مزمنة يمكن التعامل معها. على مدى العقود، ساعدت الكيمياء الأفضل والتصميم بمساعدة الحاسوب في تقديم أدوية أكثر دقة ضد الإنفلونزا والتهاب الكبد ب وسي وHIV وأخيراً SARS‑CoV‑2. يتتبع الاستعراض هذا التسلسل الزمني ويبيّن كيف أدخل كل اختراق طريقة جديدة للتفوق على الفيروسات.
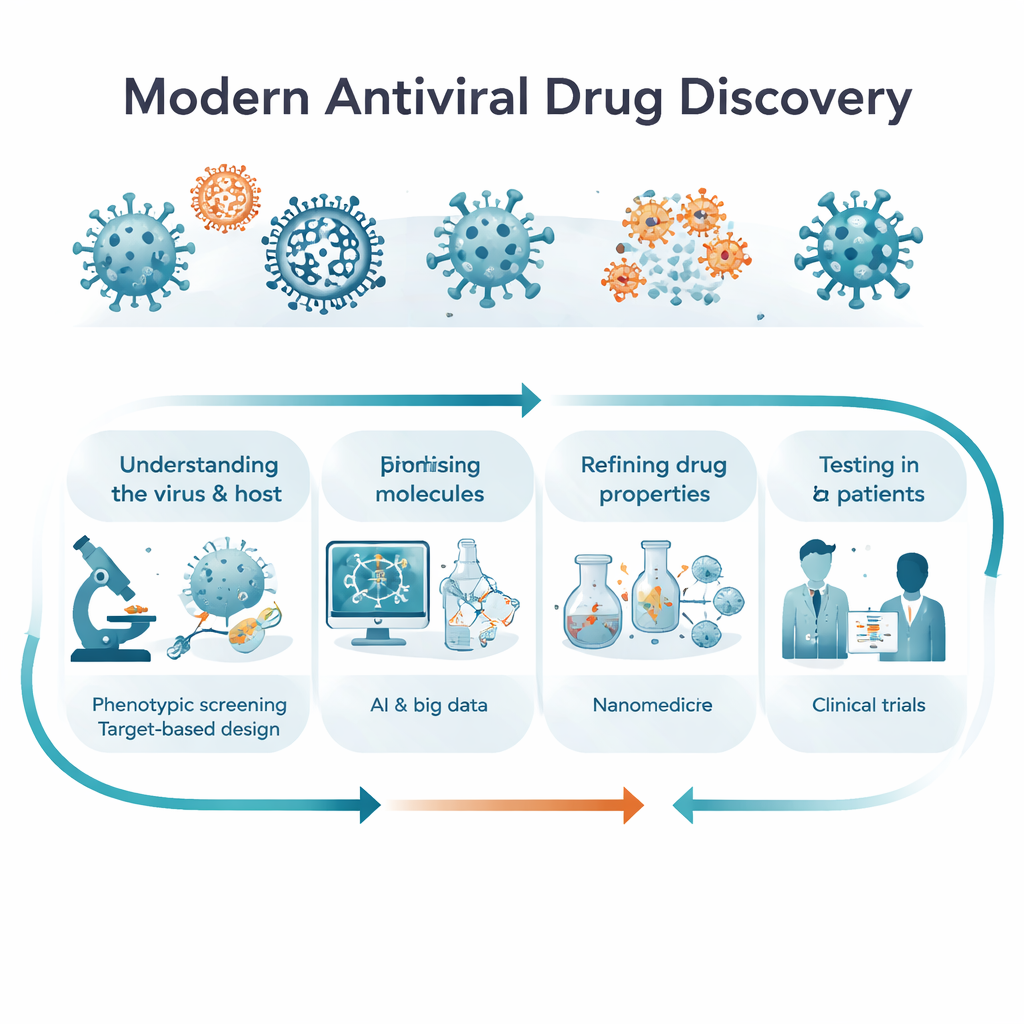
طريقتان للعثور على دواء جيد: مراقبة الخلايا مقابل استهداف الأهداف
عادةً ما يتبع الباحثون مسارين مكملين للأدوية المضادة للفيروسات. في اكتشاف «الظاهراتي» لا يبدأون ببروتين محدد؛ بدلاً من ذلك يعرضون خلايا مصابة أو كائنات نموذجية لآلاف الجزيئات ويسألون ببساطة: أيها يبقي الفيروس تحت السيطرة والخلايا على قيد الحياة؟ يمكن أن يكشف هذا عن أدوية مبتكرة وغير متوقعة، بما في ذلك أدوية تعمل على أكثر من مسار واحد. في اكتشاف «مبني على أهداف» يحدد العلماء أولاً بروتيناً فيروسياً أو بشرياً حاسماً للعدوى—مثل البوليميراز أو البروتياز أو إشارة مناعية—ثم يصممون جزيئات لحجب ذلك الهدف أو ضبطه. يشرح المقال كيف تختلف هاتان الاستراتيجيتان، ولماذا كل منهما ضروري في مراحل بحثية مختلفة، وكيف من المرجح أن تدمج المشاريع المستقبلية بينهما، متدرجةً بسلاسة من المراقبة الواسعة إلى فهم جزيئي دقيق.
ضرب الفيروس—ونظام دعمه—حيث يؤلم
لا تقتصر الأدوية المضادة للفيروسات الحديثة على إعاقة إنزيم فيروسي واحد فحسب. يسير الاستعراض عبر دورة حياة الفيروس، من دخوله إلى الخلية إلى نسخ الجينوم وإطلاقه، ويسلط الضوء على أنواع الأدوية التي تتداخل في كل مرحلة. ترتبط بعض المركبات بالإنزيمات الفيروسية أو البروتينات البنائية مباشرة. أما الأخرى فتعمل عبر استهداف عوامل المضيف التي تعتمد عليها الفيروسات—كمستقبلات سطح الخلية أو إنزيمات التمثيل الغذائي الرئيسية أو مسارات المناعة الفطرية مثل الإنترفيرونات ومستقبلات شبيهة بالتول—وبالعمل على بروتينات «المساعدة» للمضيف تقلل هذه الأدوية من احتمال تمكن فيروس يتحور سريعاً من الهروب. كما يصف المؤلفون أفكاراً ناشئة مثل جزيئات صغيرة تعطل «القطرات» الخالية من الغشاء داخل الخلايا حيث تتجمع الفيروسات، أو التي تؤدي إلى تحلل انتقائي للبروتينات والحمض النووي الريبي الفيروسي بدلاً من مجرد حجبها.
تصميم جزيئات أفضل: الشكل، الخصائص، وطرق الإيصال
تحويل «الضربة» الأولية إلى دواء مفيد يعني أكثر من تعظيم الفعالية. يقوم الكيميائيون بضبط شكل وشحنة الجزيئات لتناسب أهدافها كما المفتاح في القفل، مسترشدين غالباً بهياكل بروتينية عالية الدقة والمحاكاة. كما يعدلون ذوبانها في الماء وثباتها وعمليات التمثيل لضمان وصول الدواء إلى النسيج الصحيح، وبقائه نشطاً لفترة كافية، وتجنبه للسُمية المفرطة. يقدم المقال أمثلة على كيف يمكن لتغييرات صغيرة—كإضافة سلسلة جانبية أو تكوين ملح—رفع النشاط ضد سلالات مقاومة من فيروس HIV أو كورونا مع تحسين السلامة. كما يشرح الأدوية البديلة (prodrugs)، وهي أشكال غير نشطة أو أقل نشاطاً مصممة لأن تتحول داخل الجسم، وأنظمة الإيصال المستهدفة مثل علامات سكرية موجهة للكبد وجسيمات دهنية نانوية تنقل بأمان الحمض النووي الرسول الهش أو أدوية الأحماض النووية إلى الخلايا.
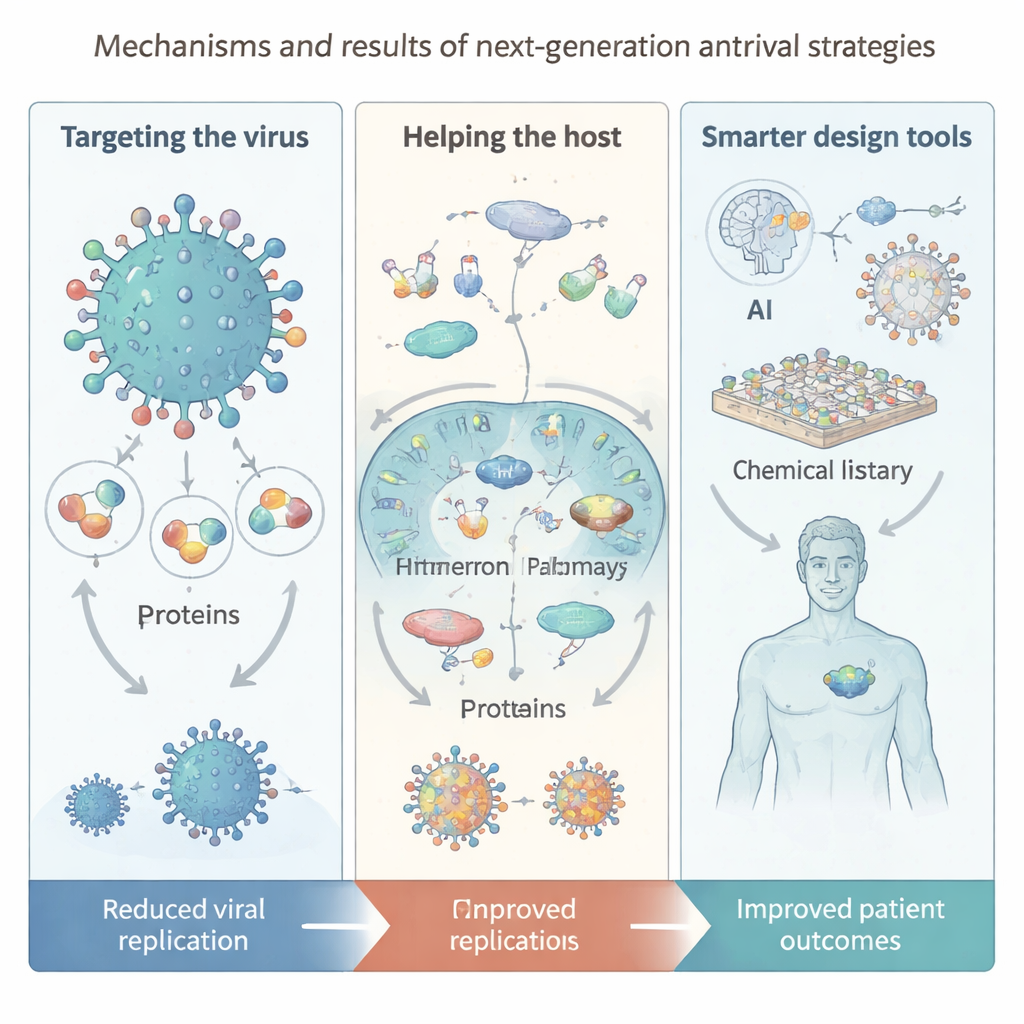
أدوات جديدة: الذكاء الاصطناعي، مكتبات هائلة، وتقنية النانو
موضوع رئيسي في الاستعراض هو كيف تعيد التكنولوجيا تشكيل اكتشاف مضادات الفيروسات. يساعد الذكاء الاصطناعي الآن في التنبؤ بهياكل البروتين، والبحث في مكتبات «افتراضية» هائلة تحتوي على مليارات الجزيئات المحتملة، واقتراح مركبات أو تركيبات دوائية جديدة. تتيح مكتبات مشفرة بالحمض النووي ومنصات الببتيدات الكبيرة الحلقية فحص مساحات كيميائية هائلة بسرعة فائقة، بينما تسرع أنظمة التخليق والتنقية الآلية حلقة البناء والاختبار. وعلى صعيد الإيصال، توفر تقنية النانو جسيمات شبيهة بالفيروسات وبوليمرات ذكية و«نانوزايمات» يمكن أن تتلف أغطية الفيروس مباشرة أو تعزز الاستجابة المناعية. مع ذلك يحذر المؤلفون من أن نماذج الذكاء الاصطناعي لا تزال تعتمد على بيانات عالية الجودة، وأن العديد من الجزيئات المولدة يصعب تصنيعها أو اختبارها، وأن قضايا السلامة والعدالة والخصوصية يجب التعامل معها مع تزايد مركزية هذه الأدوات.
إلى أين يتجه اكتشاف أدوية مضادة للفيروسات
للقارئ العام، الرسالة الرئيسية للمقال مزيج من الواقعية والأمل. تتحور الفيروسات بسرعة، ولا وجود لحبة واحدة تعمل إلى الأبد أو ضد كل تهديد. لكن عبر التعلم من كوفيد-19، وتعميق فهم تفاعلات الفيروس–المضيف، ودمج الكيمياء الذكية والبيولوجيا المتقدمة والذكاء الاصطناعي وتقنية النانو، يبني العلماء صندوق أدوات مضاد للفيروسات أكثر مرونة. من المرجح أن تكون العلاجات المستقبلية أوسع نطاقاً، أكثر تحملاً، ومصممة لضرب ليس الفيروس فحسب بل «النقاط الضعيفة» في عملية العدوى. وسيكون التعاون المستمر عبر التخصصات والصناعات والدول ضرورياً لتحويل هذه التقدمات العلمية إلى أدوية عملية وميسورة التكلفة قبل وصول الجائحة القادمة.
الاستشهاد: Du, S., Hu, X., Li, P. et al. Antiviral drug discovery and development: challenges and future directions. Sig Transduct Target Ther 11, 69 (2026). https://doi.org/10.1038/s41392-025-02539-7
الكلمات المفتاحية: اكتشاف الأدوية المضادة للفيروسات, علاجات COVID-19, مضادات الفيروسات المستهدفة للمضيف, الذكاء الاصطناعي في تصميم الأدوية, تقنية النانو في الطب