Clear Sky Science · ar
الميكرونوى: الأصول، الاختبارات، الآليات، الأمراض والعلاجات
فقاعات خفية داخل خلايانا
في أعماق خلايانا، تتكشف فقاعات صغيرة «قمرية» من الحمض النووي تُدعى الميكروأنوية لتكون أكثر من مجرد غرائب تحت المجهر. كانت تُعتبر سابقًا بقايا غير ضارة نتيجة انقسام الخلية، لكن هذه الكريات الصغيرة المليئة بالحمض النووي ترتبط الآن بتطور السرطان، وردود الفعل المناعية، وحتى بعلاجات محتملة جديدة. فهم أسباب تكوّن الميكروأنوية، وما يحدث لها، وكيف تؤثر على جيناتنا يعيد تشكيل طريقة تفكير العلماء حول تلف الجينوم والأمراض.
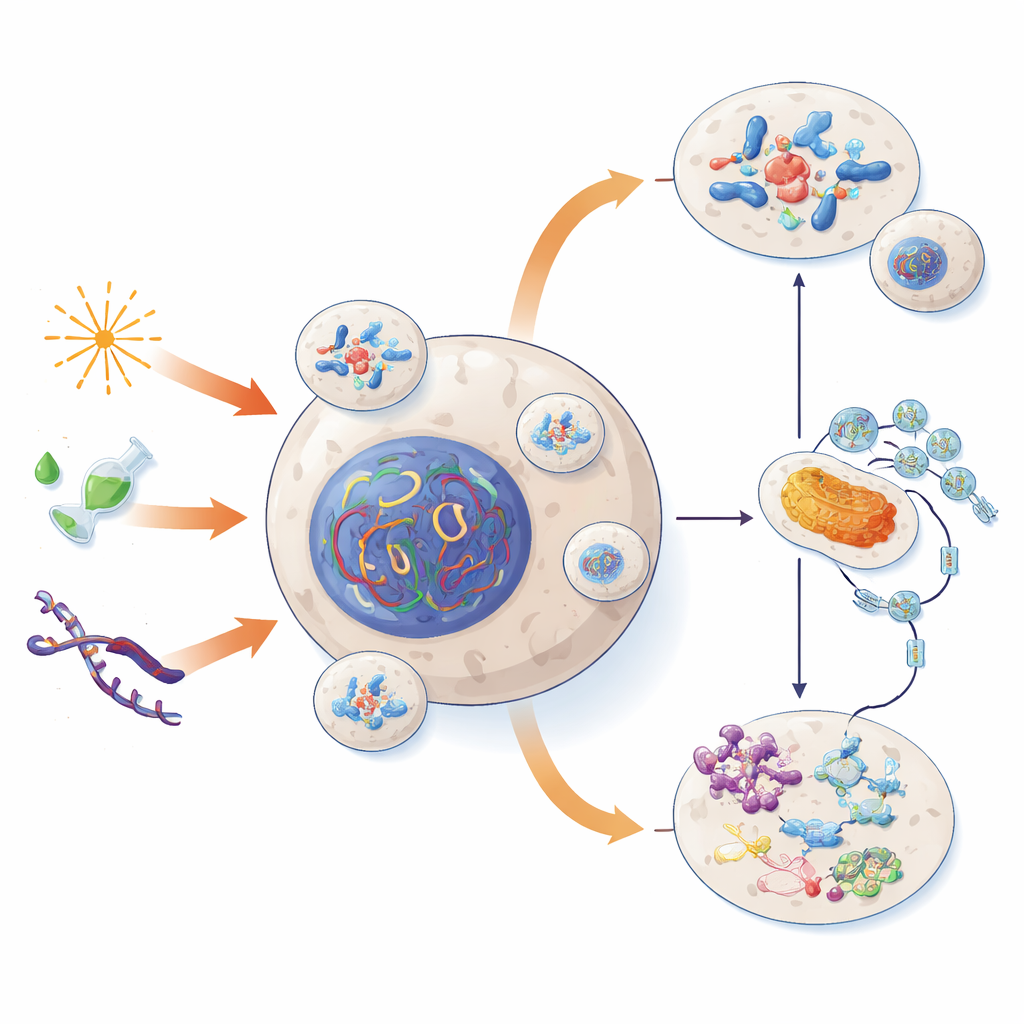
كيف تولد فقاعات الحمض النووي الصغيرة
تظهر الميكروأنوية عادةً عندما يحدث خطأ أثناء انقسام الخلية. عادةً تصطف الكروموسومات وتُسحَب بالتساوي إلى خليتين جديدتين. لكن إذا تعطل جهاز الانقسام أو تعرَّض الحمض النووي للكسر، فقد يتأخر كروموسوم كامل أو قطعة منه ويُحاط بغلاف صغير منفصل خارج النواة الرئيسية. يمكن أن تحفز الأشعة أو المواد السامة أو تآكل نهايات الكروموسومات (التيلوميرات)، أو أخطاء في بروتينات «الأزامل» التي تسحب الكروموسومات هذا الخطأ في التوزيع. في بعض الحالات، تنبثق النواة نفسها عن أجزاء إضافية من الحمض النووي خلال الفترات الهادئة بين الانقسامات، مكوِّنة ميكرونويات بدون انقسام خلوي كامل.
ما مصير جزر الحمض النووي الضالة
بعد تكوّنها، يمكن أن تسلك الميكروأنوية عدة مسارات مختلفة، لكل منها عواقب مغايرة على الخلية. بعضها يُعاد امتصاصه في النواة الرئيسية في انقسامات لاحقة، معيدًا إدماج حمضه النووي بهدوء — أحيانًا مع تغييرات دقيقة ومستمرة في نشاط الجينات. بعضها الآخر يبقى كجسم منفصل ويتم تمريره لخليّة من الخليتين الابنتين فقط، مما يزيد التنوع الجيني بين خلايا النسيج. تُهضم بعض الميكروأنوية عبر عمليات «تنظيف ذاتي» خلوية، بينما تُطرد أخرى فعليًا خارج الخلية تمامًا. لكن المصير الأكثر درامية هو التمزق: فغلافها الخارجي الهش غالبًا ما ينفصل، فينقلب الحمض النووي التالف داخلها إلى الخلية ويُعرَّض لقوى مدمرة.
من الكروموسومات الممزقة إلى الفوضى
عندما تتمزق ميكرونواة أو يُنسخ حمضها النووي بشكل خاطئ، قد تتحطم الكروموسومة المحبوسة في داخلها إلى عشرات أو مئات القطع. ثم تُعاد خياطة هذه الشظايا معًا بشكل متسرع ومعرض للأخطاء، وهي ظاهرة تُعرف بتحطم الكروموسومات (كروموثريبسيس). بدلاً من تراكم طفيف للطفرات عبر سنوات، قد تكتسب الخلية اضطرابًا وراثيًا هائلًا ومحدودًا في حدث واحد. قد تُفقد جينات مهمة أو تُخلط أو تُنسخ مرات متعددة. يمكن أن تتشكل قطع دائرية إضافية من الحمض النووي وتحمل عدة جينات تحفّز النمو، مما يمنح الخلية مزايا قوية جديدة. ما إذا كان هذا التغير يفيد الخلية أم يضرها يعتمد على الجينات المتأثرة، لكن في كثير من السرطانات تساعد هذه الأحداث الأورام على النمو والانتشار أو مقاومة العلاج.
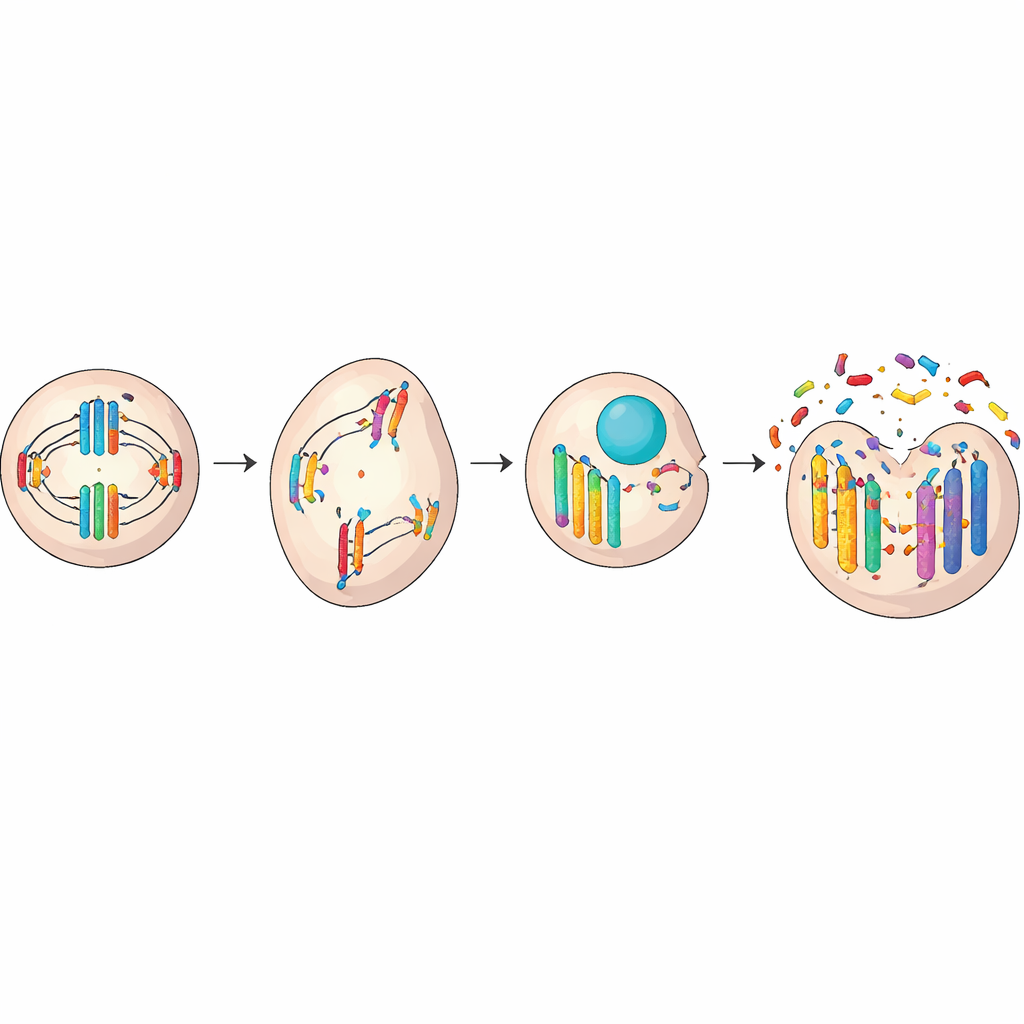
إشارات توقظ الجهاز المناعي
يعمل الحمض النووي المتسرِّب من الميكروأنوية المتمزقة أيضًا كجرس إنذار. تحافظ خلايانا عادةً على حمضها النووي محبوسًا داخل النواة، لذا يبدو الحمض النووي الحر في السيتوبلازم مريبًا كما لو كان من فيروس أو بكتيريا. يمكن لبروتين مستشعر يُدعى cGAS أن يلتصق بهذا الحمض النووي الضال ويُفعِّل شريكًا يُدعى STING، مُطلقًا استجابات التهابية ومضادة للفيروسات. في الحالات الصحية، يساعد ذلك على إزالة الخلايا التالفة أو الخطرة. لكن في العديد من السرطانات المتقدمة، تجد الخلايا الورمية طرقًا لتخفيض أو إعادة توصيل هذا النظام الإنذاري. بدلًا من إثارة هجوم مناعي، يمكن للإشارات المزمنة منخفضة المستوى الناتجة عن ميكرونويات متكررة أن تساعد الخلايا السرطانية على أن تصبح أكثر غزوًا وأكثر قدرة على التهرب من دفاعات الجسم.
قياس الميكروأنوية وتسخيرها
بما أن الميكروأنوية تُشير بصريًا إلى تلف الحمض النووي، فقد أصبحت أدوات مفيدة في الطب والصحة العامة. تكشف اختبارات صبغ بسيطة على خلايا الدم أو خلايا الخد أو كريات الدم الحمراء مقدار الضغط الجيني الذي تعرض له الشخص من التلوث أو التعرضات المهنية أو التدخين أو المرض. الأشخاص المصابون بأنواع معينة من السرطان أو فشل القلب أو أمراض الكلى أو اضطرابات وراثية في إصلاح الحمض النووي غالبًا ما يظهرون أعدادًا مرتفعة من الميكروأنوية. يستخدم الباحثون الآن طرق تصوير وفرز عالية الإنتاجية لتنقية الميكروأنوية، وفهرسة محتوياتها من البروتين والحمض النووي، ورسم خريطة كيفية ترك أنواع مختلفة من الإجهاد بصمات «تعديلية» وبنيوية مميزة بداخلها.
مخاطر جديدة وفرص جديدة
تقع الميكروأنوية عند مفترق طرق بين الضرر والدفاع: فهي قد تُدفع إلى إعادة ترتيب الجينوم بشكل خطير وتفعيل الحماية المناعية في الوقت نفسه. بعض العلاجات التجريبية للسرطان تزيد عمدًا من أخطاء فصل الكروموسومات أو تعيق مسارات إصلاح الحمض النووي المحددة لإجبار الخلايا الورمية على تكوين ميكرونويات، على أمل إثارة هجمات مناعية قوية أو دفع الخلايا غير المستقرة إلى ما بعد حدودها. ومع ذلك، فإن هذه الاستراتيجية تمشي على حبل دقيق، لأن نفس العمليات يمكن أن تولد نسخًا أكثر عدوانية ومقاومة للعلاج. يستنتج المؤلفون أن الميكروأنوية ليست ضارة محضة ولا مفيدة محضة. بل هي مؤشرات ووكلاء تغيير قويين يعتمد أثرهم الكلي على السياق. لتحويل الميكروأنوية بأمان إلى حلفاء ضد المرض، سيحتاج العلماء طرقًا أفضل لقياسها والتحكم فيها وتشكيل تكوّنها ومصيرها داخل الجسم بشكل انتقائي.
الاستشهاد: Duan, H., Peng, X., Qin, S. et al. Micronuclei: origins, assays, mechanisms, diseases and treatments. Sig Transduct Target Ther 11, 114 (2026). https://doi.org/10.1038/s41392-025-02538-8
الكلمات المفتاحية: الميكرونوى, عدم استقرار الجينوم, تحطم الكروموسومات (كروموثريبسيس), cGAS-STING, مؤشرات السرطان الحيوية