Clear Sky Science · ar
أنظمة العلاج الضوئي المعتمدة على الجسيمات النانوية: الآليات الجزيئية والتطبيقات السريرية
الضوء كأداة طبية لطيفة
يفكر معظمنا في الضوء كشيء يتيح لنا الرؤية أو يدفئ بشرتنا أو يغذي الألواح الشمسية. تستكشف هذه المقالة الاستعراضية دورًا أكثر مفاجأة: استخدام ضوء مضبوط بعناية، مع جزيئات مهندسة صغيرة، لتشخيص المرض ومعالجته من الداخل إلى الخارج. يصف المؤلفون كيف يمكن لـ «العلاج الضوئي المعتمد على الجسيمات النانوية» تركيز الضرر على خلايا السرطان، وتهدئة الالتهاب في القلب والمفاصل، وحتى مساعدة الدماغ على إزالة البروتينات السامة في حالات مثل مرض ألزهايمر، مع الحفاظ على معظم الأنسجة السليمة.
كيف تحول الجسيمات الصغيرة الضوء إلى دواء
في صميم هذا النهج توجد الجسيمات النانوية—هياكل أصغر آلاف المرات من عرض شعرة الإنسان—يمكنها حمل الأدوية، وامتصاص الضوء، وتحويل هذا الضوء إما إلى حرارة أو دفعات كيميائية قصيرة العمر. يهيمن استراتيجيان رئيسيان. في العلاج الديناميكي الضوئي، تُنتج الجزيئات المنشطة بالضوء على السطح أو داخل الجسيمات النانوية أنواعًا تفاعلية من الأكسجين—أشكال عالية الطاقة من الأكسجين تثقب مكونات الخلايا المجاورة. في العلاج بالحرارة الضوئية، تحوّل جسيمات أخرى، مثل الذهب أو الفسفور الأسود، ضوء الأشعة تحت الحمراء القريبة إلى حرارة، فتطهو الخلايا الورمية لفترة وجيزة من الداخل. وبما أن الضوء يمكن توجيهه ويمكن تصميم الجسيمات لتتراكم أساسًا في الأنسجة المريضة، يحصل الأطباء على مستوى من الدقة المكانية تفتقر إليه العلاجات الكيميائية والإشعاعية التقليدية. 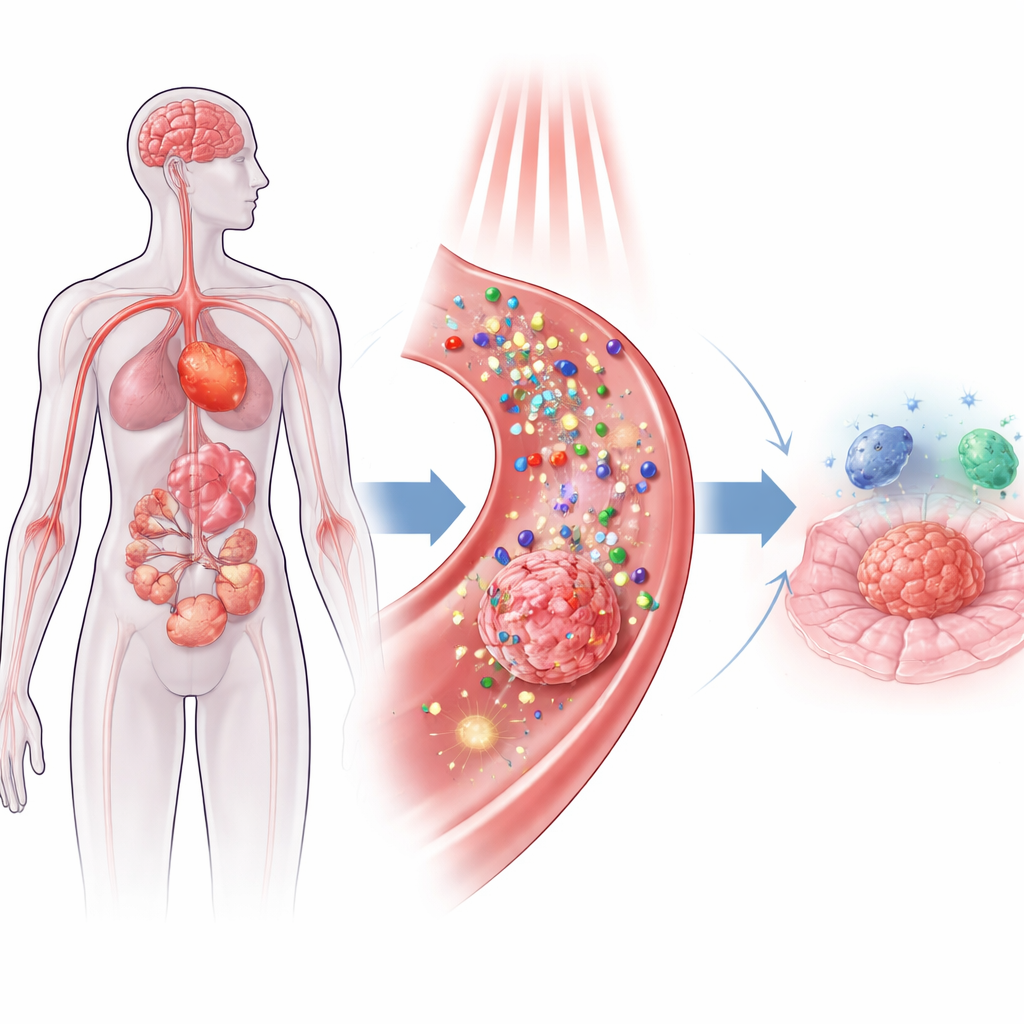
بناء ناقلات ومسارات توصيل أذكى
إن تسليط الضوء على الجسم وحده لا يكفي؛ التحدي هو إيصال الجسيمات المناسبة إلى المكان المناسب وإبقاؤها هناك وقتًا كافيًا لتؤدي عملها. يسجل الاستعراض صندوق أدوات من أنظمة التوصيل، بما في ذلك الحوامل اللينة مثل الليبوبسومات، وجسيمات الدهون الصلبة، والكرات أو الميسيلات القائمة على البوليمر، بالإضافة إلى الهياكل الصلبة المصنوعة من السيليكا أو المعادن أو الكربون أو الأطر المعدنية العضوية. يمكن تغليف أسطحها ببوليمرات مخفية لتمديد الدورة الدموية، أو بأغشية خلوية طبيعية للهروب من دفاعات المناعة، أو بـ «بطاقات عنوان» تتعرف على علامات على الخلايا السرطانية أو الملتهبة. بعض التصاميم «ذكية»: تظل خاملة في مجرى الدم لكنها تغير الحجم أو الشحنة أو الشكل استجابة للحموضة أو الإنزيمات أو ظروف التأكسد والاختزال داخل الورم، مطلقة محتوياتها فقط حيثما يلزم.
ما الذي يحدث داخل الخلايا عندما يصطدمها الضوء
بمجرد تشغيل الضوء، يتكشف تسلسل من الأحداث الجزيئية. يشرح المؤلفون كيف تولد الجسيمات المثارة ضوئيًا دفعات من المؤكسدات التي تهاجم الأغشية والحمض النووي والبنى الحيوية مثل الميتوكوندريا والليسوسومات. يمكن أن يدفع هذا الخلايا إلى الانتحاء المنظم (الاستماتة)، أو، عندما يكون الضرر شديدًا، إلى موت أكثر فوضوية. قد تضاعف الخلايا أيضًا عمليات البلعمة الذاتية (الاستقلاب الذاتي)، وهي نوع من إعادة التدوير الداخلي الذي يمكن أن يساعدها على النجاة من الإجهاد الخفيف أو يسرّع هلاکها عندما تُغمر. والأهم أن الخلايا الورمية المحتضرة يمكن أن تصدر إشارات «خطر» تعبئ الجهاز المناعي: التعرض لبعض البروتينات على سطحها، وإطلاق عوامل تجذب الخلايا المتغصنة، وإعادة تشكيل الخلايا المناعية المرتبطة بالورم من حالة مثبطة إلى حالة مقاتلة للورم. في الواقع، يمكن أن يعمل علاج ضوئي موضعي كنوع من لقاح السرطان المخصص. 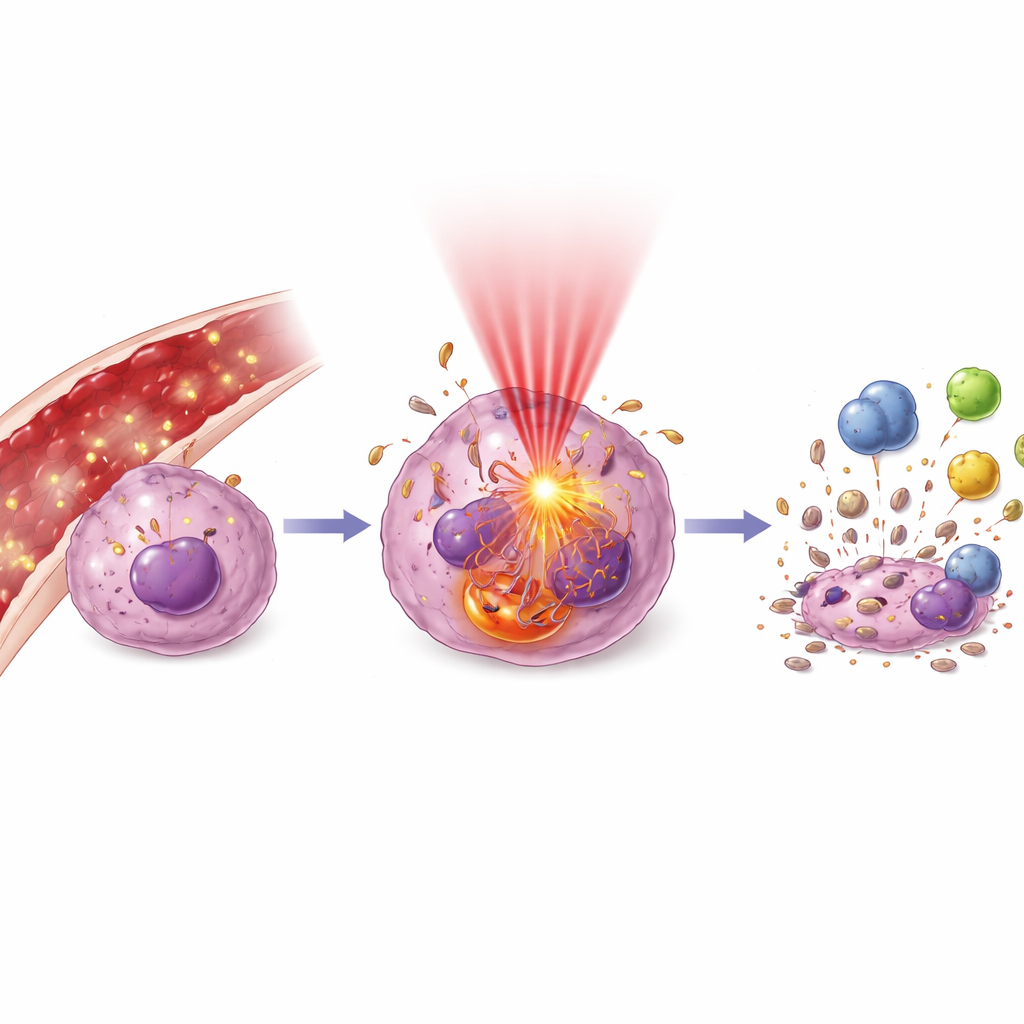
ما وراء السرطان: أهداف القلب والدماغ والأمراض المناعية الذاتية
بينما يمثل السرطان الساحة الأكثر تقدمًا، يجري تكييف نفس المبادئ لحالات مزمنة. في أمراض القلب والأوعية الدموية، تهدف المقاربات المعتمدة على الضوء ليس إلى قتل الخلايا بل إلى تقليل الإجهاد التأكسدي، واستقرار خلايا بطانة الأوعية، وحتى المساعدة في تقليص أو تحمّس اللويحات الخطرة. في الدماغ، حيث تكون الخلايا العصبية حساسة جدًا، تسعى بروتوكولات ضوئية ألطف—غالبًا ما تسمى التحفيز الضوئي الحيوي— إلى تعزيز إنتاج الطاقة الميتوكوندرية، وتقليل تكتلات البروتين السامة، وتخفيف الالتهاب الذي تقوده الخلايا النجمية والميكروغليا. يبرز الاستعراض أيضًا أعمالًا مبكرة في الأمراض الاستقلابية والمناعية الذاتية، حيث يمكن للضوء والجسيمات النانوية الموزونة بعناية دفع الخلايا المناعية بعيدًا عن سلوك هجومي مدمر للأنسجة ونحو أدوار تنظيمية ومهدئة، مع تحسين طفيف في حساسية الإنسولين وإشارات نسيج الدهون.
من المختبر إلى العيادة: الوعود والعقبات
على الرغم من عقود من البحث، فإن عددًا قليلاً فقط من الأدوية المنشطة بالضوء معتمد بالكامل، ومعظمها لأمراض العين وبعض الأورام. يجادل المؤلفون بأن النانو تكنولوجيا بدأت تفتح الموجة التالية، مما يمكّن اختراق ضوء أعمق، واستهدافًا أفضل، وتصويرًا مدمجًا لمراقبة العلاج في الوقت الحقيقي. ومع ذلك تبقى عقبات رئيسية: توسيع إنتاج الجسيمات النانوية بجودة متسقة، وإثبات السلامة طويلة الأمد والتخلص منها من الجسم، وتسليم الضوء بفعالية إلى الأعضاء العميقة، والامتثال لمتطلبات تنظيمية صارمة. يختم الاستعراض بأن توحيد علم المواد والبصريات والبيولوجيا وتصميم موجه بالذكاء الاصطناعي يهيئ العلاج الضوئي المعتمد على الجسيمات النانوية للتطور من إجراءات متخصصة إلى ركيزة غير جراحية أوسع في الطب الدقيق.
الاستشهاد: Chauhan, D.S., Prasad, R., Dhanka, M. et al. Nanoparticles-based phototherapy systems: molecular mechanisms and clinical applications. Sig Transduct Target Ther 11, 95 (2026). https://doi.org/10.1038/s41392-025-02536-w
الكلمات المفتاحية: العلاج الضوئي بالجسيمات النانوية, العلاج بالحرارة الضوئية, العلاج الديناميكي الضوئي, طب السرطان النانوي, التحفيز الضوئي الحيوي