Clear Sky Science · ar
تثبيط IFFO1 لسرطان الثدي عن طريق تنسيق انقسام الميتوكوندريا وتخليق الأحماض الدهنية عبر محور LaminA/C-PGC1α
لماذا يهم هذا البحث
يبقى سرطان الثدي أحد الأسباب الرئيسية لوفيات السرطان لدى النساء، ويرجع ذلك إلى حد كبير إلى أن بعض الأورام تستمر في النمو والانتشار وتتهرب من العلاجات الحالية. يكشف هذا البحث عن «مكبح» خلوي لم يحظَ بالاهتمام الكافي يُدعى IFFO1 يبطئ سرطان الثدي عن طريق ترويض محركين أساسيين لنمو الورم: مصانع الطاقة الخلوية، أي الميتوكوندريا، وقدرة الخلايا على صنع وتخزين الدهون. فهم هذا المكبح يفتح زاوية جديدة للعلاجات التي قد تكون فعالة عبر أنواع متعددة من سرطان الثدي.
حارس مخفي داخل خلايا الثدي
بدأ الباحثون بفحص عينات من 30 امرأة مصابة بسرطان الثدي، بالإضافة إلى قواعد بيانات سرطانية عامة واسعة. وجدوا أن مستويات بروتين IFFO1 كانت أقل باستمرار في الأنسجة الورمية مقارنة بالأنسجة الطبيعية المجاورة. كلما زادت مرحلة السرطان تقدماً، انخفضت مستويات IFFO1، والمرضى الذين كانت أورامهم تحتوي على مستويات أعلى من IFFO1 أمضوا فترات أطول من الحياة. في خلايا سرطان الثدي المُزرعة في المختبر، أدى إجبار الخلايا على إنتاج كميات إضافية من IFFO1 إلى تقليل حاد في قدرتها على النمو والانقسام والهجرة — سلوكيات لازمة لتوسع الورم وانتشاره. كما قلل IFFO1 من برنامج خلوي يعرف بالتحول الطلائي-اللحائي (epithelial–mesenchymal transition) الذي يساعد الخلايا السرطانية على الانفصال والغزو إلى أنسجة أخرى.
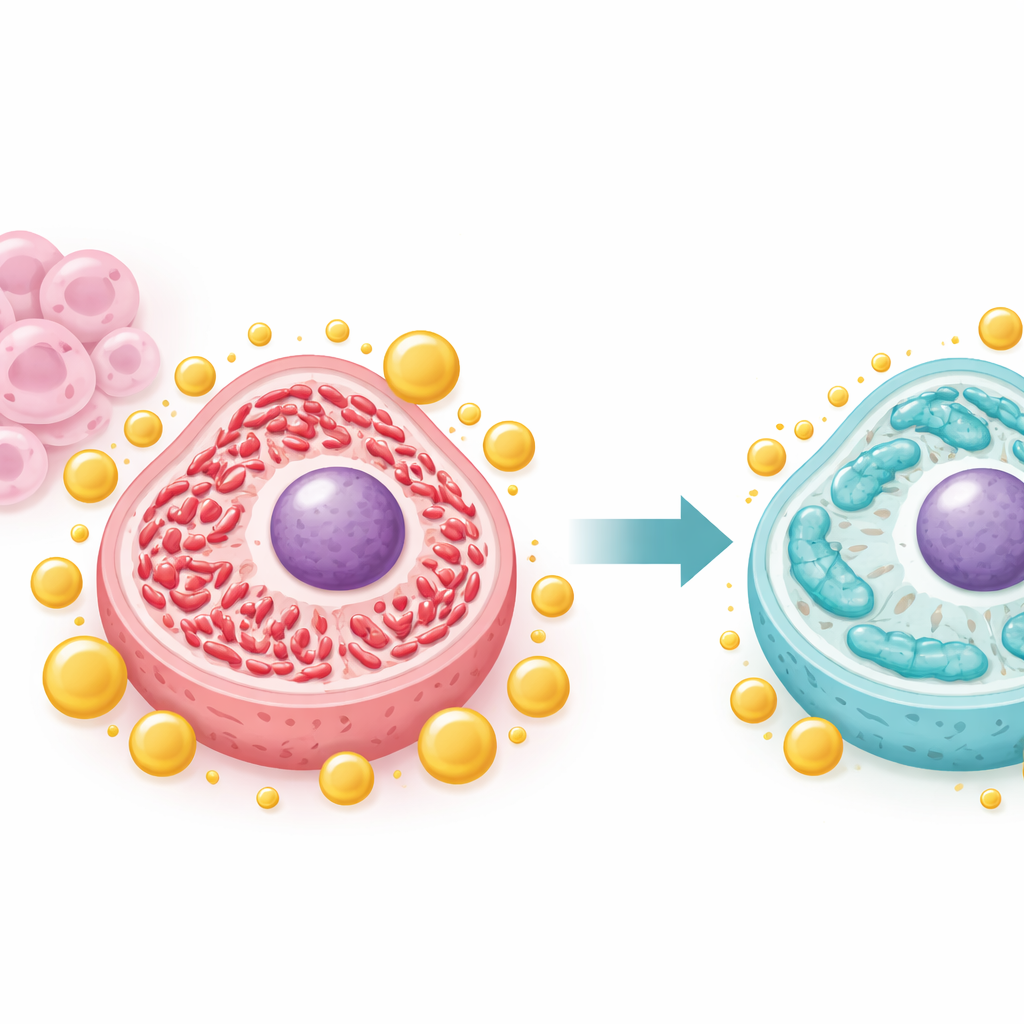
تهدئة مصانع الطاقة المفرطة النشاط
غالباً ما تعيد الخلايا السرطانية تشكيل ميتوكوندرياتها، تلك المحطات الصغيرة للطاقة داخل الخلايا، لتغذية النمو السريع. أظهر الفريق أن IFFO1 يحوّل هذا التوازن بعيداً عن الحالة المفصّمة للغاية المعروفة بالـ «انقسام» (fission) نحو حالة أكثر استطالة تعرف بالـ «اندماج» (fusion) المرتبطة عموماً بميتوكوندريا أكثر صحة واستقراراً. عندما كان IFFO1 وافراً، انخفضت بروتينات الانقسام الرئيسية مثل Drp1 وFis1، بينما ارتفعت بروتينات الاندماج. كشفت الميكروسكوب أن الميتوكوندريا أصبحت أطول وأقل تجزؤاً، كما انخفضت مقاييس الحمض النووي الميتوكوندري ومخرجات الطاقة من المستويات العالية غير الطبيعية التي تُرى في الخلايا العدوانية. تشير هذه التغيرات إلى أن IFFO1 يمنع الميتوكوندريا من الدخول في تكوين مفرط النشاط يدعم نمو الورم غير المنضبط.
قطع خط إمداد الدهون
الأورام سريعة النمو لا تحتاج فقط إلى الطاقة؛ بل تحتاج أيضاً إلى إمداد ثابت بالدهون لبناء أغشية جديدة وجزيئات إشارات. وجدت الدراسة أن IFFO1 يضغط أيضاً على هذا المسرع الأيضي. في الخلايا التي تحتوي على IFFO1 إضافي، انخفضت بروتينات بناء الدهون الأساسية — بما في ذلك FASN وSREBP‑1 وSCD1 وغيرهم. أكدت الاختبارات الإنزيمية انخفاض نشاط تخليق الدهون، وأظهرت التحاليل الكيميائية انخفاضاً في الأحماض الدهنية الحرة والدهون الثلاثية والكوليسترول. صبغات التصوير التي تبرز مخزون الدهون أظهرت قطرات دهنية أقل ودهوناً محايدة إجمالاً داخل الخلايا السرطانية. وبالعكس، فإن رفع مستوى بروتين الانقسام Drp1 أدى إلى التأثير المعاكس، مع زيادة إنتاج الدهون، بينما أدى إسكات Drp1 إلى كبحها — مما يدعم وجود رابط مباشر بين شكل الميتوكوندريا وإمداد الدهون في السرطان.
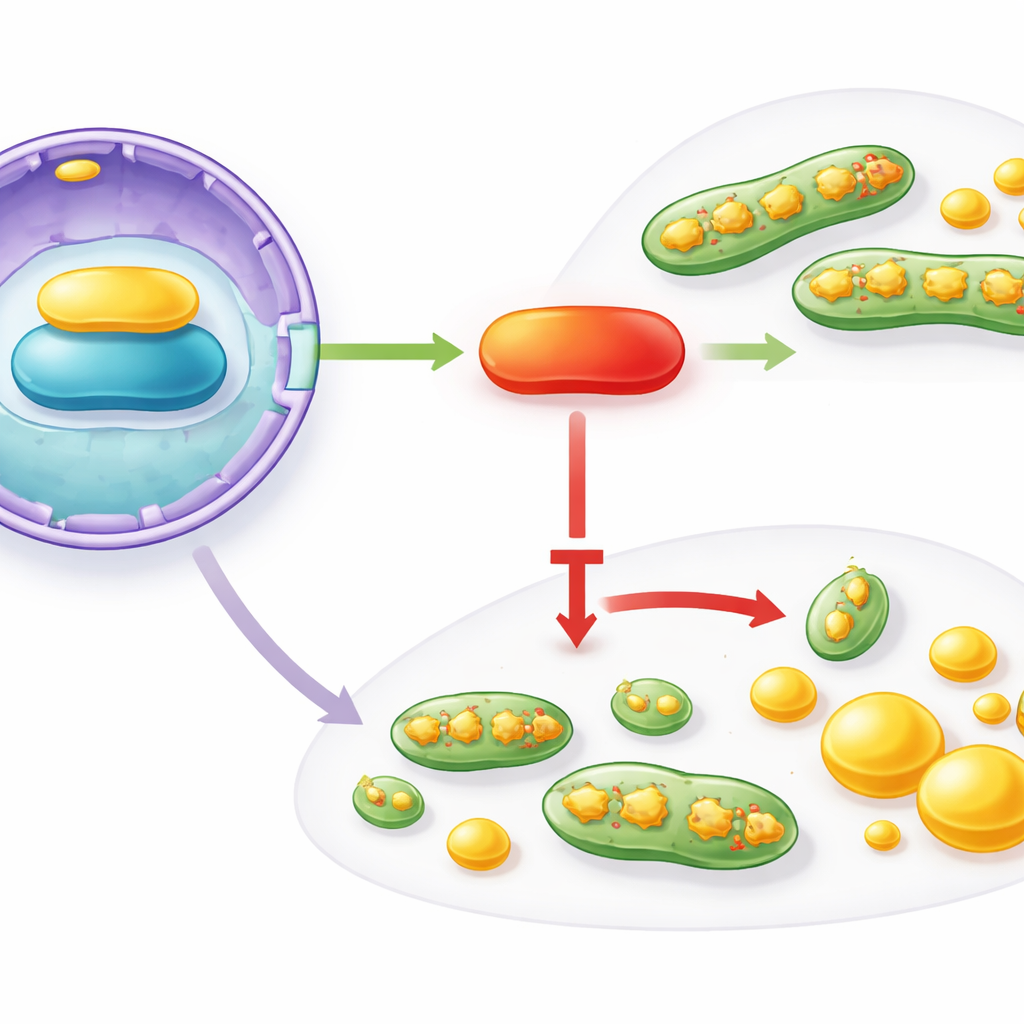
سلسلة إشارات من النواة إلى الميتوكوندريا
كيف يؤطر IFFO1 هذه التغيرات الواسعة؟ تتبع المؤلفون سلسلة من التفاعلات التي تبدأ في نواة الخلية وتنتهي عند الميتوكوندريا وآلية صنع الدهون. يرتبط IFFO1 بشكل فيزيائي ببروتين هيكلي لغلاف النواة يُدعى Lamin A/C، ويزيد من مستوياته. يدعم Lamin A/C بدوره نشاط PGC1α، المنظم الرئيسي الذي يشرف على صحة الميتوكوندريا والأيض. في أنسجة وخلايا سرطان الثدي، وُجد أن كل من Lamin A/C وPGC1α منخفضان، مما يعكس فقدان IFFO1. عندما عزز العلماء IFFO1 اصطناعياً، ارتفعت مستويات Lamin A/C وPGC1α، انخفض انقسام الميتوكوندريا، وتراجع تخليق الدهون. إنقاص مستوى Lamin A/C أزال هذه الفوائد، لكن استعادة PGC1α أعادها، مشيراً إلى محور وظيفي IFFO1 → Lamin A/C → PGC1α يقيّد التغيرات المروجة للورم في الميتوكوندريا والدهون.
اختبار المكبح في حيوانات حية
ليرى الفريق ما إذا كانت هذه التأثيرات الخلوية تمتد إلى أورام حقيقية، غرسوا خلايا سرطان ثدي بشرية معها أو بدون IFFO1 إضافي في فئران. نمت الأورام التي تحتوي على IFFO1 معزز بشكل أبطأ، ووزنت أقل عند نقطة النهاية التجريبية، وأظهرت دلائل أقل على تراكم الدهون. في نموذج منفصل حيث حقن الباحثون الخلايا السرطانية في مجرى الدم لبذر نقائل رئوية، شكلت الخلايا المفرطة الإنتاج لـ IFFO1 عدد عقد ورمية رئوية أقل بكثير. كررت تحليلات الأنسجة من هذه الفئران نتائج مزرعة الخلايا: ارتفاع Lamin A/C وPGC1α، تقليل انقسام الميتوكوندريا، وانخفاض تخليق الدهون.
ماذا يعني هذا لعلاجات المستقبل
مجتمعة، تقدم هذه الدراسة IFFO1 كباحث متعدد الطبقات يربط الهيكل الخلوي ومصانع الطاقة وآلية صنع الدهون. من خلال استقرار Lamin A/C وتعزيز PGC1α، يمنع IFFO1 الميتوكوندريا من التجزؤ المفرط ويقطع فرط إنتاج الدهون التي تعتمد عليها الخلايا السرطانية. للقراء غير المتخصصين، الرسالة الأساسية هي أن هذا البروتين يعمل كمكبح داخلي على كل من الطاقة والمواد البِنيوية التي تغذي نمو وانتشار سرطان الثدي. قد توفر الأدوية التي ترفع مستويات IFFO1 أو تحاكي تأثيراته على محور Lamin A/C–PGC1α خيارات علاجية جديدة يوماً ما، لا سيما للأشكال العدوانية أو المقاومة للعلاجات من سرطان الثدي.
الاستشهاد: Cai, H., He, J. IFFO1 inhibits breast cancer by coordinating mitochondrial fission and fatty acid synthesis via the LaminA/C-PGC1α axis. Oncogenesis 15, 16 (2026). https://doi.org/10.1038/s41389-026-00609-1
الكلمات المفتاحية: سرطان الثدي, ديناميكية الميتوكوندريا, تخليق الأحماض الدهنية, أيض الورم, مسار PGC1α