Clear Sky Science · ar
التحكم الأورمِي في تخليق النوكليوتيدات
لماذا تهم الخلايا السرطانية وحدات البناء
غالباً ما يُوصَف السرطان بأنه خلايا لا تتوقف عن الانقسام. لكن لنسخ نفسها، تحتاج هذه الخلايا إلى إمداد دائم بوحدات بناء صغيرة تسمى النوكليوتيدات، التي تشكل الحمض النووي والحمض النووي الريبي وتساعد أيضاً في تشغيل العديد من العمليات الخلوية. تشرح هذه المراجعة كيف تعيد الجينات المسببة للسرطان توصيل الكيمياء الخلوية للحفاظ على إنتاج النوكليوتيدات مرتفعاً، وكيف تتحول الأورام بين طرق مختلفة للحصول على هذه الجزيئات، وكيف يمكن للأطباء استغلال هذه الحيل باستخدام أدوية قديمة وحديثة.
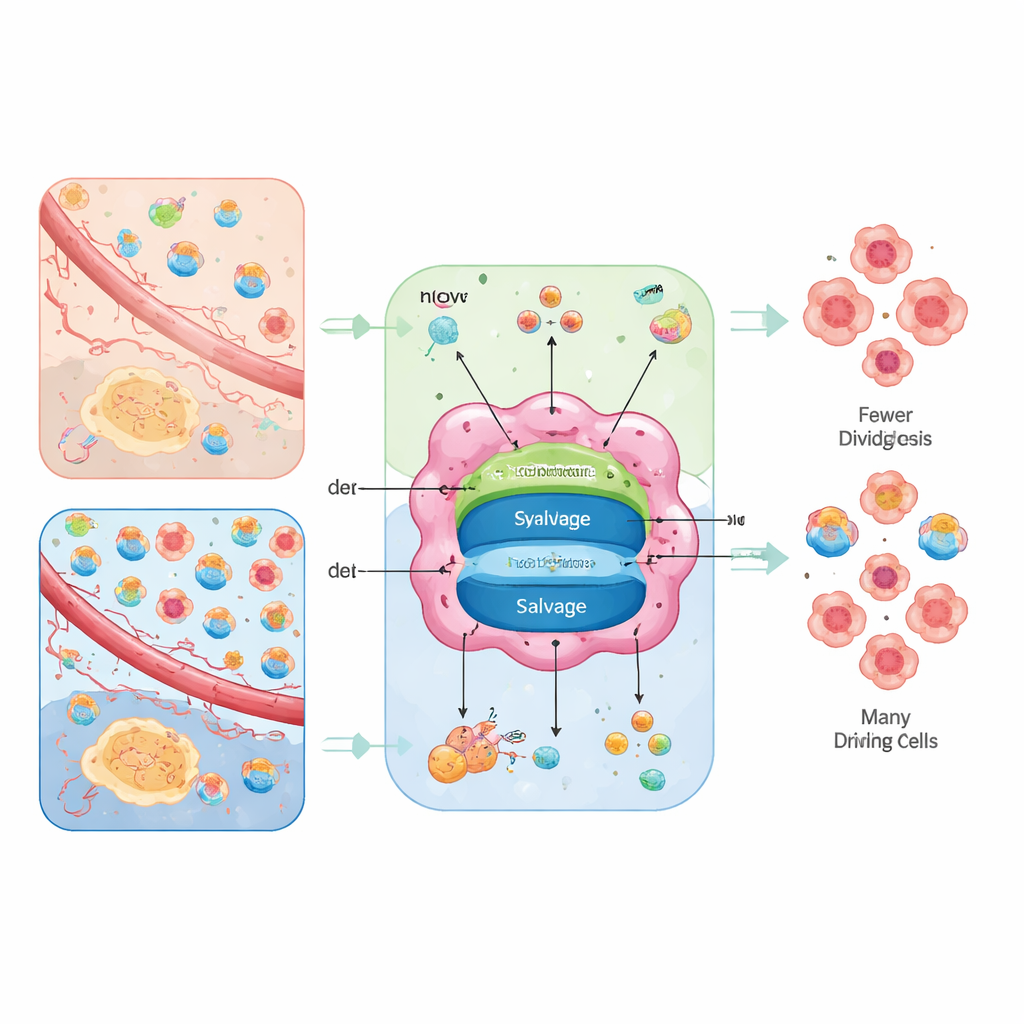
طريقتان للوصول إلى نفس وحدات البناء
يمكن للخلايا أن تصنع النوكليوتيدات من الصفر أو أن تعيد تدويرها. الطريق «من الصفر»، المسمى التخليق الجديد (de novo)، يجمع الحلقات من مغذيات أساسية مثل الجلوكوز والأحماض الأمينية وثاني أكسيد الكربون والبيكربونات، باستخدام تفاعلات متعددة المراحل تستهلك كثيراً من الطاقة. أما طريق الاسترجاع (salvage)، فيأخذ القواعد والنوكليوسيدات المتحللة من الخارج أو من نفايات الخلية ويُعيد تركيبها إلى نوكليوتيدات قابلة للاستخدام بتكلفة طاقة أقل بكثير. تستخدم الأورام كلا الخيارين، لكن التوازن بينهما يعتمد على مصدر الطاقة داخلها وما توفره الأنسجة المحيطة.
كيف يوجه بيئة الورم الاختيار
يؤطر المؤلفون إمداد النوكليوتيدات كمشكلة «توجيه يتشكّل بفعل البيئة». في مناطق محرومة من التغذية حيث تكون الأحماض الأمينية متاحة لكن النوكليوسيدات الحرة نادرة، تميل الخلايا السرطانية إلى الاعتماد بكثافة على مسارات التخليق الجديد وتصبح عرضة للأدوية التي تحجب هذه الخطوات. في المناطق ذات التروية الأفضل، حيث ينقل الدم نوكليوسيدات وفيرة أو حيث تكون الميتوكوندريا ضعيفة، يمكن للأورام الاعتماد أكثر على الاسترجاع، فتصبح حساسة بدلاً من ذلك إلى مثبطات الناقلات التي تمنع امتصاص النوكليوسيدات. عندما تكون كلا الخيارات متاحة، تظهر الأورام مرونة استقلابية وتنجو من أدوية أحادية؛ وعندما تُغلق كلاهما، تتوقف الخلايا عن تكرار الحمض النووي، وتتراكم الأضرار، وقد تموت أو تتحول إلى حالات أكثر نضجاً وأقل عدائية.
خطوط دعم مخفية تغذي إمداد النوكليوتيدات
يتطلب إبقاء مصانع النوكليوتيدات عاملة عدة دوائر مساعدة. يوفر طريق البنتوز فوسفات العمود السكرّي والطاقة المخفضة؛ يوفر الغلوتامين ودورة الطاقة في الميتوكوندريا النيتروجين والأسبارتات؛ تساهم كيمياء السيرين والجليسين والفولات بوحدات الكربون المفردة التي تُكمل الحلقات؛ وتدخل البيكربونات كربونات أساسية. ترفع محركات السرطان مثل PI3K–AKT–mTORC1 وRAS–MAPK وMYC هذه المسارات معاً، وتعزز إنزيمات رئيسية، وتكوّن حتى عُقَد إنزيمية متعددة تُوجّه الوسائط غير المستقرة بكفاءة. بالمقابل، تعمل مجسات الإجهاد مثل LKB1–AMPK وp53 عادةً كفرامل، فتقلّل إنتاج النوكليوتيدات عندما تُهدَّد الطاقة أو سلامة الحمض النووي — فرامل تعطلها العديد من الأورام.
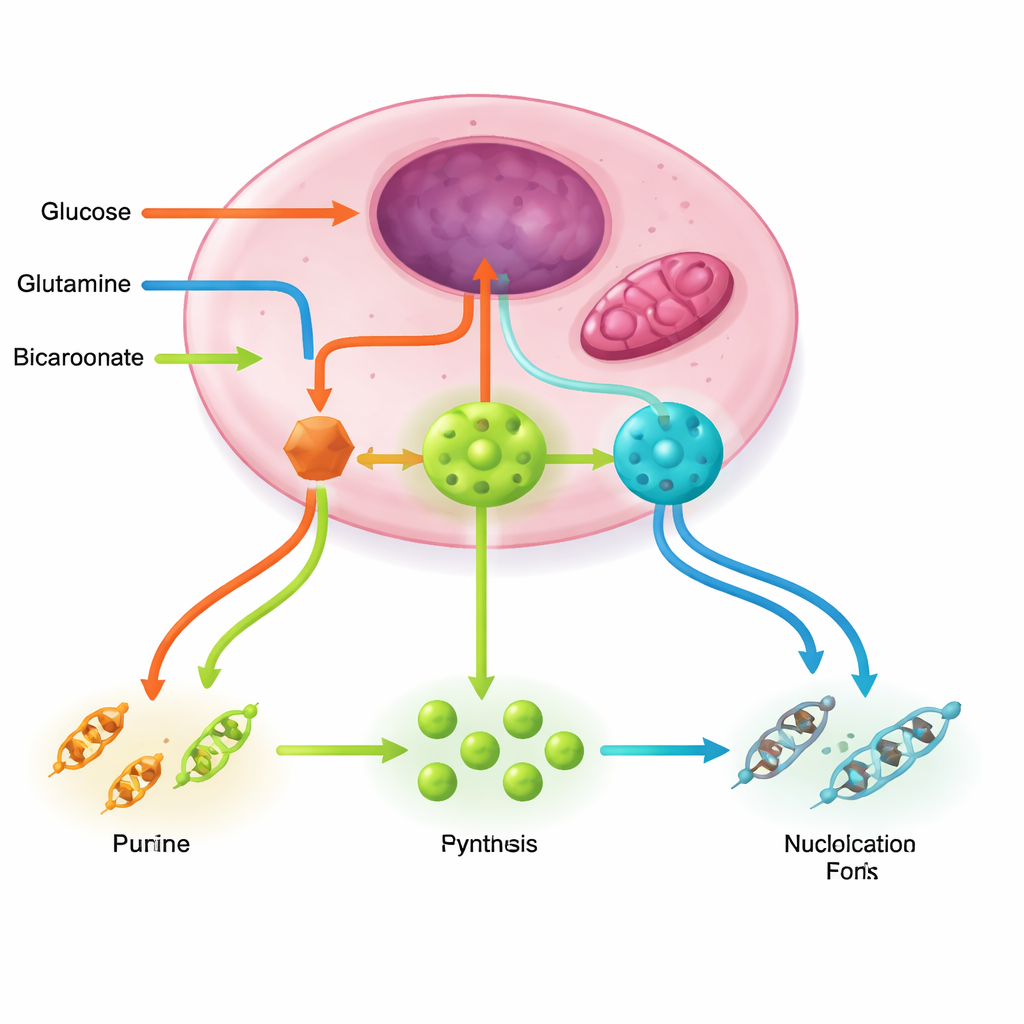
العلاج الكيماوي القديم، منطق استقلابي جديد
بسبب اعتماد الخلايا سريعة النمو بقوة على النوكليوتيدات، استهدفت بعض أقدم علاجات السرطان هذا الضعف. تحجب أدوية كلاسيكية مثل الميثوتريكسيت و5‑فلورويوراسيل والسيطارابين والجمسيتابين ومختلف نظائر البيورين استخدام الفولات أو تثبط إنزيمات محددة أو تتنكر كوحدات بناء معيبة تسمم الحمض النووي والحمض النووي الريبي. تعيد المراجعة النظر في هذه الأدوية من منظور نموذج التوجيه، موضحة لماذا تكون الآثار الجانبية والمقاومة شائعة: فالأنسجة غير السرطانية أيضاً بحاجة إلى النوكليوتيدات، وغالباً ما تستطيع الأورام إعادة توجيه التدفق عبر الاسترجاع أو مسارات موازية عندما يُحاصر أحد العقد.
استراتيجيات الجيل التالي وأسئلة مفتوحة
تهدف النهج الأحدث إلى أن تكون أكثر انتقائية بضرب أجزاء الشبكة التي تميل أكثر إلى السرطان. تُطوّر عقاقير تجريبية ضد إنزيمات أحادية الكربون الميتوكوندرية مثل MTHFD2، وإنزيمات البريديميدين مثل DHODH، وإنزيمات البيورين مثل IMPDH وPAICS، غالباً في مجموعات تحجب أيضاً ناقلات الاسترجاع. يقترح المؤلفون علامات عملية — مثل مستويات الناقلات، وكثافة الأوعية الدموية، وكفاءة الميتوكوندريا، والتعبير عن إنزيمات استقلابية محددة — لتحديد أي الأورام تعتمد أكثر على التخليق الجديد أو الاسترجاع ومطابقة المرضى بعلاجات تستهدف المسار المناسب. على المدى البعيد، يبرزون أسئلة رئيسية، منها كيف تتغير هذه المسارات عبر المكان والزمان داخل الأورام الحقيقية، وكيف تشكّل الخلايا المناعية والخلايا الدعامة المحيطة توافر النوكليوتيدات، وكيف نصمم جداول دوائية محتملة التحمل تستغل إجهاد النسخ بدون أن تطغى على الأنسجة السليمة. مجتمعة، يرى هذا العمل أن فهم واستهداف استقلاب النوكليوتيدات قد يحول مطلباً أساسياً للانقسام الخلوي إلى رافعة شخصية قوية ضد السرطان.
الاستشهاد: Vidal-Cruchez, O., Ben-Sahra, I. The oncogenic control of nucleotide synthesis. Oncogenesis 15, 17 (2026). https://doi.org/10.1038/s41389-026-00608-2
الكلمات المفتاحية: استقلاب النوكليوتيدات, استقلاب السرطان, التخليق الجديد من الصفر, مسارات الاسترجاع, علاجات استقلابية