Clear Sky Science · ar
التحليل النسخي للخلايا السرطانية والمضيفة في التعايش يكشف أن نقص الأكسجة يدفع تأثير الخلايا العضلية الهيكلية المضاد للتكاثر على الخلايا السرطانية
لماذا تقاوم بعض الأنسجة انتشار السرطان
يصبح السرطان في العادة مميتًا عندما تهرب الخلايا الورمية من موقعها الأصلي وتستقر في أعضاء بعيدة. من الغريب أن بعض الأنسجة، مثل الرئتين، تعد مواقع شائعة للاستقرار، بينما نادرًا ما تستعمر أنسجة أخرى، كالعضلات الهيكلية، رغم أنها تمثل جزءًا كبيرًا من وزن الجسم. تطرح هذه الدراسة سؤالًا بسيطًا لكن مهمًا للمرضى والأطباء على حد سواء: ما الذي يجعل العضلات تربة سيئة لنمو الخلايا السرطانية، وهل يمكن أن يعيد فهم هذا الدفاع الطبيعي تشكيل طرق تعاملنا مع الانتشار السرطاني؟
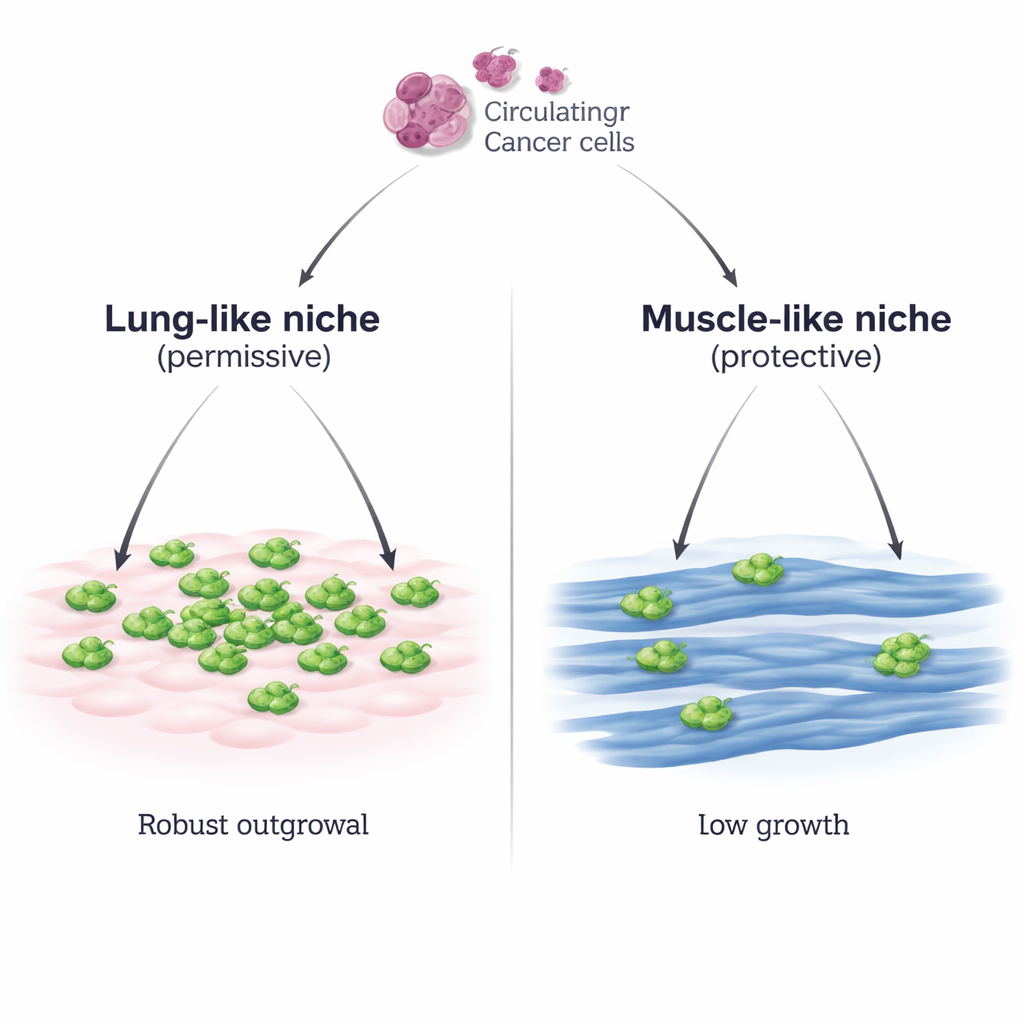
حارتان للخلايا الورمية المسافرة
أنشأ الباحثون نظامًا مخبريًا محكومًا يحاكي حيّين مختلفين قد تواجههما خلية سرطان الثدي: بيئة شبيهة بالرئة مكوّنة من خلايا النسيج الضام الرئوي (MLg)، وبيئة شبيهة بالعضل مكوّنة من ألياف عضلية هيكلية ناضجة (C2C12 myotubes). وضعوا خلايا سرطان الثدي الفأرية فوق كل طبقة ورصدوا ما يحدث. على خلايا النسيج الشبيهة بالرئة، ارتبطت الخلايا السرطانية جيدًا ثم تكاثرت بسرعة، مكونة رقعًا كثيفة. على خلايا العضلات، ارتبطت بنفس الفاعلية، لكن نموها بقي متناثرًا وبطيئًا، حتى عند زيادة عدد الخلايا المبدئي بشكل كبير أو عند استخدام سطر ورمي ثانٍ. أظهر سطر عضلي هيكلي منفصل (Sol8) نفس القدرة على كبح نمو السرطان، مما يؤكد أن هذه خاصية عامة لخلايا العضلات وليس سمة خاصة بنوع خلوي واحد.
كيف تعيد الخلايا السرطانية والمضيفة برمجة نشاطها
لفهم ما يجري داخل الخلايا، عزّل الفريق الخلايا السرطانية والمضيفة من تلك الثقافات المختلطة وسلسلوا الحمض النووي الريبوزي لديها، وهو قراءة عن الجينات المشغلة أو المكبوتة. الخلايا السرطانية الجاثمة على ألياف العضلات أظهرت تغييرات جينية أوسع بكثير من تلك التي تنمو على خلايا الرئة، مما يوحي بأن بيئة العضلات تجبرها على التكيف بقوة. في بيئة العضلات، شغّلت الخلايا السرطانية برامج مرتبطة بصفات شبيهة بالعضل، بمعالجة الطاقة، ومفاجئًا، استجابات نقص الأكسجة. في الوقت نفسه، تم خفض البرامج الجينية الاعتيادية التي تدفع الانقسام السريع. بالمقابل، احتفظت الخلايا السرطانية على خلايا الرئة بمخطط يركّز على النمو واحتاجت إلى إعادة برمجة أقل بكثير، وهو ما يتماشى مع فكرة أن الحي الشبيه بالرئة مسموح ويسهل على الخلايا الورمية الاستفادة منه.
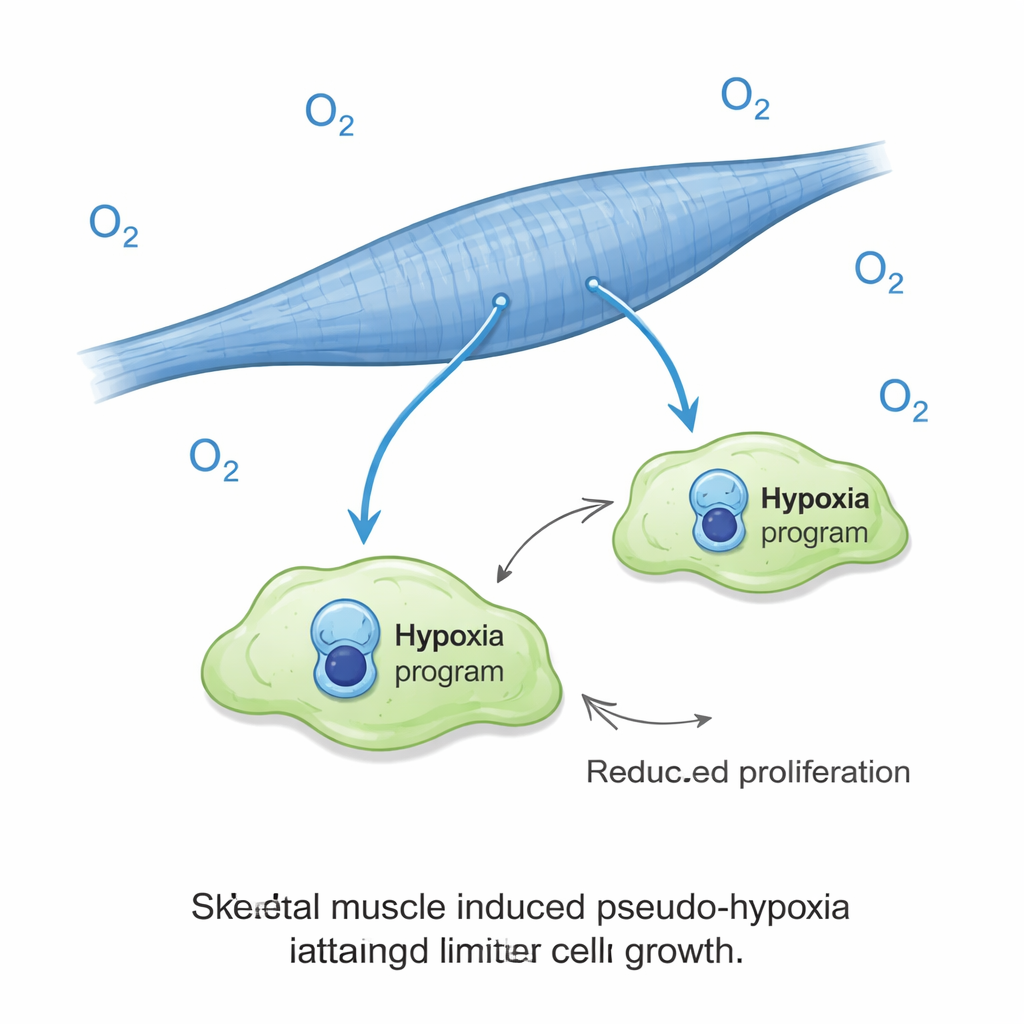
دور مفاجئ لإشارات نقص الأكسجة
كانت إحدى النتائج اللافتة أن الخلايا السرطانية على ألياف العضلات شغّلت بصمة جينية شبيهة بنقص الأكسجة رغم نموها تحت مستويات أكسجين طبيعية. في معظم الأورام، يرتبط نقص الأكسجة بمؤشرات سيئة، عادةً مع سلوك عدواني ونتائج سيئة. هنا، كان مرتبطًا بالعكس: نمو ضعيف. ثم عرض العلماء الثقافات لأكسجين منخفض فعليًا فوجدوا أن ذلك قضى تقريبًا على توسع الخلايا السرطانية على العضلات، بينما عزّز فعليًا نمو السرطان في ثقافات الشبيهة بالرئة. بمعنى آخر، نفس الإشارة التي عادةً ما تساعد الأورام على الازدهار أصبحت فرملة عندما كانت الخلايا الورمية في بيئة عضلية. لا يبدو أن هذا التأثير الأوكسيجيني يفسر بتغيرات بسيطة في اللاكتات أو الحموضة أو توفر السكر في وسط الزراعة.
أكثر من مجرد عوامل سائلة مفصوحة
اختبر الفريق أيضًا ما إذا كانت مواد ذائبة بسيطة تفرزها الخلايا العضلية يمكن أن تشرح تأثيرها الحامي. إضافة لاكتات إضافي، تعديل الحموضة، تغيير مستويات الجلوكوز، أو زراعة الخلايا السرطانية في وسط سبق وأن حمّته خلايا العضلات لم يعيد قمع النمو القوي الذي شوهد في التعايش بالاتصال المباشر. هذا يشير إلى أن الاتصال الجسدي الوثيق، أو إشارات قصيرة المدى جدًا عند سطح الخلية، هي المفتاح في كيفية دفع خلايا العضلات للخلايا السرطانية نحو حالة نمو منخفضة، وربما سبات. من المثير أن خلايا العضلات نفسها ظلت مستقرة نسبيًا في نشاطها الجيني عند مواجهتها للسرطان، بينما أعيد برمجة خلايا الرئة بسهولة أكبر، مما يبرز العضلات كنسيج متين "مقاوم للانبثاث".
ماذا يعني هذا للمرضى والعلاجات
بشكل عام، تكشف الدراسة أن العضلات الهيكلية تعمل كبيئة معادية تجبر الخلايا السرطانية على التبني لحالة شبيهة بنقص الأكسجة ومنخفضة التكاثر، حتى عندما يتوفر الكثير من الأكسجين. يساعد هذا في توضيح سبب ندرة حدوث الانبثاث في العضلات. كما يقدّم رسالة تحذيرية لتطوير الأدوية: قد تضعف العلاجات المصممة لِحجب إشارات نقص الأكسجة في أنحاء الجسم هذا الدفاع العضلي الطبيعي بطريق الخطأ، مما يسهل نمو الخلايا السرطانية في أماكن كانت نادرًا ما تنمو فيها. قد يفتح فهم والحفاظ على، أو حتى محاكاة، السمات الوقائية لأنسجة العضلات سبلًا جديدة لمنع أو السيطرة على المرض المستشري.
الاستشهاد: Aunan, A., Claeyssen, C., Abdelhalim, M. et al. Transcriptomic profiling of co-cultured cancer-host cells identifies hypoxia as a driver of the skeletal muscle cell’s anti-proliferative effect on cancer cells. Oncogenesis 15, 7 (2026). https://doi.org/10.1038/s41389-026-00601-9
الكلمات المفتاحية: انبثاث السرطان, العضلات الهيكلية, نقص الأكسجة, البيئة الدقيقة للورم, سبات السرطان