Clear Sky Science · ar
امتصاص الأحماض الدهنية المتوسط بواسطة FABP4 يعزز تكون شيخوخة الخلايا التائية CD8+ عبر تأكسد الدهون في البيئة الدقيقة الغنية بالخلايا الدهنية لسرطان المبيض
لماذا تهم الخلايا الدهنية والمناعية في سرطان المبيض
غالبًا ما ينتشر سرطان المبيض إلى التجويف البطني، حيث يواجه رواسب كبيرة من الدهون الجسدية. هذه البيئة الدهنية ليست مجرد خلفية سلبية—بل تشكل فعليًا سلوك الخلايا المناعية. على وجه الخصوص، يمكن أن تُضعف خلايا T القاتلة CD8 التي من المفترض أن تهاجم الأورام. تستكشف هذه الدراسة كيف تدفع المواد المشتقة من الدهون هذه الخلايا التائية إلى حالة متقدمة من التلف والشيخوخة، وكيف أن حجب بروتين ناقل رئيسي للدهون قد يساعد في استعادة قدرتها على محاربة السرطان.
بيئة غنية بالدهون تُشيخ مدافعي المناعة
لاحظ الأطباء منذ زمن أن العديد من النساء المصابات بسرطان المبيض المتقدم يتجمع لديهن سائل في البطن وتتموضع الأورام في أنسجة غنية بالدهون تُسمى الشحيمة (omentum). من خلال تحليل بيانات RNA أحادية الخلية من المرضى وفحص عينات الأورام تحت المجهر، وجد الباحثون أن خلايا CD8 التائية القريبة من هذه الرواسب الدهنية كانت أكثر ميلاً لإظهار سمات الشيخوخة الخلوية أو الهرم. هذه الخلايا التائية «المُشيخة» تتراكم فيها أصباغ نفاياتية، تتوقف عن الانقسام، وتنتج إشارات التهابية بدلًا من قتل الخلايا السرطانية. في كل من العينات البشرية ونماذج الفئران، كانت خلايا CD8 المستخرجة من مناطق الأورام الغنية بالدهون والسائل أكثر عرضة للشيخوخة مقارنة بتلك المأخوذة من العقد اللمفاوية أو الطحال، مما يربط البيئة الدقيقة الغنية بالخلايا الدهنية مباشرةً بنداء شيخوخة الخلايا التائية.
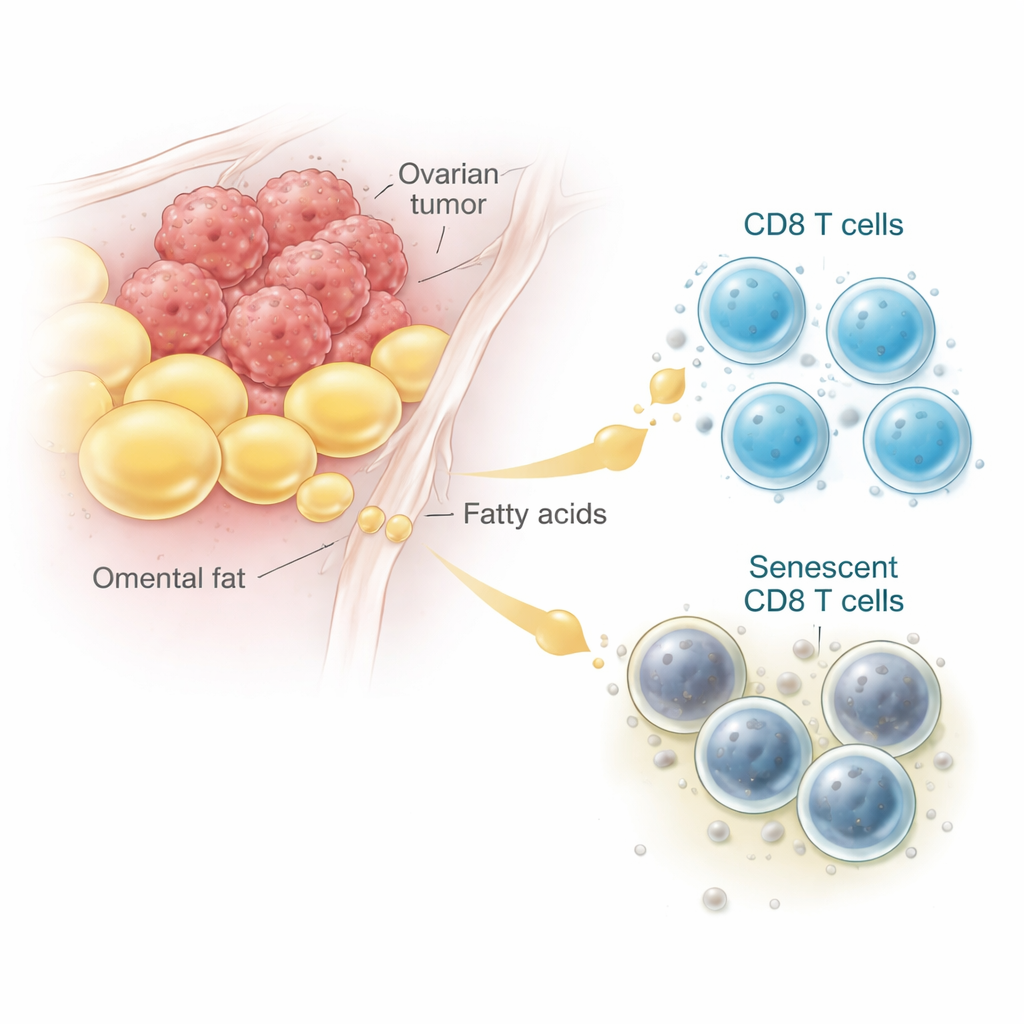
كيف يحول حمض دهني شائع الوقود المفيد إلى ضرر
لفهم تأثير الدهون على الخلايا التائية، أعاد الفريق إنشاء بيئة الورم في المختبر. نما باحثوها خلايا سرطان المبيض مع خلايا CD8 التائية للفأر، ثم أضافوا إما مستخلصات من نسيج دهني أو حمضًا دهنيًا محددًا يسمى حمض الأوليك، وهو متوافر بكثرة في سائل سرطان المبيض. بجرعات متوسطة إلى عالية، جعل حمض الأوليك عددًا أكبر من خلايا CD8 يصبح مُشيخًا—ولكن فقط عند وجود خلايا الورم. بدلًا من حرق الدهون الداخلة كمصدر للطاقة، تراكمت الدهون داخل الخلايا التائية وتحولت إلى أشكال كيميائية تالفة، وهي عملية تُعرف بتأكسد/بيري أكسدة الدهون (lipid peroxidation). أظهرت تحليلات الجينات والدهون زيادة في علامات الدهون المؤكسدة والإجهاد، بينما بقي إنتاج الطاقة من الدهون ثابتًا. باختصار، في وجود الورم، تم تحويل الدهون التي كان يفترض أن تكون وقودًا إلى تفاعلات ضارة تُشيخ وتُعطل الخلايا التائية.
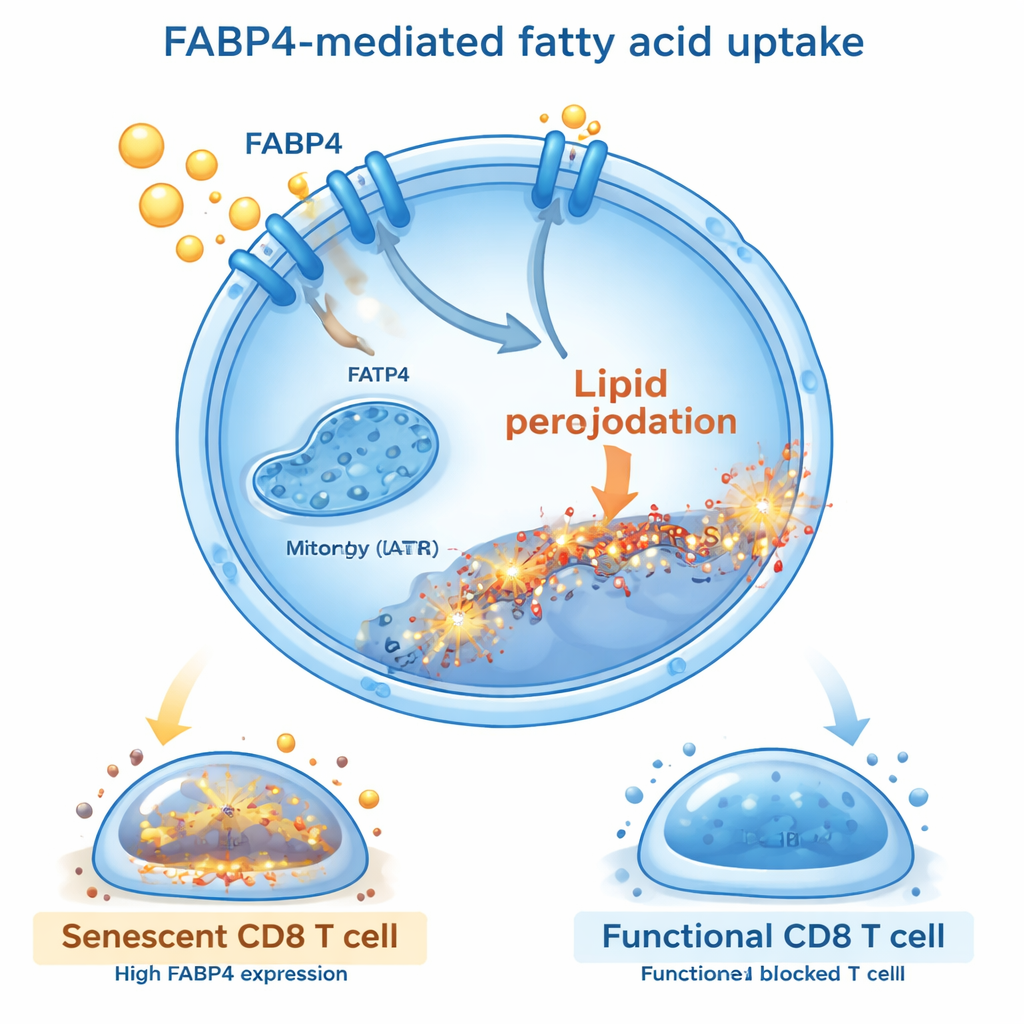
ناقِل الدهون FABP4 بوصفه بوابة محورية
بالنقر أعمق، سأل الباحثون أي الجزيئات تتحكم في هذا التدفق الضار للدهون. وجدوا أن بروتين ناقلًا يُدعى FABP4 كان مفعلًا بشدة في خلايا CD8 التائية المعرضة لمستخلصات الدهون أو حمض الأوليك. يعمل FABP4 كناقل، حاملًا الأحماض الدهنية طويلة السلسلة إلى داخل الخلايا. عندما حجبوا FABP4 باستخدام إما دواء جزيئي صغير (BMS309403) أو إسكات جيني، امتصّت الخلايا التائية دهونًا أقل، أبدت تأكسد دهون أقل، وكانت أقل عرضة للشيخوخة. هذه الخلايا التائية المحمية انقسمت بشكل أفضل، وأنتجت المزيد من جزيئات قتل السرطان مثل الإنترفيرون-غاما والجرانزيم B، وأطلقت إشارات مثبطة والتهابية أقل. إعادة مستويات FABP4 عكست هذه الفوائد، مؤكدة أن هذا الناقل هو مفتاح يربط امتصاص الدهون بشيخوخة الخلايا التائية.
من تجارب الفئران إلى استراتيجية علاجية محتملة
ثم اختبر الفريق حجب FABP4 في فئران حية لديها سرطان مبيض انتشر داخل البطن. أدى علاج الفئران بمثبط FABP4 إلى تقليل امتصاص الدهون والضرر الدهني في خلايا CD8 المستخرجة من السائل البطني، خفض نسبة الخلايا التائية المُشيخة، وزيادة مستويات جزيئات الفاعلية الرئيسية. عندما جمعوا مثبط FABP4 مع العلاج الكيميائي القياسي، شهدت الفئران عقدًا ورمية مرئية أقل، واستجابات تائية أقوى في الطحال والعقد اللمفاوية والاسيتس، وعاشت لوقت أطول من تلك التي أعطيت العلاج الكيميائي وحده. تشير هذه النتائج إلى أن استهداف استقلاب الدهون يمكن أن يجعل العلاجات الحالية أكثر فعالية عن طريق إحياء جنود جهاز المناعة في الخطوط الأمامية.
ما يعنيه هذا للمرضى
للقُرّاء غير المتخصصين، الخلاصة هي أنه في سرطان المبيض، ليس الورم وحده هو المهم، بل الحيّ الدهني الذي يعيش فيه أيضًا. يمكن للجزيئات المشتقة من الدهون، وخصوصًا أحماض دهنية معينة، أن تُشيخ خلايا T القاتلة قبل الأوان، فتجردها من قدرتها على مهاجمة السرطان. تحدد هذه الدراسة ناقل الدهون FABP4 باعتباره الجاني الرئيسي في هذه العملية. من خلال حجب FABP4، على الأقل في الفئران، يمكن للباحثين تقليل شيخوخة الخلايا التائية، واستعادة وظيفتها القاتلة، وتحسين أثر العلاج الكيميائي. وبينما يلزم المزيد من الأبحاث قبل أن يصبح هذا علاجًا للمرضى، تفتح الدراسة مسارًا جديدًا: علاج ليس فقط السرطان نفسه، بل أيضًا الفخاخ الأيضية في بيئته التي تعطل الجهاز المناعي.
الاستشهاد: Yu, C., Li, X., Qian, X. et al. Fatty acid uptake mediated by FABP4 promotes the formation of CD8+T cell senescence through lipid peroxidation in the adipocyte-rich microenvironment of Ovarian Cancer. Oncogenesis 15, 9 (2026). https://doi.org/10.1038/s41389-026-00600-w
الكلمات المفتاحية: سرطان المبيض, شيخوخة الخلايا التائية, استقلاب الأحماض الدهنية, البيئة الدقيقة للورم, FABP4