Clear Sky Science · ar
إعادة تنظيم الهيكل الخلوي الناتجة عن اندماج جديد بين الكيراتين K6-K14 تعزز خواص جذعية وسلاسة خلوية عبر اختيار مسار cGAS-STING
كيف تتفوق الخلايا السرطانية المتغيرة الشكل على بيئتها
الخلايا السرطانية لا تنمو فقط بلا ضابط؛ بل تتعلم أيضاً أن تغيّر وتلوِّى "هيكلها الداخلي" لتنجو وتختبئ وتنتشر. تكشف هذه الدراسة كيف يمكن لخلل بنيوي محدد داخل خلايا سرطان الرأس والعنق أن يكسر نواتها، ويشغّل إنذار خطر داخلي، ويدفعها إلى حالة سبات، ثم يساعدها في الظهور مجدداً كخلايا أكثر عدوانية وغزوًا ومشابهة للخلايا الجذعية. فهم هذا الطريق الميكانيكي لتطور السرطان قد يفتح طرقاً جديدة لوقف الانتكاس والانتشار.
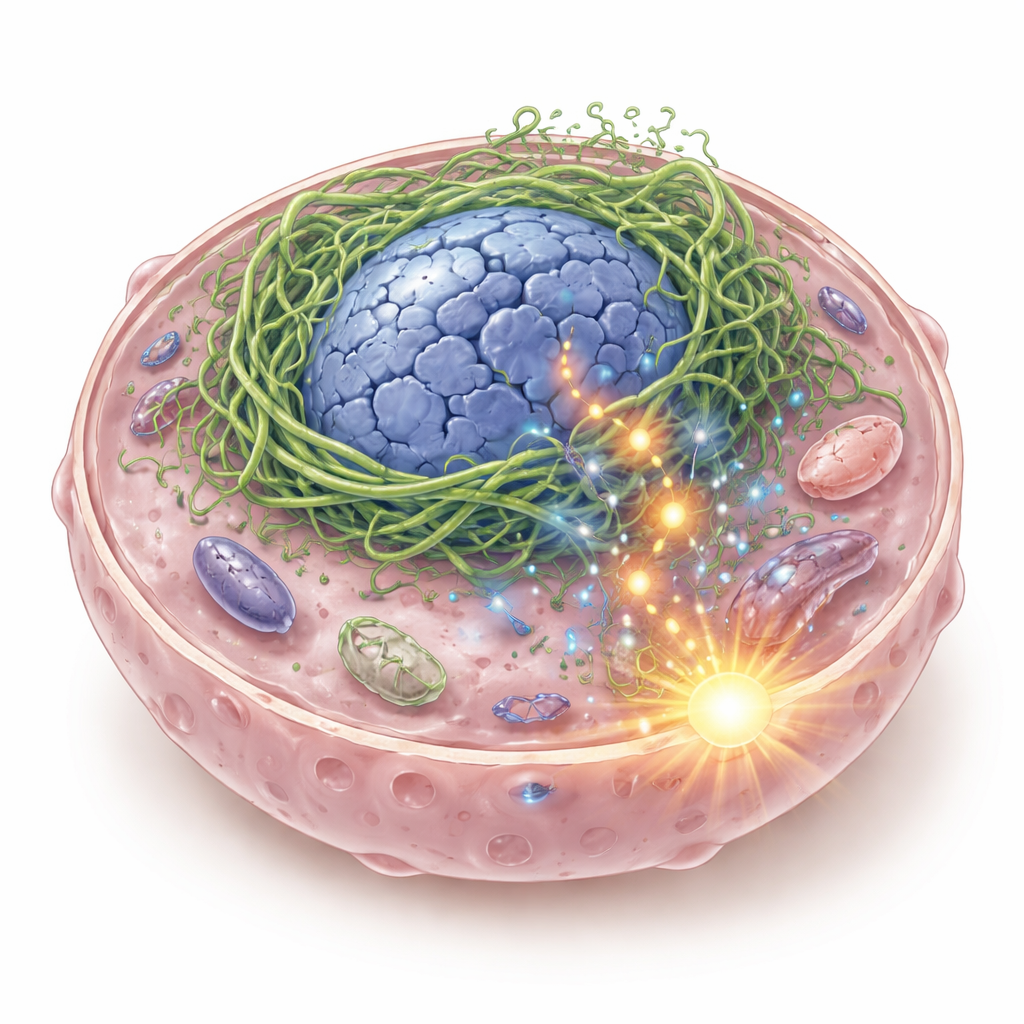
هيكل داخلي متصدع بعواقب خطرة
داخل كل خلية يوجد دعام مرن مكوّن من خيوط بروتينية يحافظ على شكل الخلية ونواتها ويساعدها على استشعار القوى الفيزيائية. ركّز المؤلفون على الكيراتينات، وهي عائلة من بروتينات الدعامة الشائعة في الأنسجة الطلائية، بما في ذلك البطانة الفموية والبلعومية. في بعض سرطانات الخلايا الحرشفية في الرأس والعنق، اكتشفوا كيراتيناً هجيناً يدعى K6-K14/V5، يتكوّن عندما تندمج جينتا كيراتين. عندما يُعبَّر عن هذا البروتين الاندماجي في الخلايا السرطانية، لا يشكل شبكة داعمة ناعمة؛ بل يتكتّل بإحكام حول النواة، مشوِّهاً إياها إلى هياكل مجوفة مشوهة ومسبّباً كسوراً في الحمض النووي. تتسرب قطع من الحمض النووي إلى سائِل الخلية، حيث تُكشف بواسطة نظام استشعار مناعي يُعرف بـ cGAS–STING، الذي عادةً ما يطلق الإنذار عند وجود حمض نووي فيروسي.
من ضغط موت الخلايا إلى البقاء المختبئ
التأثير الفوري لهذا الضرر النووي يكون ضاراً للخلايا السرطانية: يتباطأ نموها ويموت الكثير منها. ومع ذلك، ينجو جزء منها. يتأثر الناجون بشدة ببيئتهم الفيزيائية. على الأطباق البلاستيكية المسطحة العادية يتلاشى وجودهم تدريجياً، لكن عند نموهم داخل هلام كولاجين رخوي—أقرب إلى ملمس النسيج الحقيقي—فهم يستمرون ويظهرون مجدداً كسكان جدد سُمّوا خلايا 3D-V5. تُظهر تحليلات نشاط الجينات أن هذه الخلايا تستجيب لإنذار الضرر المستمر بتشغيل الاستحداث الذاتي (الانتحال)، وهو برنامج تنظيف ذاتي يعيد تدوير الأجزاء التالفة، خصوصاً الميتوكوندريا المعطوبة. يساعدهم هذا الاستجابة على الدخول في حالة سبات منخفضة النشاط تُمكّنهم من تحمل الضغوط بدلاً من إبادتهم.
الخلايا النائمة تعيد توصيل برامجها وتتهيأ للحركة
خلال سباتها، تعيد هذه الخلايا الناجية بهدوء كتابة برامجها الداخلية. تغيّر مزيج بروتينات الكيراتين وتتبنّى حالة انتقال ظهاري–وِباني جزئية (pEMT)—هوية وسطية تحافظ على بعض الصفات الطلائية لكنها تكسب مرونة وقدرة على الحركة. تصبح أفضل بكثير في تكوين الكرات وزرع مستعمرات خلوية جديدة، وهو سمة مميزة للخواص الجذعية السرطانية. مع مرور الوقت، تستعيد خصائصها الميكانيكية: تعيد تصلب نواتها، وتبني ألياف أكتين قوية، وتطوّر نتوءات طويلة تستكشف وتمسك المصفوفة المحيطة. كما تزيد من إنتاج إنزيمات تُعرف بالماتريكس ميتالوبروتينازات (MMPs)، التي تفرّغ الشبكة خارج الخلوية وتفتح مسارات للغزو.
التواصل مع الخلايا المجاورة لبناء موطن داعم
هذه الخلايا المعاد برمجتها لا تعمل منعزلة. لاحظ الفريق أن خلايا 3D-V5 تطلق أعداداً كبيرة من حزم صغيرة تُسمى الحويصلات خارج الخلوية إلى محيطها. عندما تحيط هذه الحويصلات بخلايا ليفية فموية قريبة—خلايا نسيج ضام—تتغير نشاطات الجينات فيها، فتصير أشبه بالخلايا الليفية المرتبطة بالسرطان التي تدعم نمو الورم. ترتكز العديد من الإشارات المتبادلة حول محور FGF–FGFR، عائلة عوامل نمو ومستقبلاتها المعروفة بدفعها للتكاثر والمرونة والمقاومة. في كل من المزارع المخبرية والأورام في الفئران، أدّى حجب نشاط FGFR إلى تقليل هذه الميزة النمائية. في الحيوانات، كانت الأورام المكوّنة من خلايا 3D-V5 قليلة التمايز، أكثر غزواً، غنية بعلامات الخلايا الجذعية، وأكثر ميلاً للانتشار خارج موقع الحقن.
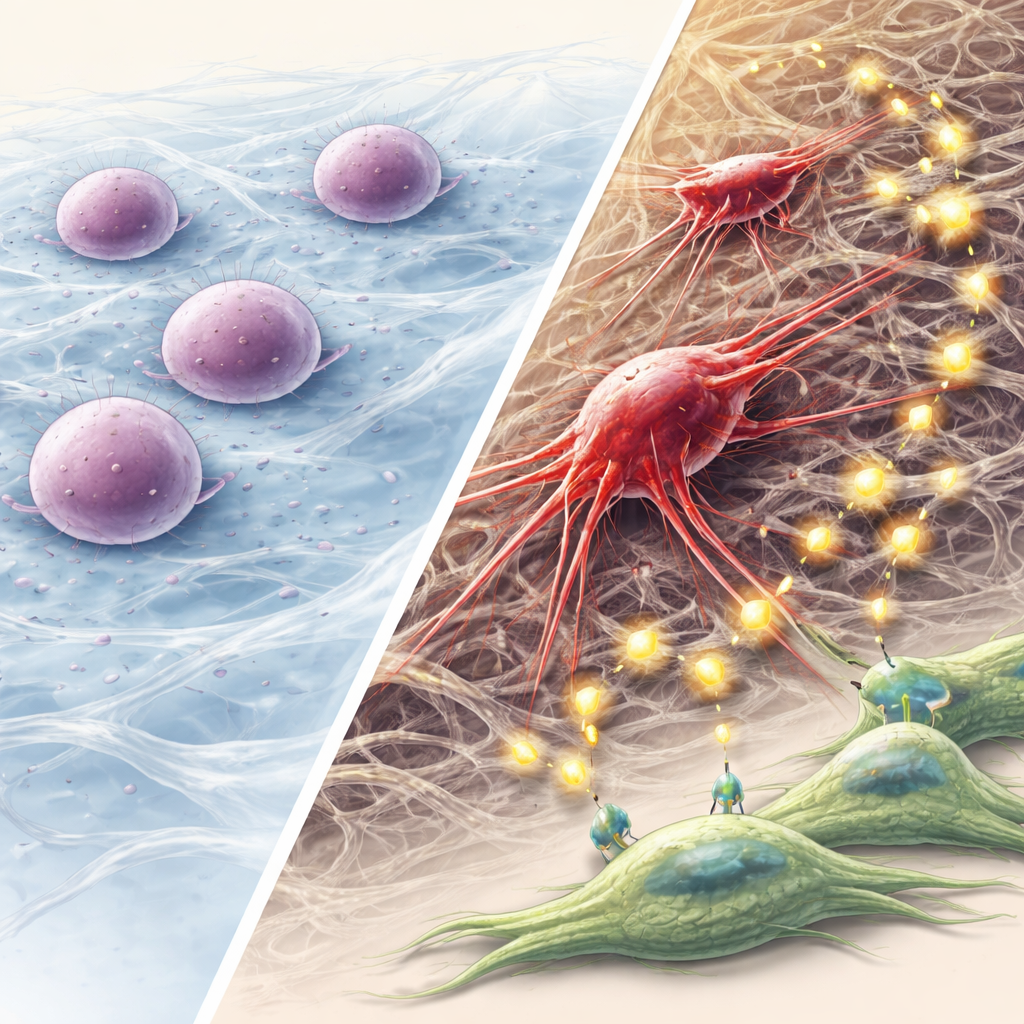
لماذا يهم هذا المسار الميكانيكي إلى سرطانية عدوانية
تقترح هذه الدراسة نموذجاً خطوة بخطوة: يؤدي اندماج الكيراتين إلى اضطراب الدعامة الداخلية للخلية، وسحق النواة، وإطلاق إنذار تلف الحمض النووي؛ ثم يسمح الاستحداث الذاتي لعدد قليل من الخلايا بدخول السبات بدلاً من الموت؛ ومع مرور الوقت، يعيد الناجون تنظيم هيكلهم، ويكتسبون صفات جذعية وغزوية، ويعيدون تشكيل بيئتهم عبر الحويصلات وإشارات FGF. للقراء غير المتخصصين، الرسالة الأساسية هي أن القوى الفيزيائية والبروتينات الهيكلية داخل الخلايا يمكن أن تكون مهمة تماماً مثل الجينات والمواد الكيميائية في دفع تطور السرطان. قد يوفر استهداف مسار الضغط الميكانيكي–الاستحداث الذاتي–FGF، لا سيما في سرطانات الرأس والعنق التي تحوي اندماجات كيراتين، استراتيجيات جديدة لمنع استيقاظ وانتشار الخلايا الورمية النائمة.
الاستشهاد: Chen, IH., Ravichandran, S., Lai, MT. et al. Cytoskeleton reorganization induced by a novel K6-K14 keratin fusion promotes cancer stemness and cellular plasticity via cGAS-STING selection. Oncogenesis 15, 5 (2026). https://doi.org/10.1038/s41389-026-00598-1
الكلمات المفتاحية: الخواص الجذعية للسرطان, هيكل الخلية, سبات الورم, سرطان الرأس والعنق, تحويل الإشارات الميكانيكية