Clear Sky Science · ar
دور دي مثيلاز الهستون PHF2 كمثبط للأورام في سرطان الكبد الكبدي عن طريق تنظيم SRXN1
لماذا تهم هذه الدراسة حول سرطان الكبد
يعد سرطان الكبد واحداً من أخطر أنواع السرطان عالمياً، والأدوية الحالية تطيل العمر بشكل متواضع فقط للعديد من المرضى. تطرح هذه الدراسة سؤالاً مختلفاً: بدلاً من استهداف الجينات المعروفة بأنها تقود السرطان، هل يمكننا استغلال كيفية تغليف الحمض النووي ووضع العلامات الكيميائية عليه داخل خلايا الكبد لإيجاد خيارات علاجية جديدة وأكثر دقة؟ ركز الباحثون على بروتين قليل المعرفة يُدعى PHF2 وكشفوا كيف قد يساعد في منع تحول خلايا الكبد إلى خلايا سرطانية.
البحث عن نقاط ضعف في نظام السيطرة على السرطان
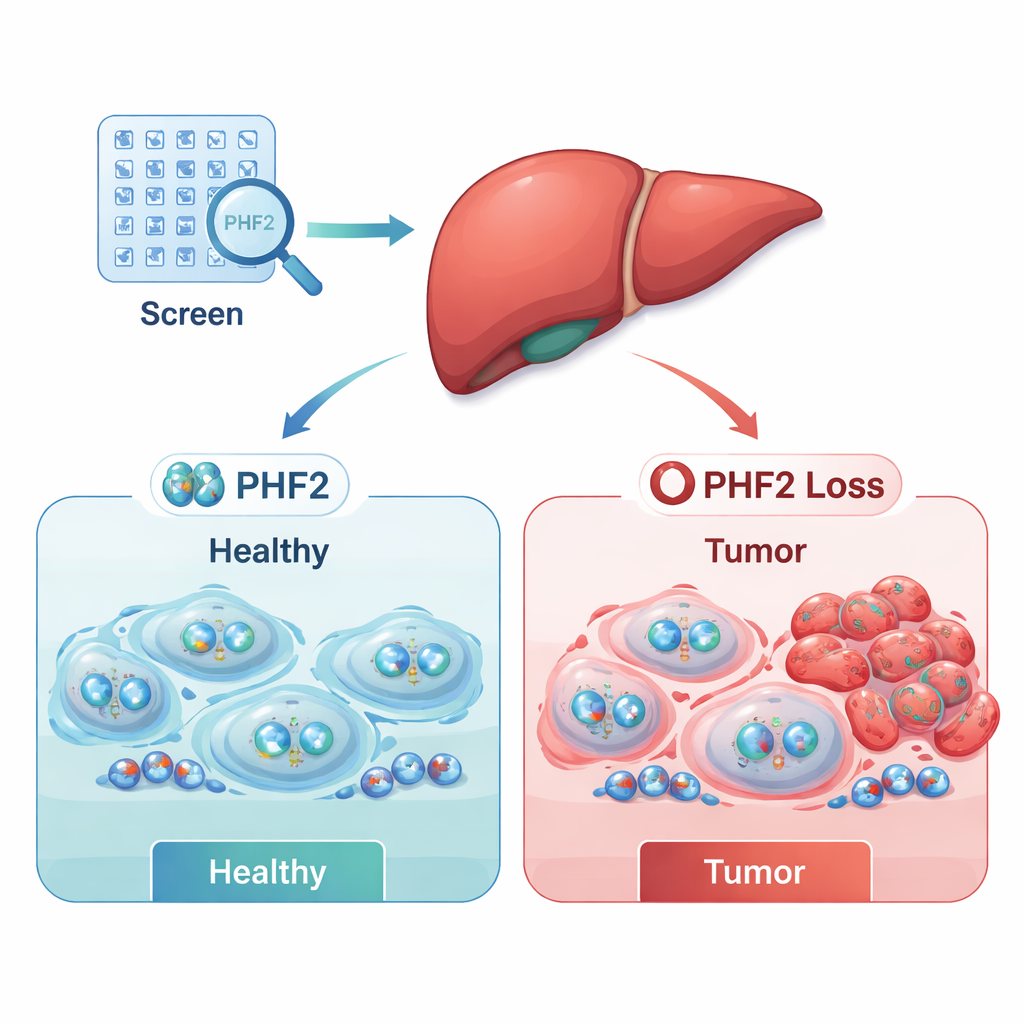
السرطان لا ينجم عن جينات معطوبة فقط؛ بل يغذّيه أيضاً خلل في الضوابط "فوق الجينية" — العلامات الكيميائية ومجمعات البروتين التي تقرر أي الجينات تُشغَّل أو تُسكَّت. في سرطان الخلايا الكبدية، الشكل الأكثر شيوعاً لسرطان الكبد، يتعرض كثير من هؤلاء المنظمين للخلل. اختبر الفريق بشكل منهجي 497 منظمًا فوق جينياً في ستة خطوط خلوية لسرطان الكبد، باستخدام أدوات RNA لتقليل كل من هؤلاء المنظمين مؤقتاً واحدًا تلو الآخر ثم قياس مدى بقاء خلايا السرطان. صُمِّم هذا الفحص الكبير لكشف أي المنظمين تعتمد عليهم الأورام للنمو، وأيهم يعمل عادة كمكبح لتشكّل الورم.
اكتشاف مساعدين وحماة جدد للسرطان
كشف الفحص مجموعتين واسعتين: مسرّعات محتملة للسرطان (جينات سرطانية) يؤدي فقدها إلى ضعف بقاء الخلايا السرطانية، و"مكابح" محتملة (مثبطات الأورام) يؤدي فقدها إلى ازدياد نمو الخلايا السرطانية. بدمج بيانات المختبر مع مجموعات بيانات مرضى عامة واسعة، ضيّق الباحثون القائمة إلى عدد قليل من المرشحين ذوي الصلة السريرية. اثنان من المنظمين، SUPT7L وSMARCC1، بدت مستويات نشاطهما أعلى في الأورام وكانا مرتبطين ببقاء أسوأ. في المقابل، كان مُنظم واحد—PHF2—أقل نشاطًا في كثير من أورام الكبد، والمرضى الذين احتفظت أورامهم بمستويات أعلى من PHF2 عاشوا عادة لفترة أطول. أشارت هذه الأنماط إلى أن PHF2 قد يعمل كمثبط للورم في سرطان الكبد البشري.
كيف يغيّر فقدان PHF2 خلايا سرطان الكبد
لاختبار PHF2 بعمق أكبر، مهندس الفريق خلايا سرطان الكبد لجعلها تُنتج هذا البروتين بمستويات أقل بشكل مستقر وتتبعوا سلوكها مع مرور الوقت. نمت الخلايا التي انخفض فيها PHF2 بسرعة أكبر وأظهرت مستويات أعلى من Ki-67، وهو وسم يدل على انقسام خلوي نشط، ما يشير إلى أن PHF2 يساعد عادة في تقييد التكاثر. كانت هذه التأثيرات أكثر وضوحًا في خطوط خلايا سرطان الكبد العدوانية بالفعل، مما يوحي بأن فقدان PHF2 وحده قد لا يطلق السرطان، لكنه يمكن أن يسرّع نمو الخلايا الخبيثة بعد تكوّن الأورام.
رابط مفاجئ بدفاعات الخلية ضد الإجهاد
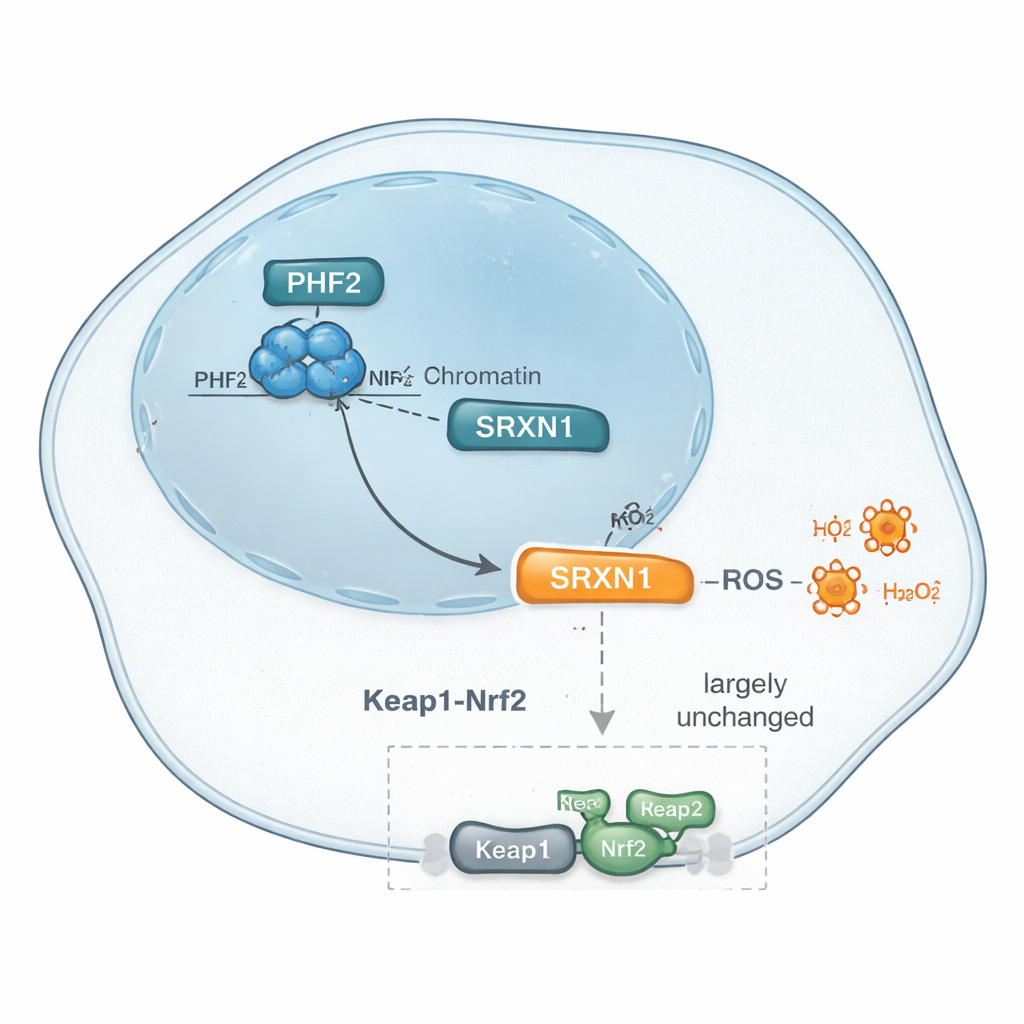
بعد ذلك، استخدم الباحثون طرقًا حديثة لمساءلة البروتينات لتصنيف آلاف البروتينات التي تغيرت مستوياتها عند تقليل PHF2. من بين العديد من التغيّرات الطفيفة، برز نمط واحد: انخفاض مستمر في مستويات بروتين واقٍ من الإجهاد يُدعى SRXN1 عند فقدان PHF2. يساعد SRXN1 الخلايا في إدارة أنواع الأكسجين التفاعلية — منتجات ثانوية كيميائية قد تُلحق الضرر بالحمض النووي والبروتينات لكنها يمكن أيضًا أن تدفع خلايا السرطان إلى التكيّف. أشارت البيانات إلى أن PHF2 يساعد في الحفاظ على مستويات SRXN1، وأن تغيير هذا التوازن قد يؤثر على كيفية استجابة خلايا سرطان الكبد للإجهاد الداخلي وفي نهاية المطاف على سرعة نموها.
العمل خارج مسار إجهاد معروف
عادةً ما يتحكم في SRXN1 مفتاح استجابة الإجهاد المسمى Nrf2، الذي يشغّل العديد من جينات مضادات الأكسدة عندما تواجه الخلايا إجهادًا تأكسديًا. بما أن SRXN1 انخفض عندما زُجّ PHF2 إلى الانخفاض، تساءل الفريق عما إذا كان PHF2 قد يعمل ببساطة عبر هذا المسار المعروف Nrf2. فحصوا جينات وبروتينات مرتبطة بـNrf2، عالجوا الخلايا بأدوية تنشّط Nrf2 عن طريق حجب مثبطه Keap1، واستخدموا أدوات جينية لتقليل Keap1 مباشرة. عبر هذه الاختبارات، بدت استجابة الخلايا الناقصة PHF2 مشابهة إلى حد كبير لاستجابة الخلايا الطبيعية، ولم تظهر تحليلات المسارات وعوامل النسخ الكبرى أن Nrf2 كان لاعبًا رئيسيًا. بدلًا من ذلك، برزت عوامل أخرى، بما فيها ZNF384 وNrf1 — كلاهما سبق ربطهما بسرطان الكبد — كمرشحين. مجتمعة، تشير الأدلة إلى أن سيطرة PHF2 على SRXN1 والاستجابات المضادة للأكسدة قد تتجاوز إشارات Nrf2 الكلاسيكية، ما يوحي بوجود مسار مميز لتنظيم الإجهاد في هذه الأورام.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
لغير المتخصص، الخلاصة الرئيسية هي أن هذه الدراسة تحدد PHF2 كعامل وقائي واعد في سرطان الكبد: عندما يكون PHF2 موجودًا ونشطًا، تنمو خلايا الورم ببطء أكبر؛ وعندما يقل، تكسب الخلايا ميزة في النمو وتغيّر طريقة تعاملها مع إجهاد الخلية. ونظرًا لأن PHF2 نفسه قد يكون صعب الاستهداف أو التعزيز باستخدام أدوية جزيئية صغيرة تقليدية، يشير المؤلفون إلى استراتيجيات ناشئة مثل العلاجات القائمة على RNA أو الأدوية التي تعزز نشاط PHF2 عن طريق شركاء إشارات علويين. كما يؤكدون أن تأثيرات PHF2 تعتمد على السياق — فقد تختلف تبعًا لطفرات أخرى مثل حالة p53 — لذا من المرجح أن أي علاج مستقبلي يحتاج إلى اختيار دقيق للمرضى. بوجه عام، يكرّس العمل فهمنا لكيفية تشكيل المنظمين فوق الجينيين لسلوك سرطان الكبد ويفتح سبلًا جديدة لتصميم علاجات تستعيد أو تحاكي التأثير المثبط للورم الخاص بـPHF2.
الاستشهاد: Thng, D.K.H., Hooi, L., Yong, W.K. et al. The role of histone demethylase PHF2 as a tumour suppressor in hepatocellular carcinoma by regulating SRXN1. Oncogenesis 15, 6 (2026). https://doi.org/10.1038/s41389-026-00597-2
الكلمات المفتاحية: سرطان الخلايا الكبدية, تنظيم فوق جيني, PHF2, SRXN1, علاج سرطان الكبد