Clear Sky Science · ar
تحلل HILPDA الوسيط عبر TRIM21 يتغلب على مقاومة العلاج المناعي المضاد لـ PD-1 في سرطان الثدي من خلال تقييد بالميتويلation PD-L1
لماذا تتوقف بعض علاجات السرطان المناعية عن العمل
أدت الأدوية التي تطلق الجهاز المناعي، مثل علاجات مضادة لـ PD‑1، إلى تحول في علاج عدة أنواع من السرطان، بما في ذلك أشكال عدوانية من سرطان الثدي. ومع ذلك، فإن العديد من الأورام إما لا تستجيب مطلقًا أو تجد في نهاية المطاف طرقًا للهروب. يغوص هذا البحث في أحد مسارات الهروب هذه في سرطان الثدي ثلاثي السلبية ويبين كيف أن إعادة توصيل استقلاب الدهون في الورم — ودواء مُعاد توظيفه يُدعى فينريتينيد — قد يعيد فتح الباب للجهاز المناعي عندما تفشل العلاجيات المناعية القياسية. 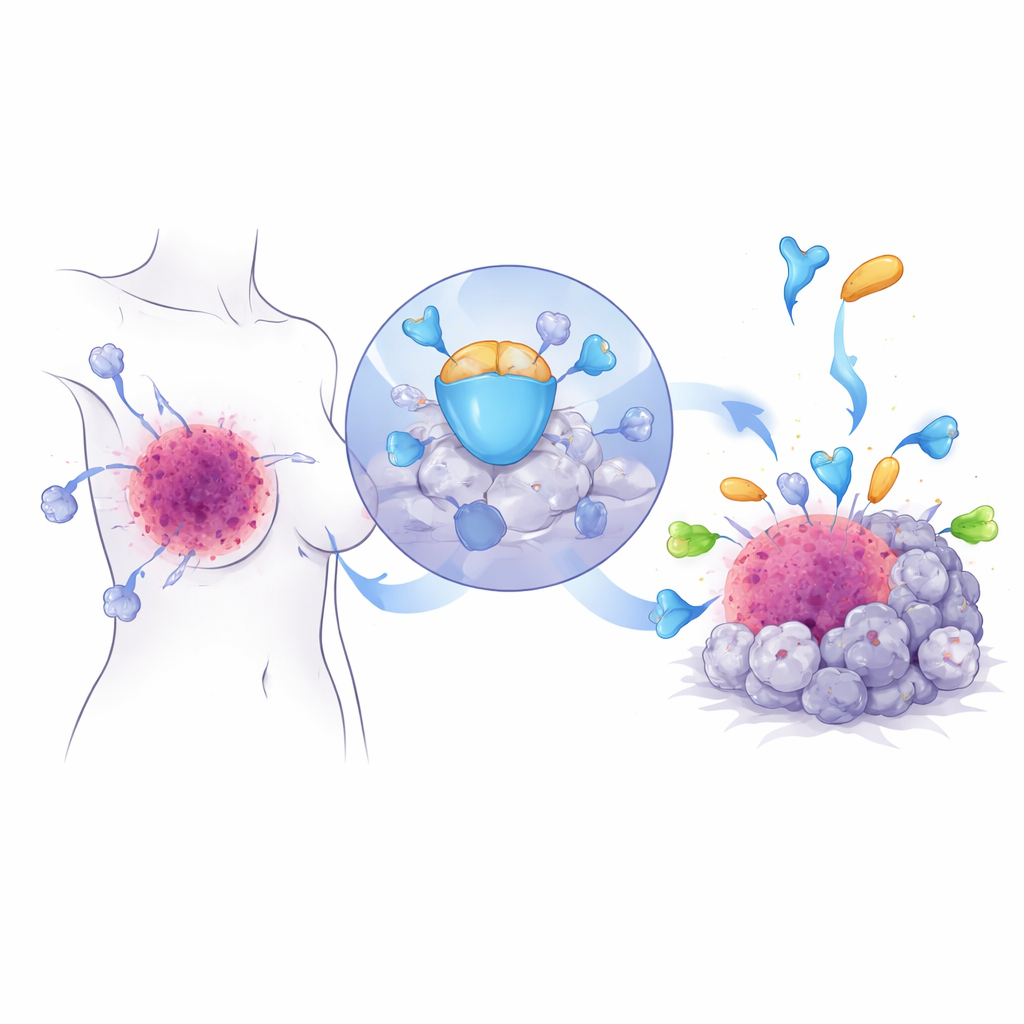
مساعد خفي يحمي الأورام
ركز الباحثون على بروتين قليل المعرفة يُسمى HILPDA، ارتبط سابقًا بكيفية تعامل الخلايا مع الدهون تحت الضغط. بمقارنة أورام ثدي فئران بقيت حساسة لعلاج مضاد لـ PD‑1 مع أورام أصبحت مقاومة، وجدوا أن مستويات HILPDA كانت أعلى بكثير في السرطانات المقاومة. وأكدت تحليلات قواعد بيانات كبيرة وعينات أورام من نساء يعانين سرطان الثدي أن HILPDA أكثر وفرة في الأورام مقارنة بالنسيج الثديي الطبيعي، خاصة في مرض ثلاثي السلبية، وأن المرضى الذين تعبر أورامهم عن HILPDA بكميات أكبر يميلون إلى نتائج أسوأ. كما أن الأورام من أشخاص لم يستفيدوا من أدوية حاصرة لـ PD‑1 كانت تحتوي أيضًا على HILPDA أعلى، مما يربط هذا البروتين مباشرة بفشل العلاج.
كيف تحوّل الأورام المشهد المناعي ضدنا
لكي يعرف الفريق ما الذي يفعله HILPDA داخل الأورام فعليًا، هندسوا خلايا سرطان الثدي لتنتج البروتين بوفرة أو تفتقده ثم نمتها مع خلايا مناعية بشرية أو في الفئران. عندما كان HILPDA مرتفعًا، جذبت الأورام المزيد من الخلايا التنظيمية التائية، وخلايا قمع مشتقة من النخاع، والبلعمات الشبيهة بـ M2 — وهي أنواع من الخلايا المناعية التي تخفف الهجوم وتساعد السرطانات على الاختباء. في الوقت نفسه، انخفض عدد وحيوية خلايا CD8 القاتلة والخلايا القاتلة الطبيعية، وتقلصت قدرتها على إطلاق الجزيئات السامة والإشارات الالتهابية. إخماد HILPDA قلب هذه الصورة: استضافت الأورام خلايا مثبطة أقل، وخلايا قاتلة أكثر نشاطًا، ونمت ببطء أكبر، وقلّت النقائل. والأهم من ذلك، عندما تلقّت الحيوانات ذات الأورام منخفضة HILPDA علاجًا مضادًا لـ PD‑1، تناقصت أورامها أكثر وعاشت الفئران لفترة أطول، ما يبيّن أن HILPDA يتحكم في مدى فعالية العلاج المناعي.
صناعة الدهون، درع جزيئي، والهروب المناعي
بالغوص أعمق، كشف العلماء كيف يعيد HILPDA تشكيل استقلاب الورم لتقوية الدفاعات المناعية. داخل الخلايا السرطانية، يلتصق HILPDA ببروتين مرافق يُدعى HSP90 لتثبيت عامل نسخي، KLF5، الذي يحفز إنتاج الدهون. هذا الثلاثي يعزز تصنيع الأحماض الدهنية، وخاصة البالمتيتات، ويملأ الخلايا السرطانية بقطرات دهنية. ثم تُرفق إحدى هذه الدهون بـ PD‑L1، بروتين الضابط الذي يجلس على سطح الورم ويُرسل إشارة «لا تهاجم» للخلايا المناعية. أظهر الفريق أن إضافة بالميتيت إلى موقع محدد على PD‑L1 تعمل كصمغ جزيئي: تساعد PD‑L1 على الثبات في غشاء الخلية وتمنع تكسّرها. أدى طفر هذا الموقع الواحد إلى فقدان PD‑L1 للاستقرار وضعف قدرتها على حماية الخلايا السرطانية، حتى عندما كان HILPDA وفيرًا. بعبارة أخرى، تغذي صناعة الدهون المدفوعة بـ HILPDA تعديلًا كيميائيًا على PD‑L1 يحوّل درع الورم المناعي من هش إلى معزز بقوة.
المكبح المدمج الذي يمكن دفعه
كل مسرع يحتاج إلى مكبح، وفي هذه الحالة يكون المكبح بروتينًا آخر يُدعى TRIM21. اكتشف المؤلفون أن TRIM21 يتعرف على HILPDA ويعلّمه بعلامات جزيئية ترسله إلى آلية التخلص داخل الخلية. في أورام الثدي من المرضى، كانت مستويات TRIM21 تميل لأن تكون منخفضة عندما يكون HILPDA مرتفعًا، وكان انخفاض TRIM21 مرتبطًا بنتائج سيئة، ما يوحي بأن هذا النظام المكبح الطبيعي غالبًا ما يكون ضعيفًا في السرطان. بحث الفريق بعد ذلك عن أدوية يمكنها تقوية TRIM21 وحددوا فينريتينيد، ريتينويد تم اختباره بالفعل في البشر. في نماذج خلوية وحيوانية لسرطان الثدي ثلاثي السلبية، عزز فينريتينيد نشاط TRIM21، وسرّع تفكك HILPDA، وخفض تصنيع الدهون وتعديل PD‑L1 الوقائي، وأبطأ نمو الورم وانتشاره. والأبرز من ذلك، أن الجمع بين فينريتينيد والعلاج المضاد لـ PD‑1 جعل الأورام أكثر عرضة للهجوم المناعي، بزيادة خلايا T القاتلة والخلايا القاتلة الطبيعية مع تقليل الخلايا المثبطة في البيئة الدقيقة للورم. 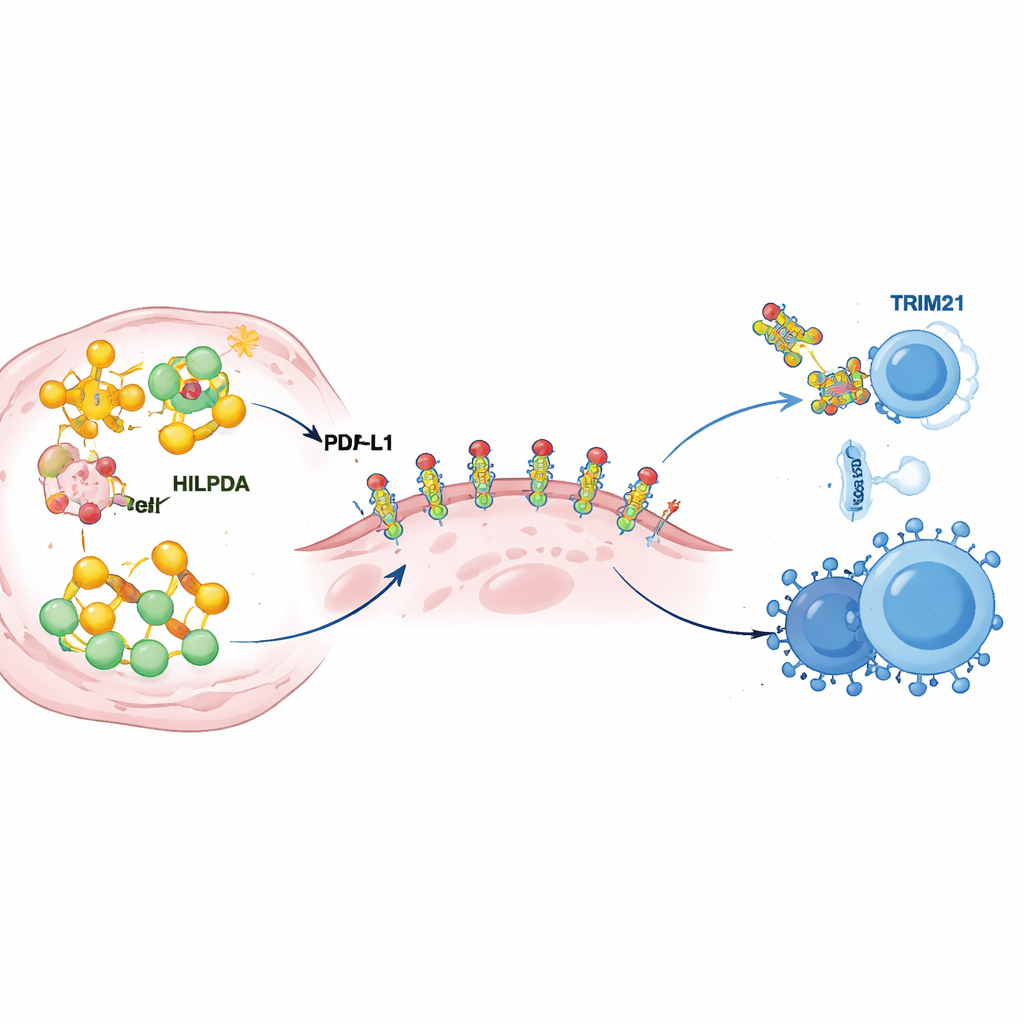
ماذا يعني هذا لرعاية السرطان المستقبلية
يكشف هذا العمل سلسلة من الأحداث حيث ترفع الخلايا السرطانية المتأثرة بالضغط مستوى HILPDA، وتزيد إنتاج الدهون، وتعزز كيميائيًا PD‑L1 على سطحها، مما يسمح لها بمواصلة قمع الخلايا المناعية حتى في وجه الأدوية الحابسة لـ PD‑1. يعمل TRIM21 كضمان داخلي يمكنه تفكيك HILPDA، لكنه غالبًا ما يكون ضعيفًا في الأورام. من خلال اكتشاف أن فينريتينيد يمكن أن يعيد تنشيط هذا الضمان، يشير البحث إلى طريقة عملية لدمج دواء استقلابي مع العلاج المناعي القائم للتغلب على المقاومة. إذا تأكد ذلك في تجارب سريرية، فقد يعطي استهداف محور TRIM21–HILPDA–PD‑L1 المرضى الذين يعانون سرطان الثدي ثلاثي السلبية صعوبة العلاج فرصة ثانية للاستفادة من العلاجات المعتمدة على الجهاز المناعي.
الاستشهاد: Wang, X., Li, G., Wu, J. et al. TRIM21-mediated degradation of HILPDA overcomes anti-PD-1 immunotherapy resistance in breast cancer by limiting PD-L1 palmitoylation. Oncogene 45, 1338–1356 (2026). https://doi.org/10.1038/s41388-026-03728-6
الكلمات المفتاحية: سرطان الثدي ثلاثي السلبية, مقاومة العلاج المناعي, بالميتويلية PD-L1, تمثيل الدهون في الورم, فينريتينيد