Clear Sky Science · ar
سيريبْلون (CRBN) يثبّط نقائل سرطان البروستاتا عبر تنظيم سلبي لإنزيم 6‑فوسفوجلوكونات ديهيدروجيناز (6PGD)
لماذا هذا البحث مهم
عندما ينتشر سرطان البروستاتا من البروستاتا إلى أعضاء أخرى، يصبح علاجه أصعب بكثير وغالبًا ما يكون قاتلًا. تكشف هذه الدراسة كيف يساعد بروتين خَلوي قليل المعرفة باسم سيريبْلون (CRBN)، الذي يعمل كآلية «مراقبة جودة»، في منع انتشار سرطان البروستاتا عن طريق تفكيك إنزيم أيضي يغذي سلوكًا عدوانيًا. فهم هذا النظام الكابح الداخلي يفتح آفاقًا لطرق جديدة لإبطاء أو إيقاف النقائل، لا سيما في أشكال المرض التي يصعب علاجها.
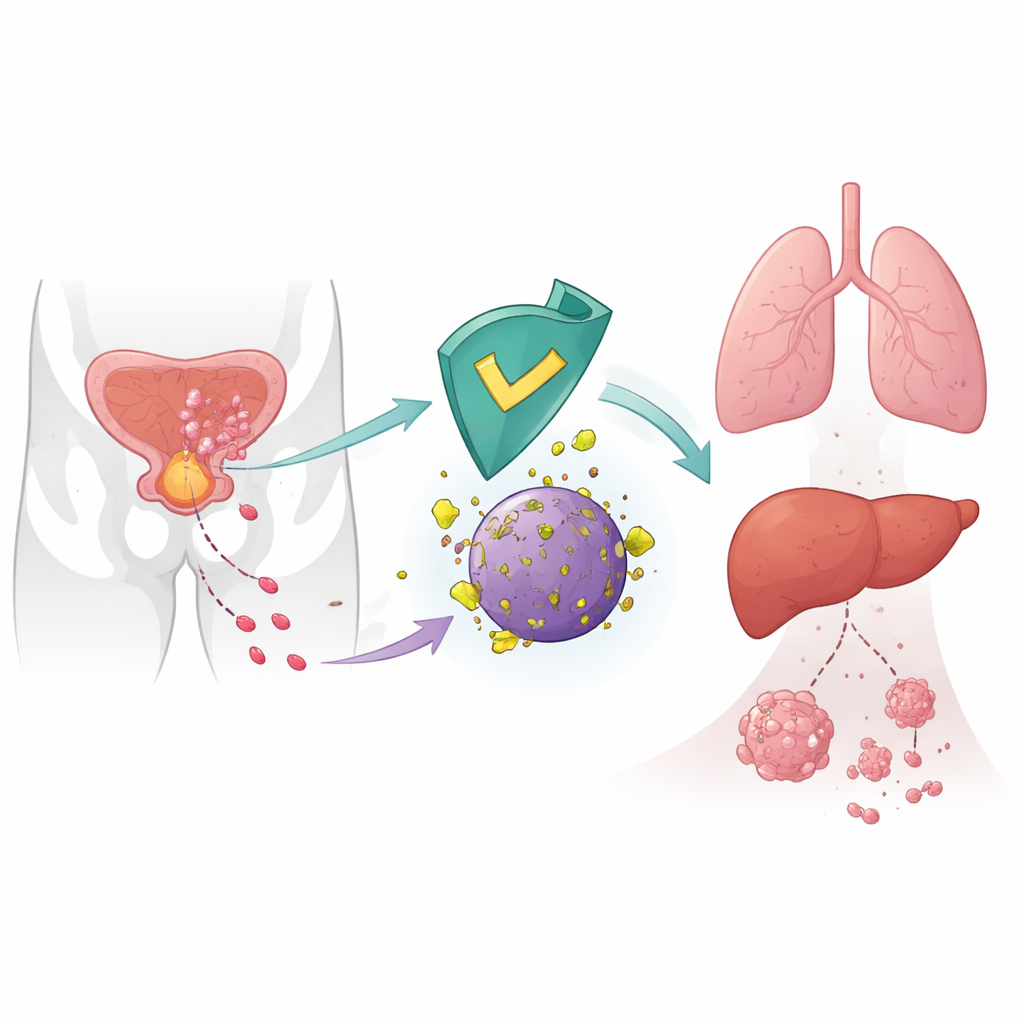
كابح داخلي لانتشار السرطان
الخلايا السرطانية لا تنتشر عشوائيًا؛ بل تعيد توصيل آلياتها الداخلية للتحرك والغزو والاستعمار في أعضاء بعيدة. ركّز المؤلفون على CRBN، بروتين معروف أساسًا كهدف لأدوية مثل ثاليدوميد المستخدمة في سرطانات الدم. في الخلايا السليمة، يشكل CRBN جزءًا من وحدة جزيئية للتخلص تضع وسمًا على بروتينات معينة لتدميرها. أشارت أعمال سابقة إلى أن مستويات CRBN المنخفضة في الأورام ترتبط بنتائج أسوأ، لكن دوره المباشر في النقائل لم يكن واضحًا. هنا يظهر الباحثون أن CRBN يعمل كمثبط طبيعي لانتشار سرطان البروستاتا عن طريق استهداف إنزيم أيضي يُدعى 6‑فوسفوجلوكونات ديهيدروجيناز (6PGD) لتحطيمه.
محرك أيضي تستولي عليه الخلايا السرطانية
يعمل 6PGD في مسار أيضي يعرف بمسار الفوسفات الخماسي التأكسدي (oxidative pentose phosphate pathway)، الذي يساعد الخلايا على توليد NADPH، جزيء يوفر كلاً من مواد البناء وقوة مضادة للأكسدة. العديد من الأورام تكثف هذا المسار للنمو بشكل أسرع وتحمل الضغوط. وجد الفريق أن عينات سرطان البروستاتا من المرضى تميل إلى احتواء CRBN أقل و6PGD أكثر مقارنةً بنسيج البروستاتا الطبيعي، وأن هذا الخلل أكثر بروزًا في أشكال المرض العدوانية. في خطوط خلايا سرطان البروستاتا، أدى تقليل CRBN أو تحليله بمركب مصمم إلى ارتفاع مستويات بروتين 6PGD ونشاطه الإنزيمي، مما زاد NADPH. إعادة CRBN كان لها التأثير المعاكس، خافضةً 6PGD وNADPH دون تغيير رسالة جين 6PGD الأساسية، مما يشير إلى ضبط على مستوى البروتين.
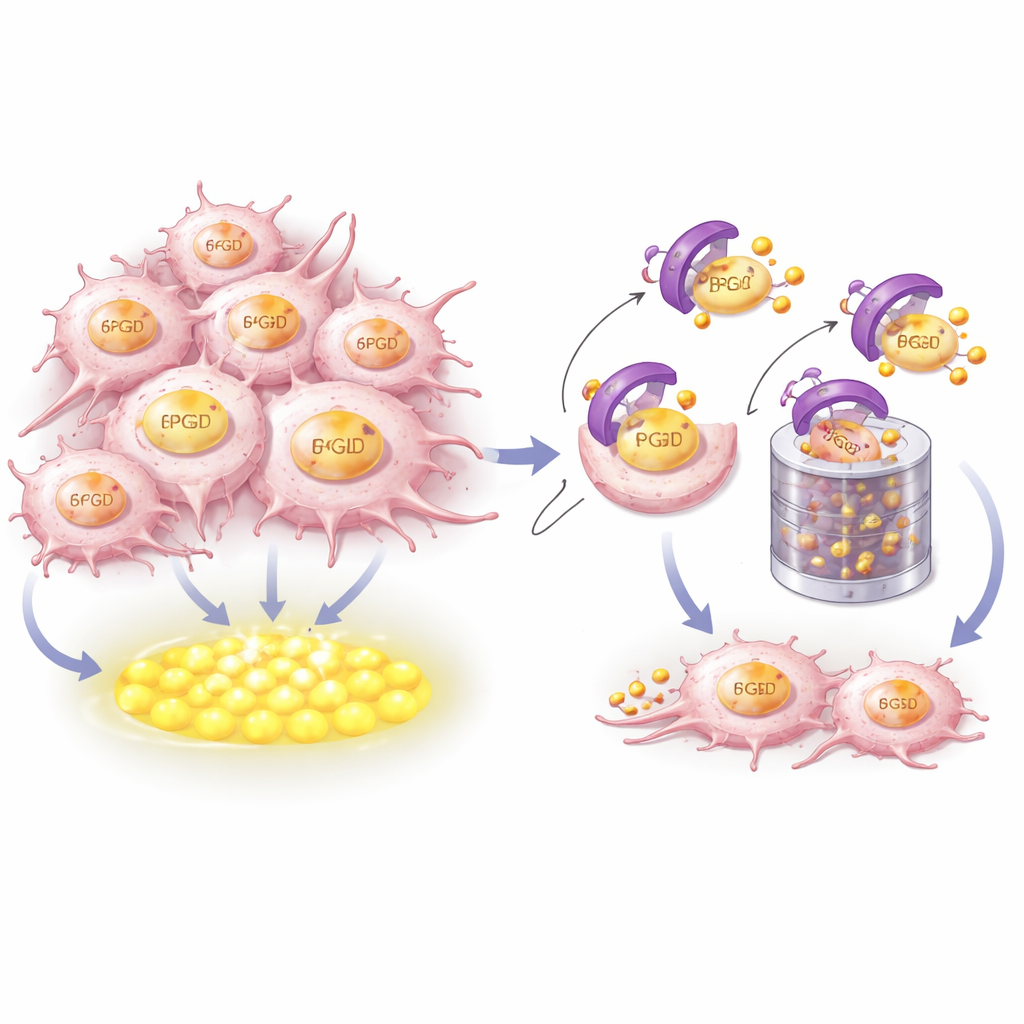
كيف يتعرف CRBN على مصدر الوقود ويقضي عليه
لفهم كيفية سيطرة CRBN على 6PGD، جمع الباحثون النمذجة الهيكلية مع تجارب بيوكيميائية. أظهروا أن CRBN يلتقط فعليًا مقطعًا لولبيًا قصيرًا ومحفوظًا جيدًا قرب الطرف الذيل لـ6PGD. تشكل أحماض أمينية رئيسية على كلا البروتينين واجهة إرساء محكمة. عندما تغيرت نقاط التلامس هذه، لم يعد CRBN قادرًا على الارتباط بـ6PGD، أو ربط شارات اليوبيكويتين الصغيرة التي تميّزه للتخلص، أو إرساله إلى آلة التفكيك الخلوية المعروفة بالمُبِرِّد البروتيني (البروتيازوم). والجدير بالذكر أن سطح التعرف هذا منفصل عن الجيب الذي ترتبط به الأدوية المنظمة للمناعة على CRBN، مما يعني أن سيطرة CRBN على 6PGD جزء من دوره المنزلي الطبيعي وليس أثرًا محرضًا دوائيًا.
من استقلاب متغير إلى خلايا متجولة
تنعكس عواقب هذه المصافحة الجزيئية على سلوك الخلية. في خلايا سرطان البروستاتا التي تفتقر إلى CRBN، صاحَبَ ارتفاع 6PGD وNADPH زيادة في الحركة والغزو عبر حواجز اصطناعية، وهي سمات تشير إلى قابلية أعلى للنقائل. عند إفراط إنتاج CRBN، أصبحت الخلايا أقل حركة وغزوًا، رغم أن معدل نموها لم يتغير. أظهر تحليل نشاط الجينات أن CRBN رفع مستويات CDH1 المرتبطة بالخلايا الطلائية الملتصقة بإحكام، وخفّض مستويات MMP1 المرتبطة بتفكك الأنسجة والهجرة. وبشكل مهم، تطلّبت هذه التحولات ارتباطًا مباشرًا بين CRBN و6PGD ويمكن عكسها عن طريق حجب نشاط إنزيم 6PGD، رابطين التغيرات الأيضية بتغيرات في السلوك النقائلي.
أدلة من نماذج حيوانية وسرطانات أخرى
اختبر الفريق هذه الأفكار في الفئران عن طريق حقن خلايا سرطان البروستاتا في مجرى الدم أو الطحال. الخلايا المعدّلة لإنتاج CRBN إضافي شكلت عقيدات نقيلية أقل بكثير في الكبد والرئتين مقارنةً بالخلايا الضابطة، مؤكدةً دورًا مضادًا للنقائل في الحيوانات الحية. الفئران المحرَّفة لتفتقر إلى CRBN أظهرت مستويات أعلى من بروتين 6PGD في عدة أعضاء. ظهرت أنماط مماثلة في خطوط خلايا الورم الدبقي، والرئة، والكلى: إزالة CRBN زادت 6PGD وعززت حركة وخَطِّيَّة الغزو للخلايا، بينما قيدت تثبيطات جينية أو دوائية لـ6PGD هذا السلوك العدواني. تدل هذه الملاحظات على أن كبح CRBN–6PGD للنقائل ليس فريدًا لسرطان البروستاتا.
ماذا قد يعني ذلك للعلاجات المستقبلية
بشكل عام، تقترح الدراسة أن CRBN يعمل كحارس أيضي يقيّد مصدر الطاقة اللازم لخلايا السرطان لتفكك الروابط، والهجرة، وزرع أورام جديدة. عند فقدان CRBN أو انخفاضه، يتراكم 6PGD، يرتفع إنتاج NADPH، وتصبح الخلايا أكثر احتماليةً للخضوع لتغيّرات تُفضّل النقائل. للمرضى، يشير هذا إلى احتمالين: قياس مستويات CRBN و6PGD قد يساعد في تمييز الأورام ذات خطر نقائلي مرتفع، والعلاجات التي تعزز وظيفة CRBN — أو تُخمد 6PGD بشكل انتقائي في الأورام الفقيرة في CRBN — قد تقدم طرقًا جديدة لإبطاء أو منع انتشار سرطان البروستاتا وسرطانات أخرى.
الاستشهاد: Guchhait, K., Yoon, HS., An, HS. et al. Cereblon (CRBN) inhibits prostate cancer metastasis by negatively regulating 6-phosphogluconate dehydrogenase (6PGD). Oncogene 45, 1234–1246 (2026). https://doi.org/10.1038/s41388-026-03717-9
الكلمات المفتاحية: نقائل سرطان البروستاتا, استقلاب السرطان, سيريبْلون, إنزيم 6PGD, مسار NADPH