Clear Sky Science · ar
بروتين هيليكاز الحمض النووي الريبي متعدد الوظائف DDX39A يدفع تطور الورم الأرومي الدبقي من خلال تعديل التجزؤ البديل لـ WISP1 الذي يحفز استقطاب بلعات مناعية مثبطة للمناعة
لماذا تهم هذه الدراسة المتعلقة بسرطان المخ
الورم الأرومي الدبقي هو أحد أكثر سرطانات المخ فتكًا، معروف بعودته بعد العلاج ومقاومته للأدوية. تكشف هذه الدراسة كيف أن «مفتاحًا» جزيئيًا واحدًا داخل خلايا الورم لا يساعد السرطان على النمو فحسب، بل يقنع أيضًا الخلايا المناعية المجاورة بالكف عن القتال والبدء في حماية الورم بدلًا من مهاجمته. من خلال تتبع سلسلة هذه الأحداث، يحدد الباحثون أيضًا دواءً مضادًا للذهان مستخدمًا يمكن إعادة توظيفه لتعطيل هذه الشبكة الضارة.
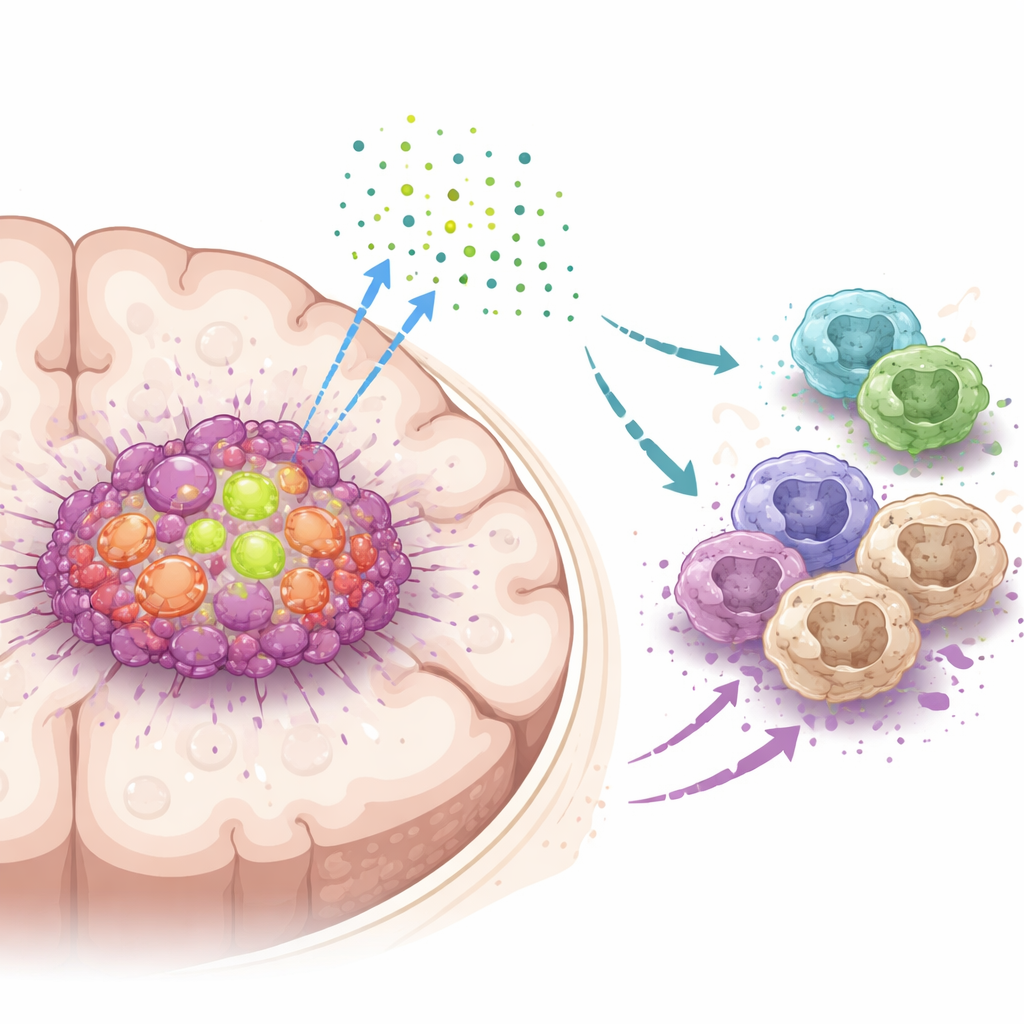
مساعد رئيسي داخل خلايا ورم المخ
ركز الفريق على بروتين يُسمى DDX39A، وهو آلية جزيئية تساعد الخلايا على معالجة الحمض النووي الريبي، النسخة العاملة من المعلومات الجينية. من خلال تحليل مجموعات بيانات كبيرة من المرضى وعينات الأورام، وجدوا أن نشاط DDX39A أعلى بكثير في الورم الأرومي الدبقي مقارنة بنسيج المخ الطبيعي، وأن مستوياته تزداد مع درجة الورم. أظهرت تحليلات الخلايا المفردة أن DDX39A وفير بشكل خاص في الخلايا الورمية سريعة الانقسام وفي بعض الخلايا المناعية المسماة البلعات داخل كتلة الورم. المرضى الذين كانت أورامهم تحتوي على مستويات أعلى من DDX39A كانوا يميلون إلى نتائج أسوأ، ما يوحي بأن هذا البروتين مرتبط ارتباطًا وثيقًا بالمرض العدواني.
كيف يغذي هذا المساعد النمو والانتشار
لاختبار وظيفة DDX39A فعليًا، استخدم الباحثون أدوات جينية لتقليله في خلايا جذعية شبيهة بالورم الأرومي الدبقي مزروعة في المختبر ونماذج أورام مخ في الفئران. عندما انخفض DDX39A، نمت خلايا الورم أبطأ، وغزت الأنسجة المحيطة بشكل أقل، وكانت أكثر عرضة للخضوع للموت المبرمج للخلايا. كما فقدت الخلايا الجذعية الشبيهة بالورم الكثير من قدرتها على تكوين كرات ورمية جديدة، وهو علامة على تراجع قدرتها على التجدد الذاتي. في الفئران، كانت الأورام ذات مستويات منخفضة من DDX39A أصغر وعاشت الحيوانات لفترة أطول، مما يؤكد أن هذا البروتين يدفع تقدم الورم بنشاط وليس مجرد علامة عليه.
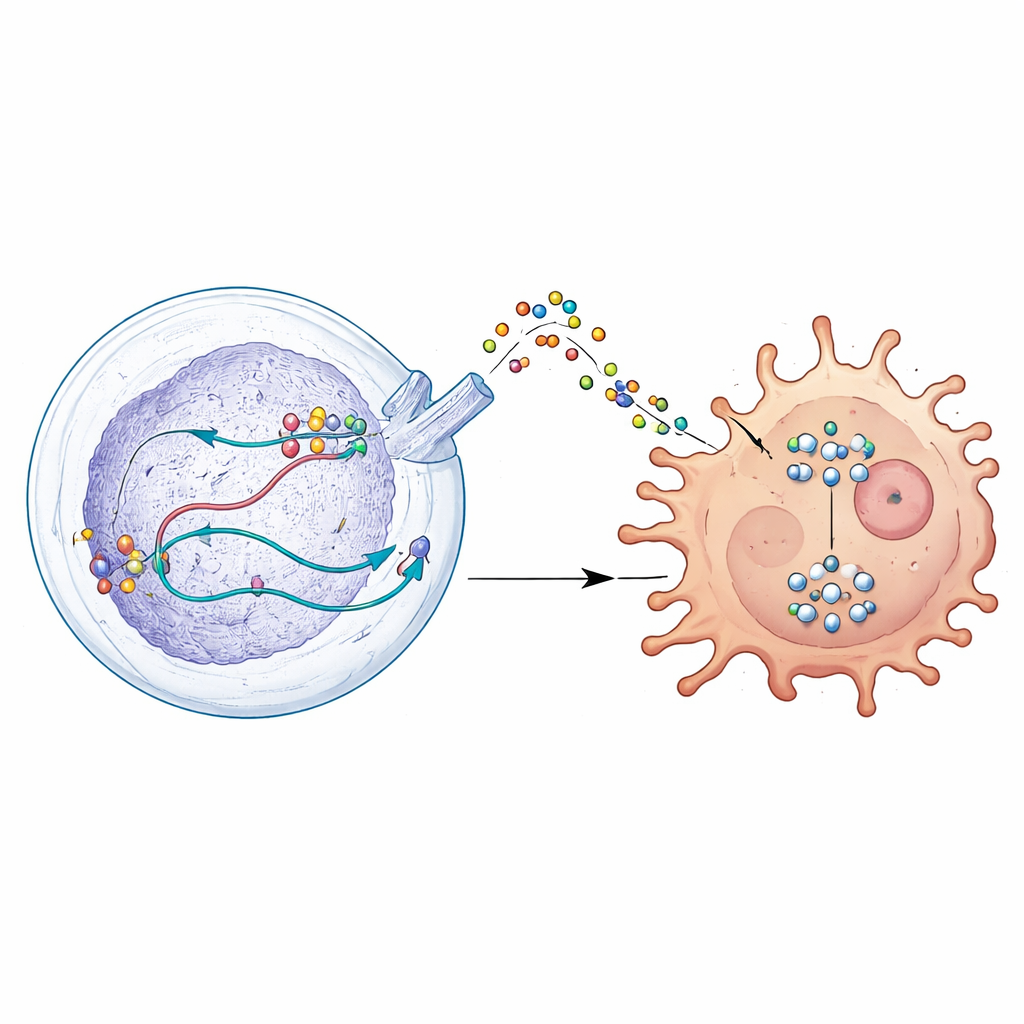
إشارة سرية تعطل المدافعين المناعيين
بالتعمق أكثر، اكتشف العلماء أن DDX39A يغير كيفية معالجة جين يسمى WISP1. بدلاً من مجرد تشغيل WISP1 أو إيقافه، يساعد DDX39A في تشكيل حمضه النووي الريبي بطريقة تثبت الرسالة وتزيد إنتاج بروتين WISP1. ثم تطلق خلايا الورم WISP1 إلى محيطها، حيث يتصرف كمنارة مضللة مزعجة. تستجيب البلعات المجاورة—التي يمكن أن تهاجم الأورام أو تدعمها—لهذه الإشارة بالتحول إلى حالة مثبطة للمناعة وتساعد الورم. يقود هذا التحول تنشيط مسار تحكم في النمو داخل الخلايا يعرف باسم AKT. عندما تم تقليل DDX39A أو WISP1، هدأ هذا المسار، أصبحت خلايا الورم أقل عدوانية، وعادت البلعات إلى نمط أقرب إلى محاربة الورم.
تحويل دواء نفسي إلى سلاح ضد السرطان
مسلحين بخريطة هذا المسار، بحث الباحثون في قواعد بيانات الأدوية عن جزيئات قد تعيق نشاط DDX39A. استقروا على فلوفينا زين، دواء مضاد للذهان مستخدم منذ زمن طويل ويُعرف بقدرته على الوصول إلى المخ. أظهرت نمذجة حاسوبية واختبارات الارتباط أن الفلوفينا زين يمكن أن يرتبط مباشرة بـ DDX39A. في خلايا الورم، أضعف الدواء تماسك DDX39A مع حمض WISP1 الريبي، وخفض مستويات WISP1، وقلل إشارة AKT. خلقت الخلايا المعالجة حالة نمو أقل، غزت أقل، كونت كرات ورمية أقل، وكانت أكثر ميلاً للموت. في نماذج الفئران، أبطأ الفلوفينا زين نمو أورام المخ، وقلل عدد البلعات المساعدة للورم، ووسع البقاء على قيد الحياة، وكل ذلك بجرعات مماثلة لتلك المستخدمة بالفعل لدى البشر لحالات أخرى.
ماذا يعني هذا للعلاج المستقبلي
بعبارات بسيطة، تُظهر هذه الدراسة أن خلايا الورم الأرومي الدبقي تستغل DDX39A لضبط رسالة (WISP1) تعمل على زيادة صمودها وإعادة برمجة الخلايا المناعية المجاورة لتصبح حراسًا بدلاً من محاربين. إن حجب هذا المساعد، سواء جينيًا أو بدواء مثل الفلوفينا زين، يضعف السرطان على جبهتين: خلايا الورم نفسها ودرع البلعات المثبطة للمناعة. وبينما هناك حاجة إلى اختبارات أكثر بكثير قبل أن يصل هذا الإجراء إلى المرضى، تفتح الدراسة طريقًا واعدًا لإعادة توظيف دواء مألوف لضرب نقطة ضعف جديدة مكشوفة في أحد أكثر سرطانات المخ عنادًا.
الاستشهاد: Zhang, Y., Xue, Z., Zhang, N. et al. The multifunctional RNA helicase DDX39A drives glioblastoma progression by modulating WISP1 alternative splicing that induces an immunosuppressive macrophage polarization. Oncogene 45, 1026–1041 (2026). https://doi.org/10.1038/s41388-026-03715-x
الكلمات المفتاحية: الورم الأرومي الدبقي, تجزؤ الحمض النووي الريبي, البيئة الدقيقة للورم, استقطاب البلعات, إعادة توظيف الأدوية