Clear Sky Science · ar
PMM2 يتفاعل مع TRIM28 لتجنيد E2F4 وتعزيز التحلل الجلوتيك الذي يتوسطه KIFC3 وتقدّم سرطان القولون والمستقيم
لماذا تهم هذه القصة السرطانية
سرطان القولون والمستقيم هو واحد من أكثر السرطانات فتكًا في العالم، ويرجع ذلك جزئيًا إلى أن العديد من الأورام تتعلم كيف تختطف نظم الطاقة في الجسم لتغذية نمو لا يمكن السيطرة عليه. تكشف هذه الدراسة كيف يساعد إنزيم غير معروف جيدًا، PMM2، أورام القولون والمستقيم على حرق السكر بشكل أكثر عدوانية والانتشار، ولماذا يجعل ذلك منه هدفًا واعدًا للأدوية والاختبارات التشخيصية المستقبلية.
محرك ورمي جائع للسكر
غالبًا ما تعيد الخلايا السرطانية برمجة طريقة استخدامها للجلوكوز، مفضلة شكلًا عالي السرعة ومنخفض الكفاءة من حرق السكر يُعرف بالتحلل الجلوتيك. بدأ الباحثون بمقارنة آلاف الجينات في عينات أورام القولون والمستقيم مع الأنسجة السليمة المجاورة. برزت PMM2، وهو إنزيم يساهم عادة في ربط سلاسل السكر بالبروتينات، كواحدة من الجينات التي ازداد تعبيرها بشكل ملحوظ في السرطان. الخلايا الورمية التي بها مستويات إضافية من PMM2 نمت أسرع، شكلت مستعمرات أكثر، وانتشرت بسهولة أكبر في أطباق المختبر، بينما تباطأ نمو الخلايا التي تم تعطيل PMM2 فيها، وهجرت أقل، وكانت أكثر عرضة للموت.
كيف تعزز الخلايا الورمية استخدام السكر
عندما خفض الفريق مستويات PMM2 في خلايا سرطان القولون والمستقيم، أخذت الخلايا جلوكوزًا أقل، أنتجت ATP أقل (عملة الطاقة الرئيسية لديها)، وأطلقت لاكتات أقل، وهو ناتج فضلات التحلل الجلوتيك. أكدت قياسات أيضية حساسة أن الحموضة العامة للوسط المحيط انخفضت، بينما زاد استخدام الأكسجين، ما يعني أن الخلايا انتقلت بعيدًا عن التحلل الجلوتيك المعجل نحو التنفس الأكسجيني الأكثر طبيعية. كما انخفضت البروتينات المساعدة الرئيسية في التحلل الجلوتيك، PKM2 وLDHA. والمفاجئ أن نسخة من PMM2 معطلة كيميائيًا (عديمة النشاط التحفيزي) كانت لا تزال قادرة على دفع هذا السلوك الجائع للسكر، ما يدل على أن دور الإنزيم في السرطان لا يعتمد على نشاطه الكيميائي المعتاد، بل على الشركاء الذين يرتبط بهم داخل الخلية.
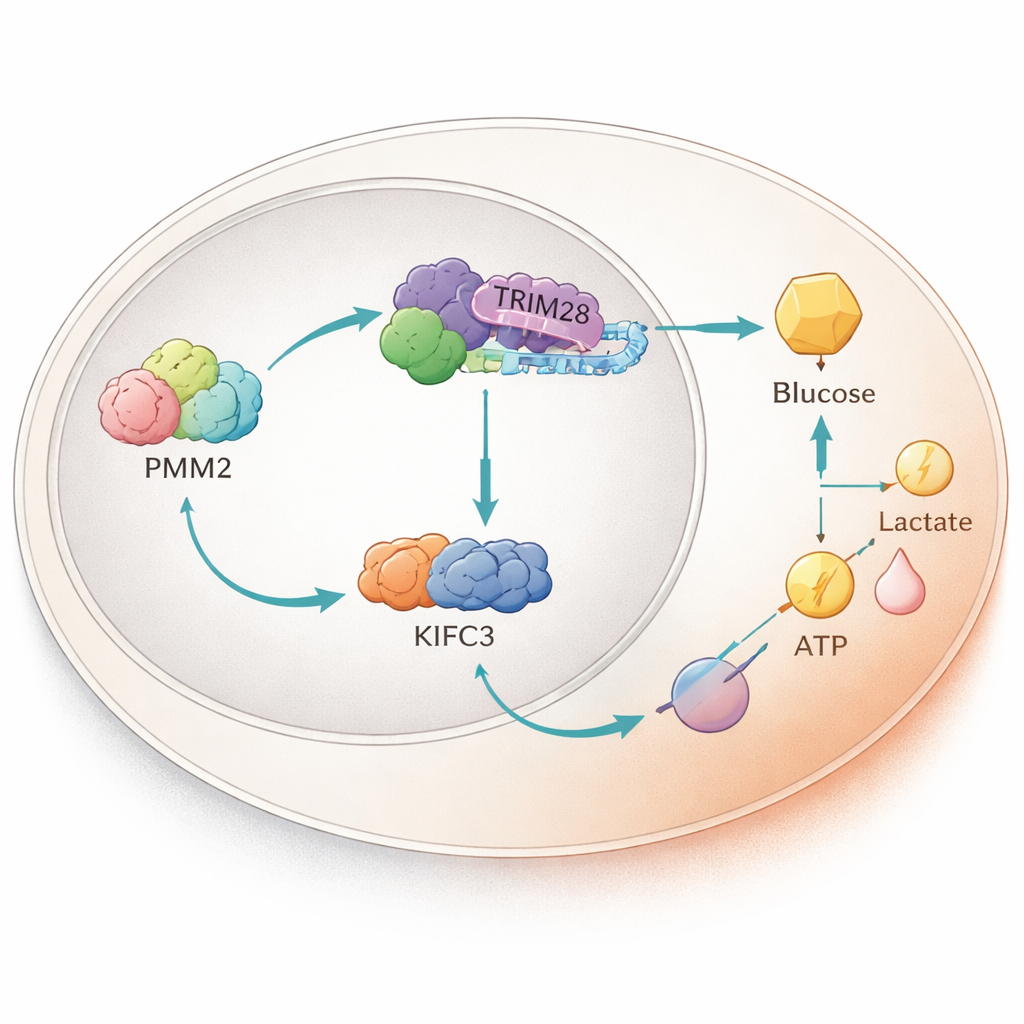
تتابع بروتيني داخل النواة
عند التعمق أكثر، وجد العلماء أن PMM2 يرتبط فعليًا ببروتين آخر يُدعى TRIM28، والذي يمكنه الانتقال إلى نواة الخلية والتأثير على نشاط الجينات. يساعد PMM2 على تراكم TRIM28 في النواة، حيث يتعاون TRIM28 مع عامل نسخ، E2F4. معًا، يعززون إنتاج بروتين ناقل يُدعى KIFC3 عن طريق الارتباط بمقطع محدد من منطقة التحكم في دنا هذا الجين. التجارب التي حذفت أجزاء من PMM2 اللازمة لارتباطه بـTRIM28 ألغت قدرة PMM2 على زيادة التحلل الجلوتيك ونمو الخلايا، ما يبرز أن شراكة هذه البروتينات — وليس وظيفة PMM2 الإنزيمية الكلاسيكية — هي ما يمنح الورم هذه الميزة.
تشغيل مفتاح أيضي مهم
تبين أن KIFC3، المعروف أكثر بدوره في نقل الحمولات عبر الهيكل الداخلي للخلية، هو مفتاح أيضي حاسم. عندما خفض الباحثون مستويات KIFC3، استهلكت خلايا سرطان القولون والمستقيم جلوكوزًا أقل، أنتجت ATP ولاكتات أقل، وأظهرت نشاطًا تحلليًا أضعف، بينما زاد استخدام الأكسجين. والأهم من ذلك، أن إسكات KIFC3 ألغى جزئيًا الزيادة في التحلل الجلوتيك والميزة النمائية التي يسببها عادة PMM2. في فئران نُغرت بخلايا سرطان القولون والمستقيم البشرية، نمت الأورام التي تحتوي على PMM2 إضافي أكبر، لكن هذا التأثير تقلص عندما تم خفض KIFC3. أظهرت عينات الأورام من هذه الحيوانات مستويات أعلى من PMM2 وKIFC3 وعلامات التحلل الجلوتيك، مما يربط سلسلة الأحداث هذه في نسيج حي.
من نماذج المختبر إلى عينات المرضى
للتقريب بين العمل والعيادة، أنشأ الفريق أورامًا ثلاثية الأبعاد مصغرة، تُعرف بالأورجانويد، من سرطانات القولون والمستقيم للمرضى. نمَت الأورجانويدات ذات المستويات الأعلى من PMM2 وKIFC3 أسرع وأنتجت ATP ولاكتات أكثر من تلك ذات المستويات الأدنى. إجبار الأورجانويدات على إنتاج مزيد من PMM2 زاد KIFC3 والتحلل الجلوتيك، بينما أدى خفض PMM2 إلى التأثير المعاكس. أظهرت تحليلات مصفوفات أورام المرضى أيضًا أن المستويات العالية من PMM2 ارتبطت بمرض أكثر تقدمًا، وانتشار للعقد اللمفاوية، وبقاء إجمالي أقصر، مما يجعل PMM2 مرشحًا قويًا كمؤشر حيوي.
ماذا يعني هذا للرعاية المستقبلية
بعبارات بسيطة، تُظهر هذه الدراسة أن العديد من أورام القولون والمستقيم يبدو أنها توصل PMM2 إلى تتابع بروتيني نووي — عبر TRIM28 وE2F4 — لرفع مستوى KIFC3 وبالتالي نظامها المحرق للسكر. تساعد هذه الزيادة الأيضية السرطانات على النمو والانتشار. وبما أن هذا المسار يعتمد على تفاعلات البروتين بدلاً من وظيفة PMM2 الإنزيمية المعتادة، فإنه يفتح آفاقًا جديدة للعلاج: يمكن أن تعمل جزيئات صغيرة، ببتيدات، أو أدوية المحلل (degrader) التي تعطل ارتباط PMM2 بـTRIM28، تمنع وصول E2F4 إلى الدنا، أو تخفف نشاط KIFC3، كلها — من حيث المبدأ — على تجويع الأورام من وقودها المفضّل. على الرغم من أن مثل هذه العلاجات غير متاحة بعد، فإن سلسلة PMM2–TRIM28–E2F4–KIFC3 تبرز الآن كخريطة طريق واعدة لاستراتيجيات أكثر دقة وتركيزًا على الأيض ضد سرطان القولون والمستقيم.
الاستشهاد: Peng, Z., Ma, B., Song, Z. et al. PMM2 interacts with TRIM28 to recruit E2F4 and promote KIFC3-mediated tumor glycolysis and colorectal cancer progression. Oncogene 45, 1145–1160 (2026). https://doi.org/10.1038/s41388-026-03707-x
الكلمات المفتاحية: سرطان القولون والمستقيم, أيض الورم, التحلل الجلوتيك, إشارات مسرطنة, مؤشر حيوي