Clear Sky Science · ar
يحسّن ULK1 التقدّم النقائلي في نماذج تجريبية لسرطان المبيض الظهاري
لماذا يهم هذا البحث
غالباً ما يُكتشف سرطان المبيض الظهاري بعد أن يكون قد انتشر بهدوء داخل البطن، ما يجعله واحداً من أكثر السرطانات فتكاً لدى النساء. خطوة رئيسية في هذا الانتشار هي تكوّن مجموعات صغيرة من الخلايا السرطانية، تُسمى الكُرَيّات (spheroids)، التي تطفو في سائل البطن، وتنجو من العلاج الكيميائي، وتؤسس أوراماً جديدة. يطرح هذا البحث سؤالاً محدداً بتبعات كبيرة: هل يساعد «مفتاح بقاء» خلوي يُدعى ULK1 هذه التجمعات على الصمود والانتشار، وهل قد يفتح تعطيله طرقاً جديدة لعلاج سرطان المبيض المتقدّم؟
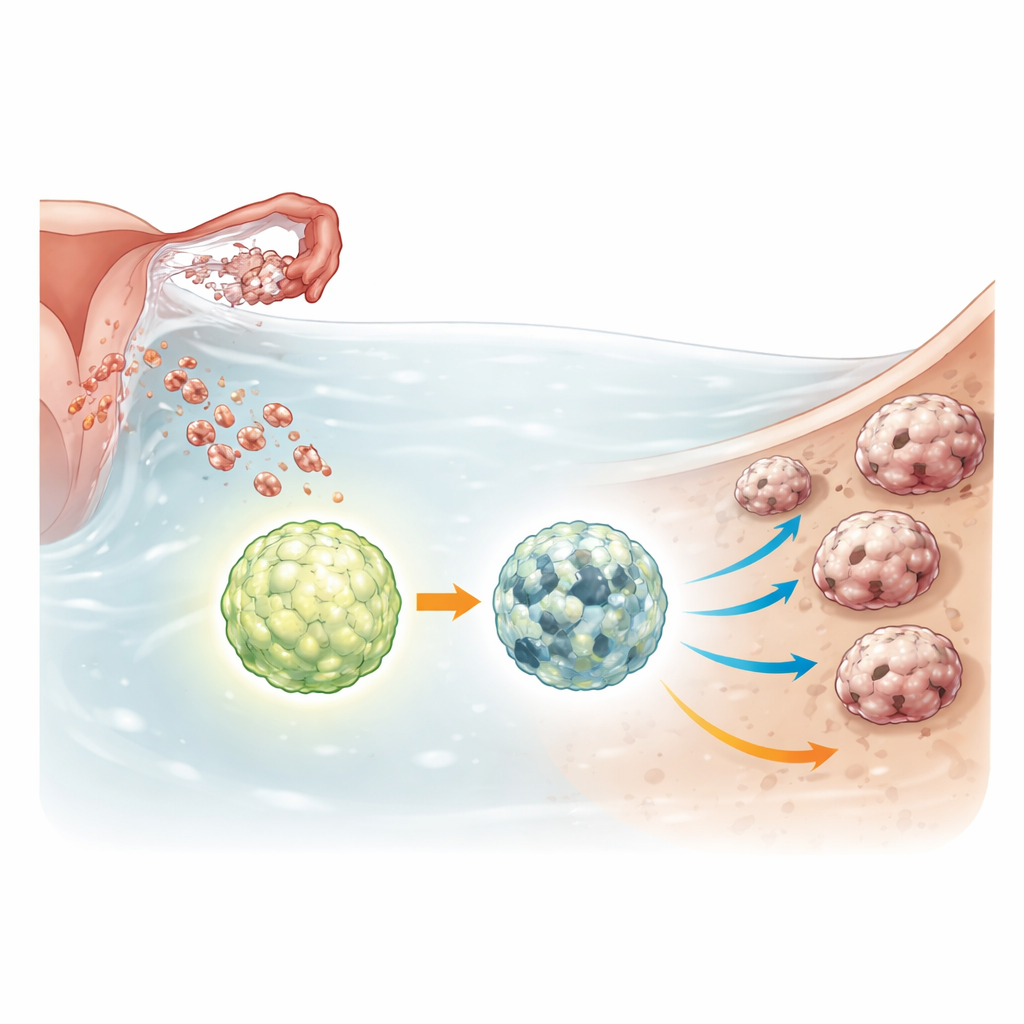
مفتاح بقاء داخل عناقيد الخلايا السرطانية
تواجه كُرَيّات سرطان المبيض ظروفاً قاسية: قِلّة المغذيات، فقدان الالتصاق، والتعرّض للعلاج الكيميائي. للتكيّف، تزيد من عملية إعادة التدوير الخلوية المعروفة بالالتهام الذاتي، التي تُحلّل مكونات داخلية وتعيد توظيفها لإبقاء الخلايا على قيد الحياة تحت الضغط. يُعد ULK1 مفتاحاً رئيسياً يشغّل هذا النظام. استخدم الباحثون أدوات تحرير الجينات لحذف ULK1 تماماً من عدة خطوط خلايا لسرطان المبيض ومن خط خلوي غير سرطاني من قناة فالوب يمثل المراحل المبكرة ما قبل السرطان. ثم قارنوا سلوك الخلايا الطبيعية ونظائرها الناقصة لـ ULK1 عند زراعتها ككُرَيّات طافية أو كأورغانويدات ثلاثية الأبعاد تشبه أوراماً صغيرة.
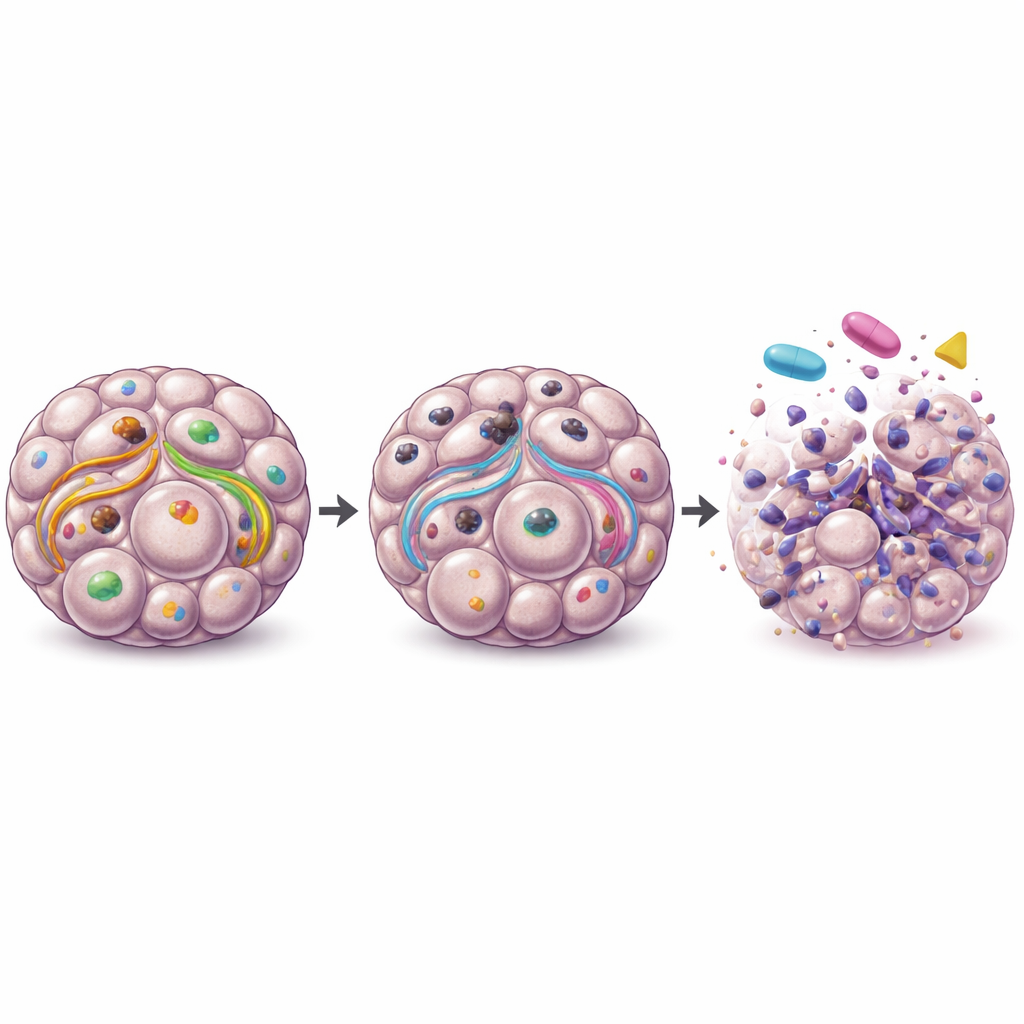
ماذا يحدث عندما يُطفأ المفتاح
عند حذف ULK1 في خلايا سرطان المبيض، تَعَطّلت بشكل قاطع قدرتها على إجراء الالتهام الذاتي داخل الكُرَيّات، كما أظهرت تغييرات في بروتينات إعادة التدوير الرئيسية. احتوت هذه الكُرَيّات الخالية من ULK1 على خلايا حية أقل وأظهرت علامات متزايدة للموت المبرمج للخلايا، مما يشير إلى أن تجمعات السرطان لم تعد قادرة على تحمل الظروف القاسية بفعالية. من المثير للاهتمام أن إزالة ULK1 من الخلايا السليمة السابقة للسرطان لم تقم بإيقاف نظام إعادة التدوير لديها بنفس الدرجة، ما يوحي بأن الخلايا السرطانية أعتمد أكثر على ULK1 مقارنة بنظيراتها الصحية. يجعل هذا الاعتماد الخاص بالسرطان ULK1 هدفاً علاجياً جذاباً.
إبطاء الانتشار وإضعاف مواقع الورم
إلى جانب البقاء في الحالة العائمة، يجب على الكُرَيّات أن تلتصق وتغزو بطانة البطن الملساء لتشكيل أورام جديدة. باستخدام نماذج مخبرية تحاكي هذه الخطوة المبكرة من النقائل، بيّن الفريق أن الكُرَيّات الناقصة ULK1 كانت أضعف بكثير في دفع وإخلال طبقة الخلايا الميزوثيلية التي تبطن عادةً الأعضاء البطنية. عندما نمت خلايا السرطان الخالية من ULK1 كأورغانويدات مدمجة في مصفوفة شبيهة بالهلام، شكّلت أيضاً هياكل ورمية أصغر وأقل قوة. في نماذج فأرية حيث حُقنت خلايا سرطان المبيض البشرية في التجويف البطني، أدت خسارة ULK1 إلى ترسّب أورام أقل وكمية سائل بطني أقل، وهما علامتان لتقدّم المرض، رغم أن البقاء العام للحيوانات لم يتحسن.
إضعاف إشارات رئيسية وتعزيز تأثيرات أدوية موجهة
لفهم كيف يدعم ULK1 السرطان بخلاف دوره في إعادة التدوير، خرّط الباحثون التغيرات البروتينية في الكُرَيّات الخالية من ULK1. وجدوا أن طرق النمو والبقاء الكبرى داخل الخلية — خصوصاً مسارات MEK–MAPK وPI3K–AKT–mTOR — اختلت. هذه المسارات تساعد الخلايا السرطانية عادة على مقاومة الموت والاستمرار في الانقسام. عندما عالج الفريق الكُرَيّات الناقصة ULK1 بأدوية تثبط MEK أو mTOR، أصبحت التجمعات السرطانية أكثر عرضة بكثير، مع تراجع حاد في الحيوية وقدرة الالتصاق من جديد. بالمقابل، لم يجعل حذف ULK1 أدوية العلاج الكيميائي القياسية مثل الكاربوبلاتين أو باكليتاكسيل أو مثبط PARP أولاباريب تعمل بشكل أفضل، وفي بعض الظروف بدا أنه يقلل من فائدتها.
قرائن من أورام المرضى ونماذج مرضى مصغرة
بالنظر إلى مجموعات بيانات عامة كبيرة لأورام المبيض، وجد المؤلفون أن نشاط جين ULK1 الأعلى رُبط ببقاء طويل الأمد أسوأ وكان مرتفعاً بشكل خاص في العينات النقيلية مقارنة بالأورام الأولية والنسيج الطبيعي. وللاقتراب من التطبيق السريري، اختبروا حبة سريرية حابسة لـ ULK1 تُدعى DCC-3116 على أورغانويدات مشتقة من مرضى نمت من عينات أورام نقيليّة. في مجموعة فرعية من هذه النماذج المأخوذة من المرضى، خفضت حجب ULK1 وحده، أو استخدام أدوية MEK أو mTOR منفردة، بقاء الأورغانويدات، على الرغم من أن الجمع بين العوامل لم يضف فائدة متسقة. كانت أورغانويدات مرضى أخرى مقاومةً لجميع العلاجات، مما يبرز التنوع الكبير لسرطانات المبيض والحاجة إلى مؤشرات حيوية لتحديد من قد يستفيد.
ماذا يعني هذا لرعاية المستقبل
تجمع النتائج معاً لتصوّر ULK1 كمساعد مركزي لانتشار سرطان المبيض: فهو يغذي إعادة التدوير الداخلي التي تحافظ على حياة كُرَيّات السرطان، ويدعم قدرتها على غزو مواقع جديدة، ويساهم في الحفاظ على إشارات نمو قوية. يؤدي إيقاف ULK1 إلى إضعاف هذه العمليات، وتصغير الأورام التجريبية، وجعل تجمعات الخلايا السرطانية أكثر حساسية لبعض الأدوية الموجهة، وإن لم يكن للعلاج الكيميائي القياسي. بالنسبة للمرضى، يقترح هذا العمل أن ULK1 قد يصبح جزءاً من استراتيجية الطب الدقيق — خصوصاً لمن لديهم أورام نقيليّة عالية التعبير عن ULK1 — حيث تُدمَج مثبطات ULK1 مع مُعَطِّلات MEK أو mTOR للحد من نمو الورم وانتشاره، بشرط أن تُجرى اختبارات دقيقة لتحديد الأورام الأكثر احتمالاً للاستجابة.
الاستشهاد: Webb, J.D., Buensuceso, A., Tomas, E.J. et al. ULK1 promotes metastatic progression in experimental models of epithelial ovarian cancer. Oncogene 45, 1111–1127 (2026). https://doi.org/10.1038/s41388-026-03702-2
الكلمات المفتاحية: سرطان المبيض, النقائل, الالتهام الذاتي, ULK1, العلاج الموجَّه