Clear Sky Science · ar
YEATS2 يعزز إصلاح الحمض النووي ويحدث مقاومة للانتحار الخلوي الناجم عن الانفصال عبر زيادة نفاذية الكروماتين لدفع نقائل سرطان البروستاتا
لماذا تهم الخلايا السرطانية التي ترفض الانفصال
عندما ينتشر السرطان من موضعه الأصلي إلى أعضاء بعيدة، يصبح العلاج أصعب بكثير. سرطان البروستاتا ليس استثناءً: بمجرد أن يزرع أورامًا جديدة في العقد اللمفاوية أو العظام، ينخفض معدل البقاء على قيد الحياة بشكل حاد. للانتشار، يجب على الخلايا الورمية أولاً الانفصال عن نسيجها الأصلي والدخول إلى الأوعية الدموية أو اللمفاوية. تموت معظم هذه الخلايا المتجولة، لكن قلة خطيرة تكتسب القدرة على مقاومة هذا النوع من موت الخلايا المحفز بالانفصال، وهي عملية تسمى الأونويكس. تكشف هذه الدراسة كيف يساعد بروتين يسمى YEATS2 خلايا سرطان البروستاتا على النجاة في تلك الرحلة المحفوفة بالمخاطر من خلال تعزيز قدرتها على إصلاح تلف الحمض النووي.
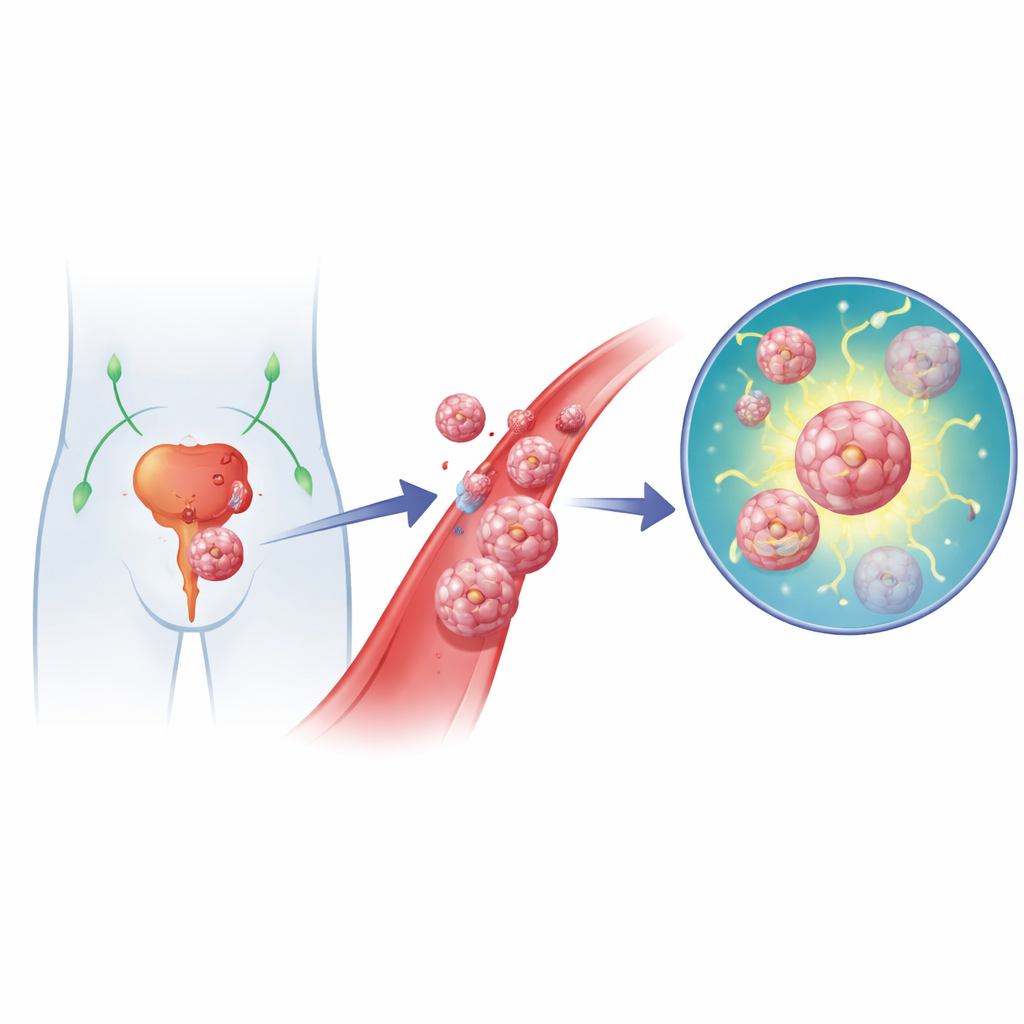
الخلايا في حالة حركة
بدأ الباحثون بسؤال ما الذي يميز أورام البروستاتا المنقولة مقارنة بالنُسخ الأولية منها. قارَنوا بيانات جينية من قواعد بيانات سرطانية عامة مع تجاربهم الخاصة على خلايا سرطان البروستاتا التي جرى دفعها للنجاة دون ارتباط، محاكاةً لظروف المرور في مجرى الدم. عبر عينات المرضى والخلايا المزروعة معملًا، برزت مجموعة صغيرة من الجينات باستمرار على أنها متغيرة في الخلايا المنقولة والمقاومة للأونويكس. من بينها، أظهر YEATS2 زيادة تعبير قوية وارتباطًا وثيقًا بنتائج سيئة: الرجال الذين كانت أورامهم تحتوي على مزيد من YEATS2 كانوا يميلون إلى قصر مدة البقاء وتقدّم المرض المبكّر.
اختبار مشتبه به
لفحص دور YEATS2، بنى الفريق نماذج فئران لانتشار إلى العقد اللمفاوية عبر حقن خلايا سرطان البروستاتا في أخمص أقدام الحيوانات وجمع كل من الأورام الأولية والعقد اللمفاوية الركبية المجاورة لاحقًا. كانت الخلايا المأخوذة من نقائل العقد اللمفاوية أفضل في البقاء في حالة تعليق، والتنقل، والغزو مقارنة بنظيراتها من الورم الأصلي. كما حملت هذه الخلايا المنقولة مستويات أعلى من YEATS2. عندما زاد العلماء اصطناعيًا مستوى YEATS2 في خلايا سرطان البروستاتا، أصبحت الخلايا أصعب في القتل بعد الانفصال وأكثر قدرة على الهجرة والغزو في اختبارات المعمل. أدى خفض YEATS2 إلى تأثير معاكس وقلل بشكل حاد نقائل العقد اللمفاوية في الفئران.
إصلاح الحمض النووي كخدعة للبقاء
يؤدي الانفصال عن النسيج المحيط إلى إجهاد الخلايا السرطانية، جزئيًا عن طريق زيادة جزيئات ضارة تتلف الحمض النووي. باستخدام علامات لكسور الحمض النووي، أظهر المؤلفون أن الخلايا العائمة في التعليق تتراكم فيها إصابات حمض نووي أكثر، لا سيما إذا كانت مأخوذة من الأورام الأولية بدلاً من المنقولة. قللت زيادة التعبير عن YEATS2 هذا التلف، بينما زاد صمت YEATS2 الضرر وأضعف البقاء في حالة تعليق. كشفت تحليلات إضافية لمجموعات بيانات مرضى كبيرة أن الجينات المرتبطة باستجابة وإصلاح تلف الحمض النووي كانت مرتبطة بقوة بنشاط YEATS2. وبرز جين إصلاح واحد، RAD50، كشريك رئيسي: فقد كان معبرًا عنه بكثرة في الخلايا المنقولة والمقاومة للأونويكس، وارتفع عندما زاد YEATS2، وساعد على استعادة البقاء عندما أعيد إدخاله في خلايا ناقصة YEATS2.
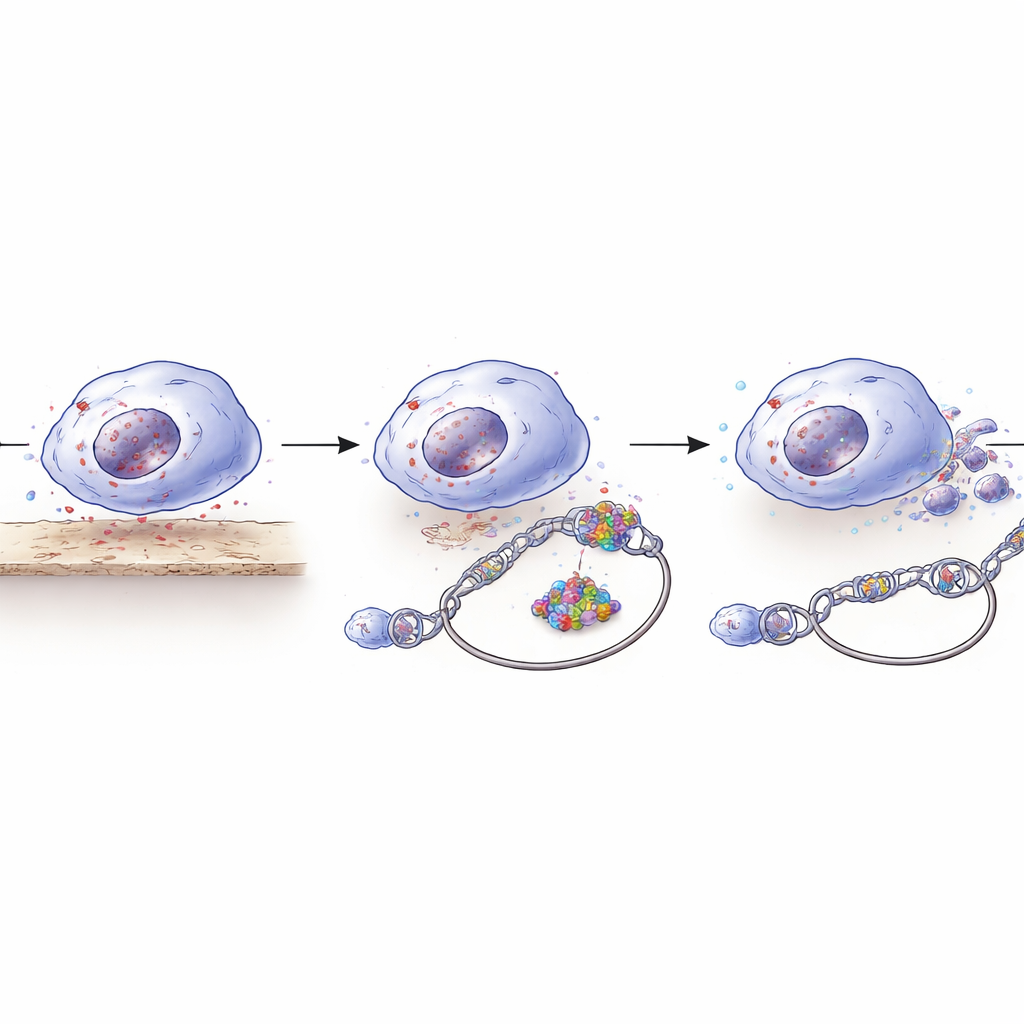
فتح إشارات مرجعية للحمض النووي
كيف يرفع YEATS2 مستوى RAD50؟ ينتمي YEATS2 إلى مركب بروتيني يغير مدى إحكام تغليف الحمض النووي، مما يجعل جينات معينة أكثر أو أقل سهولة للقراءة. استخدم الفريق تقنية ترسم خرائط المقاطع «المفتوحة» مقابل «المغلقة» من الحمض النووي ووجدوا أن YEATS2 جعل منطقة محفز RAD50 أكثر نفاذية. عند هذا الجزء المرتخي من الحمض النووي، تعرف YEATS2 على وسم كيميائي على بروتينات الهيستون (أستلة H3K27) ومن خلال نطاق YEATS المتخصص فيه ساعد في جذب علامات أستلة إضافية على مواضع مجاورة. عملت هذه التغيرات كفتح صفحة مؤشرة وتظليل فقرة، مما أتاح لعامل النسخ NR2C2 أن يرتبط بكفاءة أكبر ويحفز إنتاج RAD50. شكل YEATS2 وNR2C2 دائرة مؤيدة للبقاء عززت قدرة الإصلاح بالضبط عندما كانت الخلايا المنفصلة بحاجة إليها أكثر.
حجب طريق الهروب
لأن RAD50 جزء من مركب MRN، الآلية الأساسية لإصلاح الكسور المزدوجة الخطرة في الحمض النووي، فحص العلماء ما إذا كان تعطيل هذه الآلية قد يقلل من النقائل. استخدموا ميرين (Mirin)، جزيء صغير يثبط مركب MRN، وخفضوا أيضًا مستويات أحد شركاء RAD50، MRE11. زادت كلتا الاستراتيجيتين تلف الحمض النووي وقللتا من قدرة خلايا سرطان البروستاتا على استعمار الرئتين أو العقد اللمفاوية في الفئران، حتى عندما كان RAD50 وافرًا. تشير هذه النتائج إلى أن سرطان البروستاتا المنقول يعتمد اعتمادًا كبيرًا على تعزيز إصلاح الحمض النووي ليبقى حيًا أثناء الانفصال والسفر.
ماذا يعني هذا للمرضى
بعبارات بسيطة، تُظهر هذه الدراسة أن بعض خلايا سرطان البروستاتا تفلت من الموت عبر تعلم رقع حمضها النووي بشكل أكثر فعالية خلال أخطر مرحلة في رحلتها: عندما تنكسر وتبتعد عن موطنها الأصلي. يعمل YEATS2 كمسهل جزيئي، يفتح الصفحات الصحيحة من كتاب التعليمات الجينية حتى يمكن إنتاج RAD50 وشركائه في الإصلاح بكميات كبيرة. يتيح هذا الإصلاح المعزز للخلايا الخارجة أن تتحمل السفر في مجرى الدم أو الجهاز اللمفاوي دون الموت، مما يزيد فرص تكوين أورام جديدة. لذا قد يوفر استهداف مسار YEATS2–NR2C2–RAD50، أو مركب إصلاح MRN الذي يغذيه، طرقًا جديدة لوقف انتشار سرطان البروستاتا وتحسين النتائج للرجال المصابين بمرض متقدم.
الاستشهاد: Li, H., Song, Y., Cong, Y. et al. YEATS2 promotes DNA repair and induces anoikis resistance by enhancing chromatin accessibility to drive prostate cancer metastasis. Oncogene 45, 971–988 (2026). https://doi.org/10.1038/s41388-026-03696-x
الكلمات المفتاحية: نقائل سرطان البروستاتا, إصلاح الحمض النووي, مقاومة الانتحار الخلوي (أونويكس), نفاذية الكروماتين, RAD50