Clear Sky Science · ar
تسهيل O-GlcNAcylation لبروتين POM121 لنقائل العظم في سرطان الرئة غير صغير الخلايا عبر تعزيز استيراد c-MYC النووي وإعادة برمجة ECM
لماذا يهم هذا البحث
عندما ينتشر سرطان الرئة إلى العظام يسبب ألماً شديداً وكسرًا ويقصر العمر بشكل حاد، ومع ذلك لا تزال لدى الأطباء أدوات محدودة لإيقاف هذه المطاف المميت. يغوص هذا البحث في الآليات الداخلية لخلايا سرطان الرئة ليكشف كيف تكتسب بعض الخلايا ميزة خاصة تتيح لها الانتقال من الرئة إلى العظم والازدهار هناك. من خلال تتبُّع هذه العملية حتى تغييرات دقيقة على بروتين بوّاب وحيد عند حافة نواة الخلية، يحدد المؤلفون سلسلة جديدة من الأحداث التي قد تُستغل للتنبؤ بنقائل العظم أو الوقاية منها أو علاجها لدى مرضى سرطان الرئة غير صغير الخلايا.
علامة سكرية تغير سلوك السرطان
ركز الباحثون على التعديلات التالية للترجمة، وهي تغييرات كيميائية صغيرة تطرأ على البروتينات بعد تصنيعها. أحد هذه التعديلات، المسمّى O-GlcNAcylation، هو ربط سكر صغير بمواقع محددة على البروتينات. باستخدام خطوط خلايا سرطان الرئة ونماذج فئران، قارن الفريق خلايا الورم العادية مع مجموعات فرعية تم اختيارها تكرارًا لقدرتها على استعمار العظام. وجدوا أن هذه الخلايا الباحثة عن العظم كانت تملك مستويات أعلى بكثير من O-GlcNAcylation، مدفوعة بزيادة نشاط إنزيم OGT الذي يركب العلامة السكرية. من بين مئات البروتينات المعدَّلة برز بروتين واحد: POM121، مكوّن أساسي من مسام النواة، البنية التي تتحكم في حركة المواد داخل النواة وخارجها.
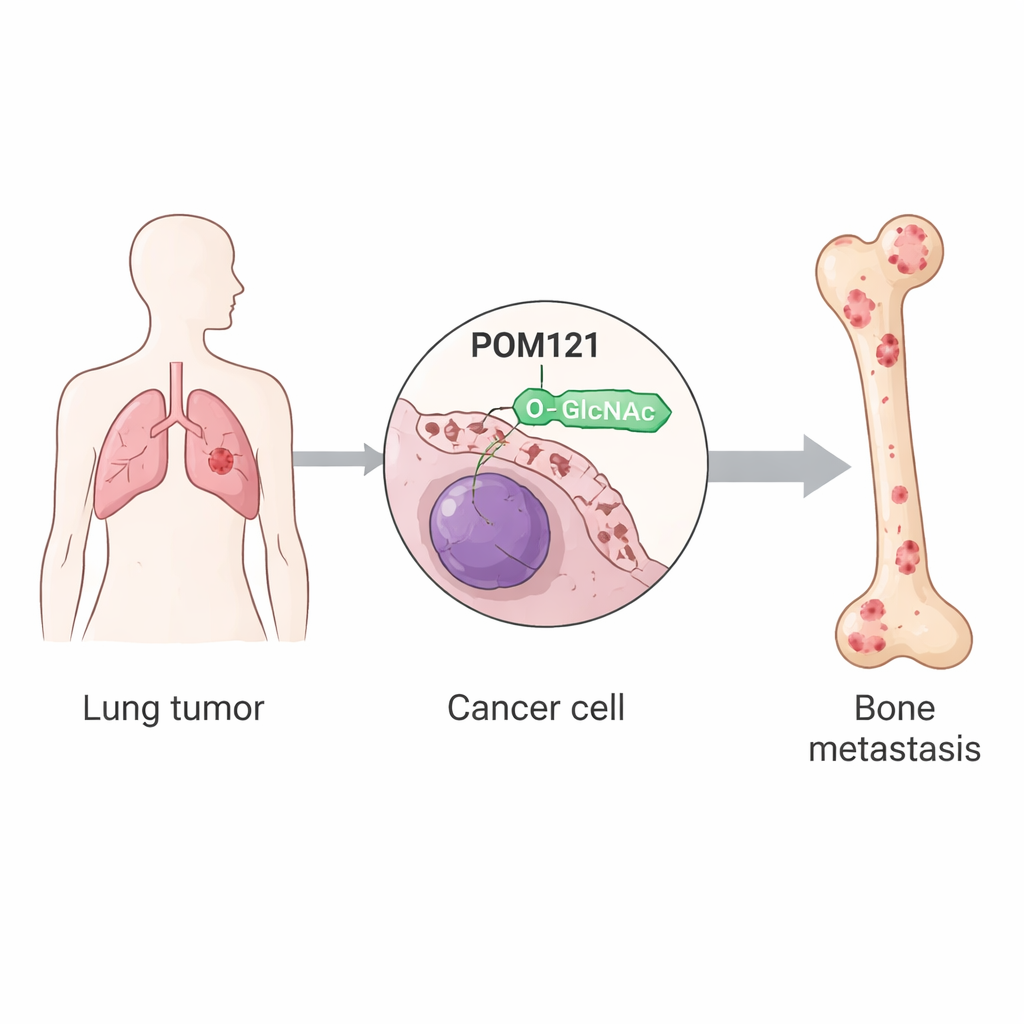
بوّاب النواة POM121 يتثبّت
يموضع POM121 في الغشاء المحيط بالنواة، ويشكّل جزءًا من القناة التي يجب أن تمر عبرها العديد من بروتينات الإشارة. في خلايا سرطان الرئة المسببة لنقائل العظم، حمل POM121 حمولة كبيرة من O-GlcNAc في موضع أميني واحد يُسمى السيرين 199. عندما غيّر الباحثون هذا الموقع بحيث لا يمكن تعديله، أصبح البروتين غير مستقر وتكسّر بسرعة بواسطة آليات التخلص الخلوية. تظهر الدراسة أن العلامة السكرية تحمي POM121 من أن يُعلَّم للتدمير بواسطة إنزيم يُدعى TRIM21، الذي يعلّق عادةً ملصقات اليوبكويتين "للتخلص". بوجود O-GlcNAc، لا يرتبط TRIM21 جيدًا، فتقل اليوبكويتينة ويتراكم POM121 في مسام النواة دون تغيير موضعه.
فتح الباب لسائق قوي للسرطان
ما الفرق الذي تحدثه زيادة ثبات POM121؟ يكمن الجواب في بروتين مشهور محفز للسرطان، عامل النسخ c-MYC. يجب أن يدخل c-MYC إلى النواة لتشغيل الجينات، لكن عبوره يعتمد على مكوّنات مسام النواة مثل POM121. أظهر المؤلفون أنه عندما يكون POM121 وفيرًا ومعدّلًا بـO-GlcNAc، يُعثر على قدر أكبر من c-MYC داخل النواة؛ وعندما انخفضت مستويات POM121 أو أزيلت علامته السكرية، تراجع استيراد c-MYC النووي بشكل حاد. في الفئران، شكلت خلايا سرطان الرئة التي تحمل الطفرة غير القابلة للتعديل في POM121 عددًا أقل بكثير وحجمًا أصغر من نقائل العظم، بينما أعاد استعادة c-MYC في الخلايا قليلة POM121 كثيرًا من قدرتها على استعمار العظم. يضع هذا POM121 في مستوى أعلى من c-MYC في طريق حاسم للنقائل.
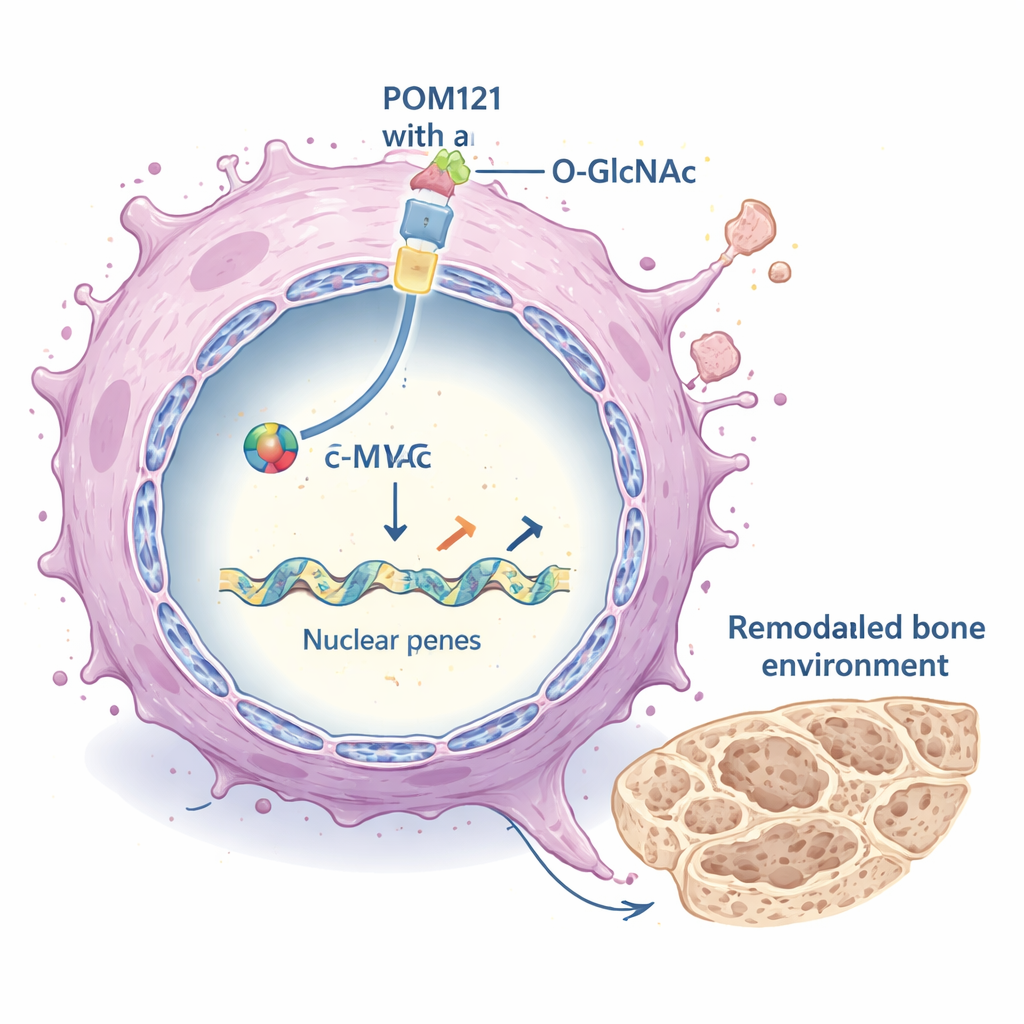
إعادة توصيل محيط الورم
بمجرد دخوله إلى النواة، يعمل c-MYC كمفتاح رئيسي للعديد من الجينات. هنا وُجد أنه ينشّط بقوة مجموعة من الجينات التي تشكل المصفوفة خارج الخلوية (ECM) — الهيكل البروتيني المحيط بالخلايا. تراجع تعبير هذه الجينات المتعلقة بالمصفوفة، التي تشمل أنواعًا متعددة من الكولاجين وإنزيمات تعيد تشكيل النسيج، عند حجب POM121 أو c-MYC، وزاد تعبيرها عندما كانت مستويات O-GlcNAc وPOM121 مرتفعة. بدورها عززت المصفوفة المعدلة مسارات نمو رئيسية داخل الخلايا السرطانية، وبصورة بارزة مسار الإشارة PI3K–AKT–mTOR الذي يدعم البقاء والنمو والانتشار. ظهرت أنماط مماثلة عبر عدة نماذج مختلفة من سرطان الرئة، مما يوحي أن الآلية ليست مقصورة على خط خلوي واحد.
من الاكتشاف في المختبر إلى تأثير على المرضى
عند فحص بيانات المرضى، وجد الباحثون أن المستويات العالية من OGT وPOM121 وc-MYC، وكذلك جينات المصفوفة خارج الخلوية التي ينظّمونها، ارتبطت بنتائج أسوأ ومع أورام رئوية كانت قد انتشرت بالفعل إلى العظام. مجتمعةً، توضح النتائج محور OGT–POM121–c-MYC–ECM: زيادة O-GlcNAcylation تثبت بوّاب النواة POM121، مما ينقل المزيد من c-MYC إلى النواة، الذي يعيد بدوره برمجة السقالة النسيجية وإشارات النمو لصالح نقائل العظم. للمرضى، يشير هذا إلى أنواع جديدة من العلامات البيولوجية لتمييز من هم معرضون لخطر الانتشار العظمي، وإلى زوايا علاجية جديدة — من حجب وظيفة OGT أو POM121 إلى كبح c-MYC أو إعادة تشكيل المصفوفة — التي قد تساعد يومًا في منع وصول سرطان الرئة إلى الهيكل العظمي.
الاستشهاد: Ren, YZ., Zhao, MN., Du, FL. et al. POM121 O-GlcNAcylation facilitates bone metastasis in non-small cell lung cancer through enhanced c-MYC nuclear import and ECM reprogramming. Oncogene 45, 728–743 (2026). https://doi.org/10.1038/s41388-026-03687-y
الكلمات المفتاحية: نقائل العظم في سرطان الرئة, POM121, O-GlcNAcylation, c-MYC, المصفوفة خارج الخلوية