Clear Sky Science · ar
تعطيل تفاعلات مستقبل الأندروجين مع العوامل المساعدة بواسطة بروتين ربط الرنا FUS/TLS يغيّر إشارة الأندروجينات في سرطان البروستات
لماذا يهم هذا البحث لصحة الرجال
يعتمد سرطان البروستات إلى حد كبير على الهرمونات الذكرية المسماة الأندروجينات وعلى بروتين يستشعرها يسمى مستقبل الأندروجين. تعمل معظم العلاجات الحديثة عن طريق قطع هذه الهرمونات أو حجب هذا المستقبل. ومع ذلك، تتخطى العديد من الأورام هذا التحكم في نهاية المطاف وتعود في شكل أكثر عدوانية وصعوبةً في العلاج. يكشف هذا البحث كيف يمكن لبروتين آخر، FUS/TLS، أن يعمل كفرامل قوية لإشارات الأندروجينات في المراحل المبكرة من سرطان البروستات — وكيف يبدو أن هذه الفرامل تفشل مع تقدم المرض.
مُنظّم لحركة إشارات الهرمونات
يتصرف مستقبل الأندروجين مثل مفتاح جزيئي. عندما ترتبط به الأندروجينات، ينتقل المستقبل إلى نواة الخلية، ويلتصق بالحمض النووي، ويشغّل جينات تساعد خلايا البروستات على النمو. لا يعمل بمفرده: يمكن للبروتينات المساعدة أن تعزز نشاطه أو تخفّضه. ركز الباحثون على FUS/TLS (يسمى FUS)، وهو بروتين معروف بدوره في تعاملات الرنا والتحكم في التعبير الجيني، وقد رُبط سابقًا بتباطؤ نمو الأورام. باستخدام خلايا سرطان البروستات المزروعة في المختبر، أظهروا أن العديد من الجينات التي يتحكم بها FUS تتداخل مع الجينات التي يتحكم بها مستقبل الأندروجين، مما يوحي بأن FUS يشكل مباشرةً الطريقة التي تُترجم بها إشارات الهرمونات إلى تعليمات نمو.
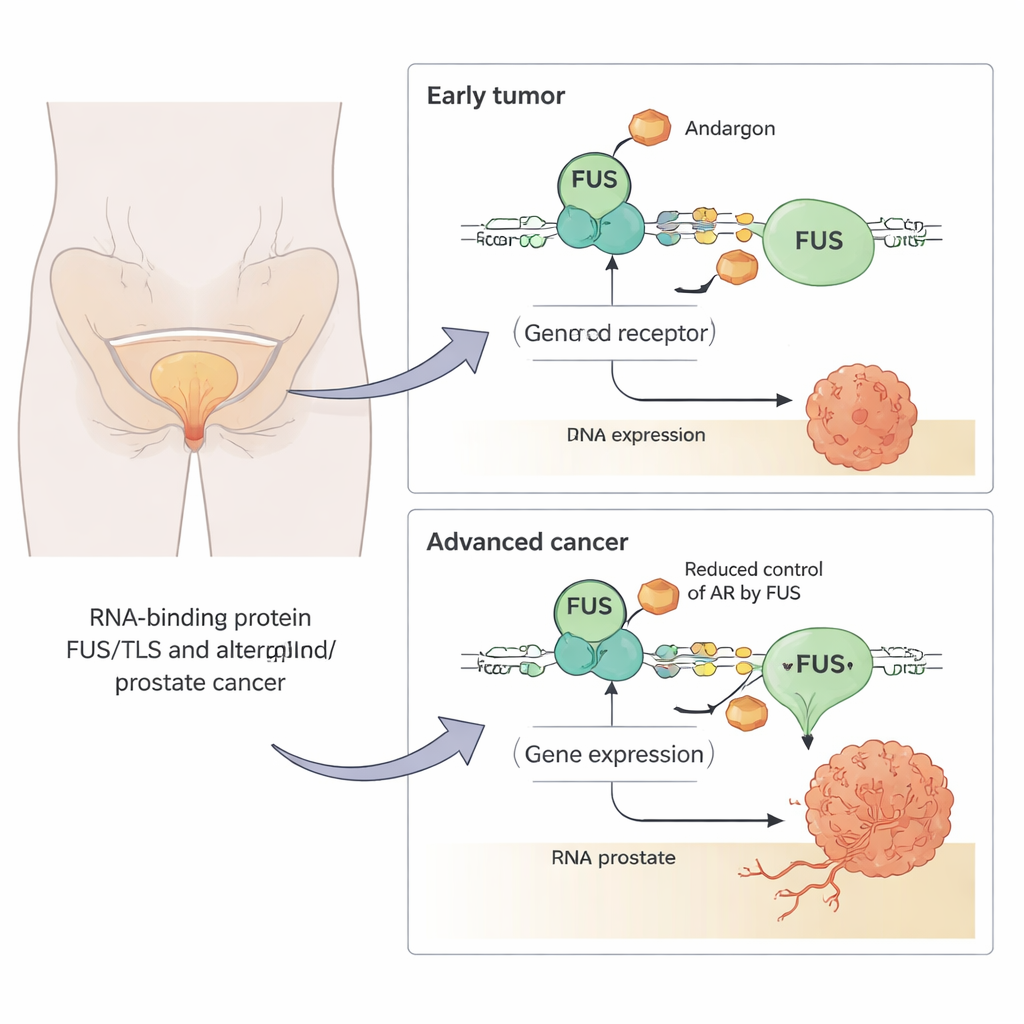
كيف يفرِض FUS الفرامل على الجينات المحفِّزة للورم
لمعرفة ما يفعله FUS، رفع الفريق أو خفّض مستوياته اصطناعيًا في خلايا سرطان البروستات وتتبعوا الجينات التي تغيّرت استجابةً لعقار شبيه بالأندروجين قوي التأثير. وجدوا أن FUS يمكن أن يدفع الجينات التي يتحكم بها الأندروجين في اتجاهين، أحيانًا يعزز وأحيانًا يضعف استجابتها. مع ذلك، كان التأثير الطاغي هو القمع: حيث أن الجينات التقليدية المحفزة بالأندروجين مثل PSA (KLK3) وTMPRSS2 انخفضت عندما كان مستوى FUS مرتفعًا وارتفعت عند إزالة FUS. اختبارات المراسل — قياسات بسيطة لنشاط مستقبل الأندروجين — أكدت أن زيادة FUS خفَّضت نشاط المستقبل بنحو النصف إلى ثلثي النشاط عبر عدة أنواع خلوية.
حاجز فيزيائي على آلية الهرمون
بعد ذلك تساءل العلماء كيف يمارس FUS هذا السيطرة. أظهرت الميكروسكوبات واختبارات التفاعل أن FUS ومستقبل الأندروجين يلتقيان داخل النواة ويرتبطان جسديًا. يلتصق FUS بمنطقة محددة من المستقبل عبر مجال تعرفه على الرنا. كما يرتبط بعدد من البروتينات المساعدة الأساسية التي عادةً ما تعزز نشاط المستقبل. كشفت تجارب مفصّلة عند جين معروف بأنه مستجيب للأندروجين أن FUS لا يوقف المستقبل عن الالتصاق بالحمض النووي؛ بل يمنع تجمّع كامل طاقم المساعدين وآلية النسخ الأساسية هناك. بعبارة أخرى، يترك FUS «المفتاح» على الحمض النووي لكنه يجرّد الأجزاء اللازمة لرفع مستوى التعبير الجيني بالكامل.
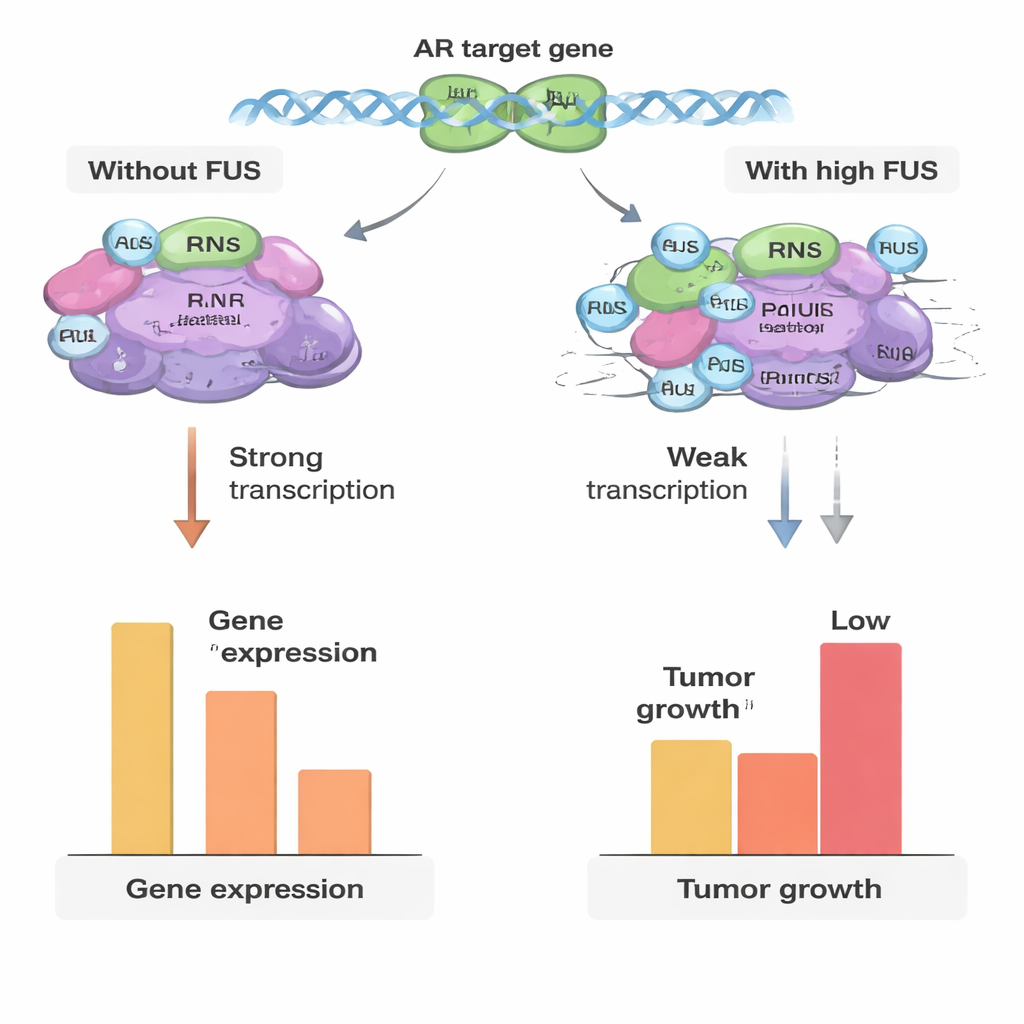
دور متغيّر مع تقدم السرطان
نظرًا لأن مقاومة العلاج في سرطان البروستات غالبًا ما تتضمن تغيُّرات في هذه البروتينات المساعدة، درس الباحثون مستويات FUS في خطوط خلوية وعينات مرضى تشمل الأنسجة الحميدة، والأورام الأولية، وسرطان البروستات المقاوم لخفض الأندروجينات المتقدم (CRPC). في الأورام المبكرة، كانت مستويات بروتين FUS عمومًا أقل منها في العينات الحميدة، وهو ما يتوافق مع فكرة أن الأورام تُخفض هذا المكبح الطبيعي لتسهيل نموها. والمفاجئ أنه في CRPC المتقدم، ارتفعت مستويات FUS مجددًا وكانت أعلى مما هي عليه في الأورام الأولية. ومع ذلك، في نموذج خلوي يشبه CRPC، لم تعد زيادة FUS تغير جينات المعتمدة على الأندروجين بقوة، رغم أنها ما تزال تبطئ نمو الخلايا بشكل عام. يشير ذلك إلى أنه مع تطور السرطان تُعاد برمجة شبكة الأندروجين بحيث يفقد FUS كثيرًا من تأثيره على المستقبل، بينما قد يعمل عبر مسارات أخرى مرتبطة بالنمو.
ما معنى ذلك للعلاجات المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن FUS يتصرف مثل جهاز أمان مدمج يمنع عادةً إشارات الهرمونات الذكرية من دفع خلايا البروستات إلى الإدراك المفرط في النمو. في المراحل المبكرة من السرطان، يساعد خفض FUS الأورام على النمو؛ في المرض المتقدم، يتغير نظام الهرمونات بما يكفي ليصبح FUS وافرًا لكنه لم يعد يقيّد مستقبل الأندروجين بفعالية. يمكن أن يؤدي فهم كيفية عمل هذه الفرامل بالضبط — ولماذا تفشل — إلى إلهام استراتيجيات جديدة تستعيد السيطرة أو تحاكي قدرة FUS على تعطيل آلية النمو المدفوعة بالهرمونات، مما قد يحسّن العلاجات للرجال المصابين بسرطان البروستات المتقدم.
الاستشهاد: Brooke, G.N., Leach, D.A., Culley, R.L. et al. Disruption of androgen receptor-cofactor interactions by the RNA-binding protein FUS/TLS alters androgen signalling in prostate cancer. Oncogene 45, 757–773 (2026). https://doi.org/10.1038/s41388-026-03682-3
الكلمات المفتاحية: سرطان البروستات, مستقبل الأندروجين, مقاومة العلاج الهرموني, بروتينات رابطة الرنا, FUS TLS