Clear Sky Science · ar
يعكس السورتيلين نشاطًا شبيهًا بمثبط الورم من خلال الحد من وظيفة نقل الإشارة لمستقبل EGFR
لماذا هذا مهم لعلاج السرطان
يُعد سرطان الرئة السبب الرئيسي للوفيات الناجمة عن السرطان على مستوى العالم، وتستهدف العديد من الأدوية الحديثة جزيئًا يُسمى EGFR الذي يدفع نمو الأورام. غالبًا ما تُظهر هذه الأدوية فاعلية في البداية، لكن الأورام تتطور عادة لتصبح مقاومة. يكشف هذا البحث عن "مكابح" طبيعية داخل خلايا سرطان الرئة — دور غير متوقع لبروتين اسمه سورتيلين — يمكنه تخفيف إشارات EGFR المحفزة للسرطان. فهم هذه العلاقة قد يساعد في توضيح سبب استجابة بعض المرضى لعلاجات تستهدف EGFR بشكل أفضل، ويقترح طرقًا جديدة لإطالة مدة فاعلية تلك العلاجات. 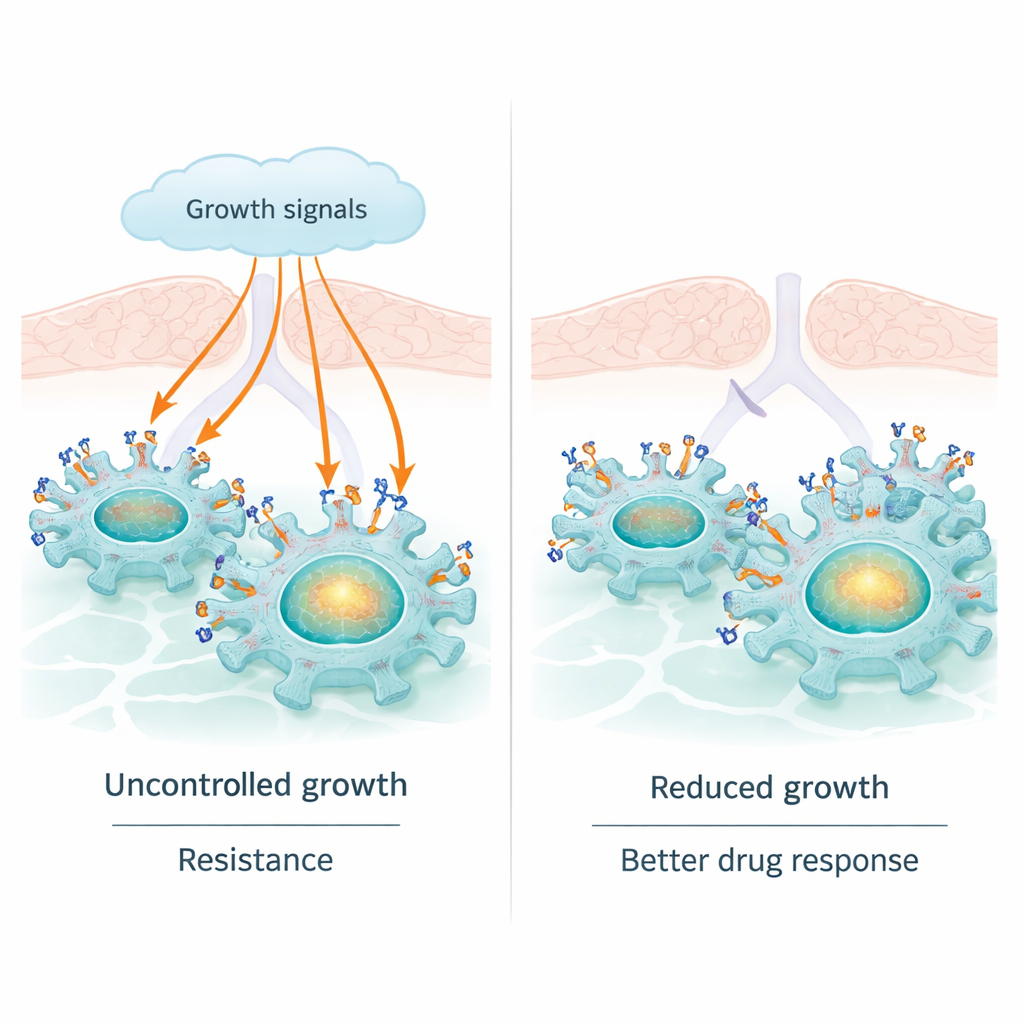
مفتاح النمو الذي انقلب إلى تسريع مفرط
EGFR هو مستقبل موجود على سطح العديد من الخلايا، حيث يستشعر إشارات النمو من البيئة المحيطة. في شريحة كبيرة من الأورام الغدية الرئوية، يتغير EGFR بحيث يبقى في حالة تشغيل دائم. هذا يمد الخلايا بنشاط مستمر للنمو والانقسام، ولهذا السبب يمكن لأقراص حابسة التايروسين كيناز أن تقلص الأورام. لكن لـ EGFR جانبًا آخر أقل شهرة: يمكنه الانتقال إلى نواة الخلية والتصرف مباشرة على الحمض النووي، مفعّلًا جينات مثل cMYC وCCND1 التي تعزز النمو والبقاء ومقاومة العلاج. قد يساعد هذا الدور النووي لـ EGFR الأورام على الهروب حتى عندما تُمنع نشاطاته السطحية كيميائيًا.
دخول السورتيلين إلى النواة
كان السورتيلين معروفًا سابقًا بشكل أساسي كبروتين فرز يساعد في إدخال EGFR من سطح الخلية وإرساله نحو التحلل، مما يضعف إشاراته المحفزة للنمو. في هذا العمل، يبيّن المؤلفون أن السورتيلين يتبع EGFR أيضًا إلى النواة عندما تُحفّز خلايا سرطان الرئة. باستخدام مجهرية عالية الدقة وتجزيء حيوي كيميائي للكسور الخلوية، لاحظوا تكوّن مركبات من EGFR والسورتيلين داخل النوى بعد وقت قصير من التنشيط. والأهم من ذلك، أنه عندما لم يستطع EGFR دخول النواة، بقي السورتيلين خارجها كذلك، مما يشير إلى أن EGFR يعمل كـ "تذكرة" للسورتيلين للدخول إلى هذا الحيز. وبمجرد وجودهما هناك، وُجدت مركبات EGFR–السورتيلين مرتبطة بمقاطع من الحمض النووي قرب مواقع بدء بعض الجينات المسؤولة عن التحكم في النمو، بما في ذلك cMYC وCCND1.
مكابح داخلية على جينات السرطان
لفهم وظيفة هذه المركبات، رسم الباحثون خارطة لارتباطها عبر الجينوم وقاسوا التغيرات في نشاط الجينات. وجدوا أن EGFR بمفرده يميل إلى تعزيز تنشيط الجينات المرتبطة بالنمو، في حين أن وجود السورتيلين في نفس مناطق الحمض النووي يخفف من هذا التأثير. عندما خُفضت مستويات السورتيلين اصطناعيًا، زاد ارتباط EGFR عند الجينات المستهدفة، وأصبحت الجينات المحفزة للسرطان مثل cMYC وCCND1 أكثر نشاطًا. وعلى النقيض من ذلك، أدى رفع مستويات السورتيلين إلى العكس: خفّت قبضة EGFR على الحمض النووي، وتراجع جذب آلية النسخ، وانخفض التعبير عن هذه الجينات المسببة للسرطان. في نماذج الفئران، نمت أورام الرئة المهندسة لإنتاج سورتيلين بكثرة بوتيرة أبطأ وأظهرت مستويات منخفضة من cMYC وCCND1. 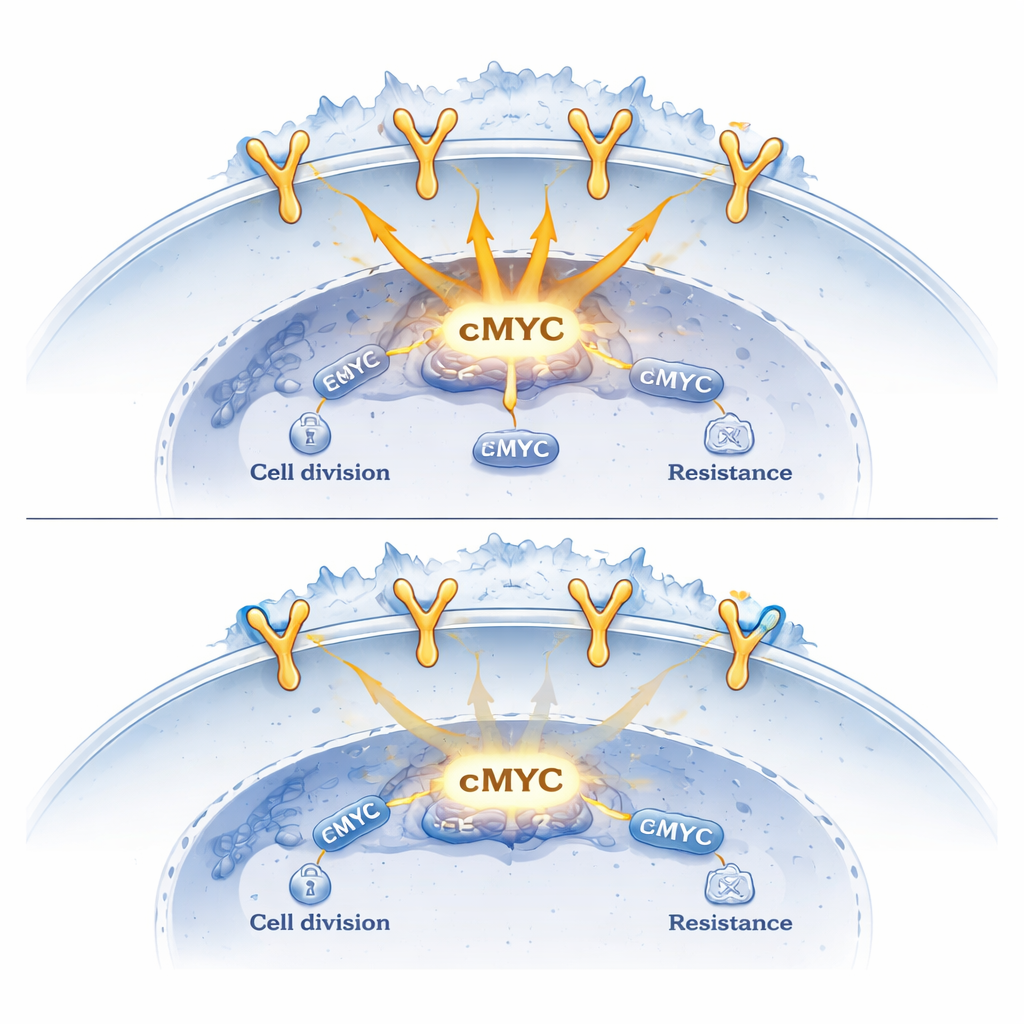
التداخل مع أدوية تستهدف EGFR
استكشف البحث أيضًا كيف يتفاعل هذا الآلية مع أوزيمرتينيب، دواء واسع الاستخدام موجه لـ EGFR ومصمم لحجب طفرات EGFR المزعجة. بشكل مفاجئ، حتى عندما أوقف أوزيمرتينيب نشاط إنزيمات EGFR، استمر المستقبل في التحرك إلى النواة. هناك، واصل الارتباط بالحمض النووي، خصوصًا بالقرب من جين cMYC. تراكم السورتيلين أيضًا في النواة تحت هذه الظروف. عندما كان السورتيلين وفيرًا، انخفضت مستويات cMYC بقوة أكبر استجابةً لأوزيمرتينيب، وأصبحت خلايا السرطان أقل قابلية للبقاء. أظهرت تحليلات لأورام المرضى ومجموعات بيانات سرطانية عامة واسعة أن مستويات السورتيلين غالبًا ما تكون أقل في الأورام الغدية الرئوية مقارنةً بنسيج الرئة الطبيعي، وأن التعبير الأعلى عن السورتيلين يرتبط باستمرار بتعبير أقل عن cMYC.
ما معنى هذا للمرضى
عند النظر إلى النتائج مجتمعة، تصوّر الدراسة السورتيلين كشريك يشبه مثبط الورم يرافق EGFR إلى النواة ثم يقيده. من خلال الحد من قدرة EGFR على تشغيل جينات نمو قوية مثل cMYC، يمكن للسورتيلين إبطاء تقدم الورم وتعزيز تأثير الأدوية الحابسة لـ EGFR. وبما أن العديد من أورام الرئة تحتوي على سورتيلين منخفضًا، فقد تفتقر إلى هذا المكبح الداخلي، مما يساعد في تفسير سبب كون بعض السرطانات أكثر عدوانية أو تصبح مقاومة للأدوية بسرعة. قد يساعد قياس مستويات السورتيلين في الأورام على التنبؤ بمدى استجابة المريض للعلاجات الموجهة إلى EGFR، وقد توفر استراتيجيات رفع نشاط السورتيلين وسيلة جديدة للحفاظ على السيطرة على السرطانات المدفوعة بـ EGFR لفترات أطول.
الاستشهاد: Lapeyronnie, E., Granet, C., Tricard, J. et al. Sortilin exhibits tumor suppressor-like activity by limiting EGFR transduction function. Oncogene 45, 875–888 (2026). https://doi.org/10.1038/s41388-026-03680-5
الكلمات المفتاحية: سرطان الرئة, EGFR, سورتيلين, cMYC, مقاومة العلاج المستهدف