Clear Sky Science · ar
ميكروفلويديك قصوري متسلسل للثرّية عالية الإنتاجية ومتعددة المقاييس لخلايا الورم والعناقيد السليمة نحو تحسين تشخيص الخباثة
لماذا يهم فرز خلايا السرطان في السوائل
عندما ينتشر السرطان، تهرب خلايا الورم أحياناً إلى السوائل التي تغمر أعضائنا. لدى مرضى سرطان الرئة، قد يشمل ذلك السائل الذي يتراكم حول الرئتين والمعروف بالانصباب الجنبي. مخفيّة داخل هذا السائل توجد خلايا ورمية مفردة نادرة وتكتلات محكمة من الخلايا. تُعد هذه العناقيد خطرة بشكل خاص لأنها مرتبطة بقوة بمرض عدواني وبنتائج سيئة. ومع ذلك، تكافح طرق المختبر الحالية لاستخراج كل من الخلايا المفردة والعناقيد بلطف وبفعالية من أحجام كبيرة من سوائل المرضى. تقدم هذه الدراسة تقنية جديدة مُبسطة على شريحة تستطيع فرز هذه الخلايا من الانصباب الجنبي بسرعة وبعناية، مما يفتح الباب لتشخيص أكثر موثوقية وفهماً أفضل لكيفية انتشار الأورام.
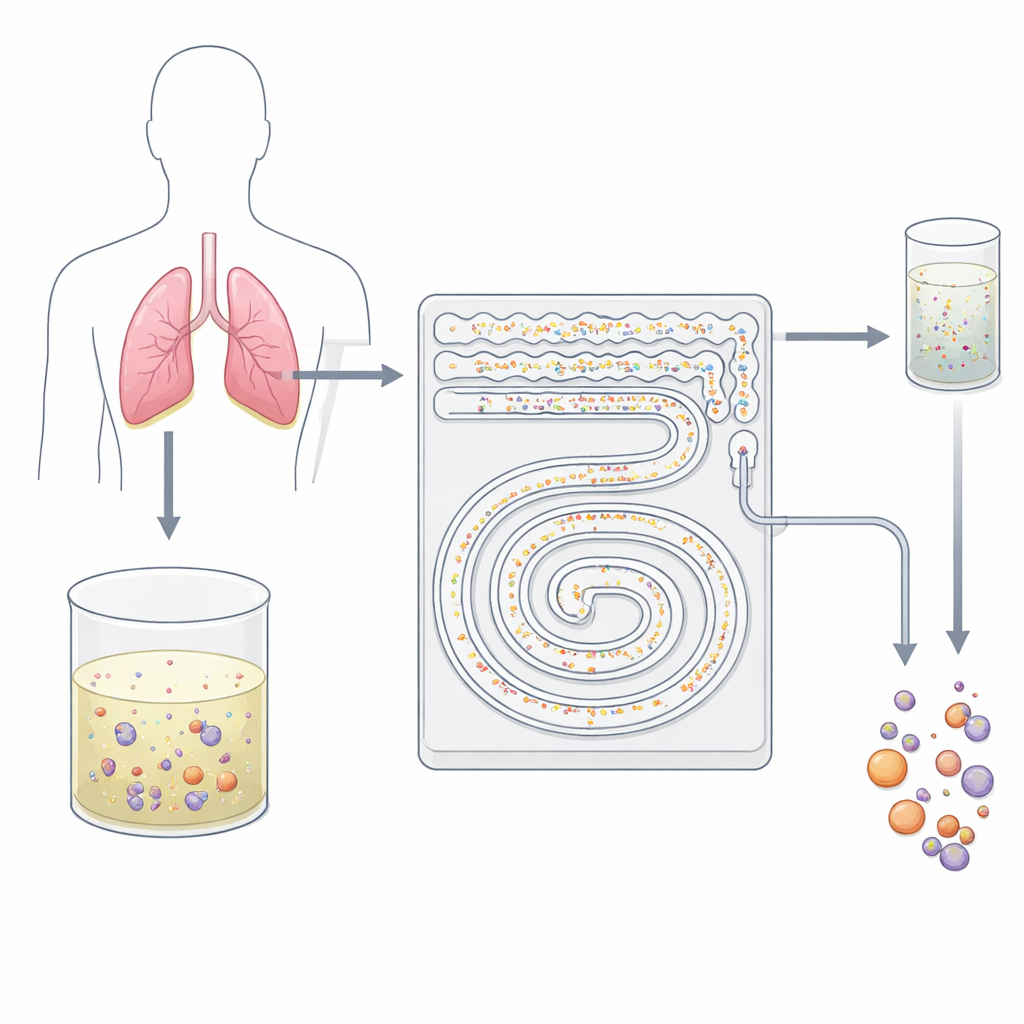
مصفاة خلوية لطيفة على شريحة
صمَّم الباحثون جهازاً بلاستيكياً بحجم راحة اليد محفوراً بقنوات دقيقة تعمل كمرشح ذكي من خطوتين. بدلاً من استخدام الأجسام المضادة اللاصقة أو التنقية الخشنة، يعتمد الشريحة على سلوك الخلايا في تيار سائل سريع. عند اندفاع السائل عبر قنوات دقيقة منحنية، تدفع قوى غير مرئية الجسيمات ذات الأحجام المختلفة إلى مسارات تيارية مختلفة. تستفيد الفريق من هذا التأثير المعروف عموماً بالميكروفلويديك القصوري للفصل بين خلايا الدم الخلفية الصغيرة وخلايا الورم الأكبر وعناقيدها دون لمسها أو تمييزها بعلامات. وبما أن كل شيء يحدث في تدفُّق مستمر ومغلق، يمكن للجهاز معالجة عشرات الميليلترات من السائل في دقائق معدودة — وهو ما يصعب تحقيقه في علم الخلايا التقليدي المعتمد على شرائح.
الخطوة الأولى: إفراغ الحشد
في المرحلة الأولى من الجهاز، يُدفع الانصباب الجنبي — بعد إزالة السائل الزائد وإعادة تعليق الخلايا — عبر مصفوفة من القنوات الحلزونية المتوازية. هنا، يدفع التدفق الدائري والمنحني خلايا الدم البيضاء الصغيرة نحو جدران القناة، بينما تبقى خلايا الورم الأكبر والعناقيد قرب مركز التيار. تُوجَّه الخلايا الصغيرة إلى مخارج النفايات، مما يخفف الخلفية بشكل كبير. يمكن لهذه الخطوة عالية الإنتاجية أن تعمل عند نحو 8 ميليلتر في الدقيقة، مما يعني أن عينة سريرية معتادة بحجم 50 ميليلتر يمكن معالجتها في حوالي ست دقائق ونصف دون انسداد. ما يخرج من هذه المرحلة هو خليط أنظف بكثير، مُخصَّب بالخلايا المحتملة الخبيثة وجاهز للفصل الأدق.
الخطوة الثانية: فصل المفردات عن العناقيد
تدخل العينة المُخصَّبة جزئياً بعد ذلك قناة حلزونية مائلة تتضمن نمطاً متكرراً من مقاطع ضيقة وعريضة. في هذه المرحلة، تتوازن عدة قوى تدفقية بشكل مختلف بالنسبة للأجسام ذات الأحجام المختلفة، مما يوجهها إلى مجارى متميزة قرب الجدار الداخلي أو الخارجي لللولب. تستقر الخلايا الوحيدة الشبيهة بالورم، الأصغر حجماً، في موقع جانبي واحد، بينما تهاجر العناقيد الأضخم إلى موقع مختلف أقرب إلى الجدار الداخلي. عن طريق وضع المخارج في المواضع الصحيحة، تقسم الشريحة هذه المسارات ماديّاً: يجمع مخرج واحد في المقام الأول الخلايا الورمية المفردة، ويجمع مخرج آخر العناقيد السليمة، وتزيل مخارج أخرى الخلايا الصغيرة المتبقية. والأهم أن العناقيد تبقى كاملة، متجنبة التلف والتفكك الذي غالباً ما تسببه طرق الترشيح التقليدية.
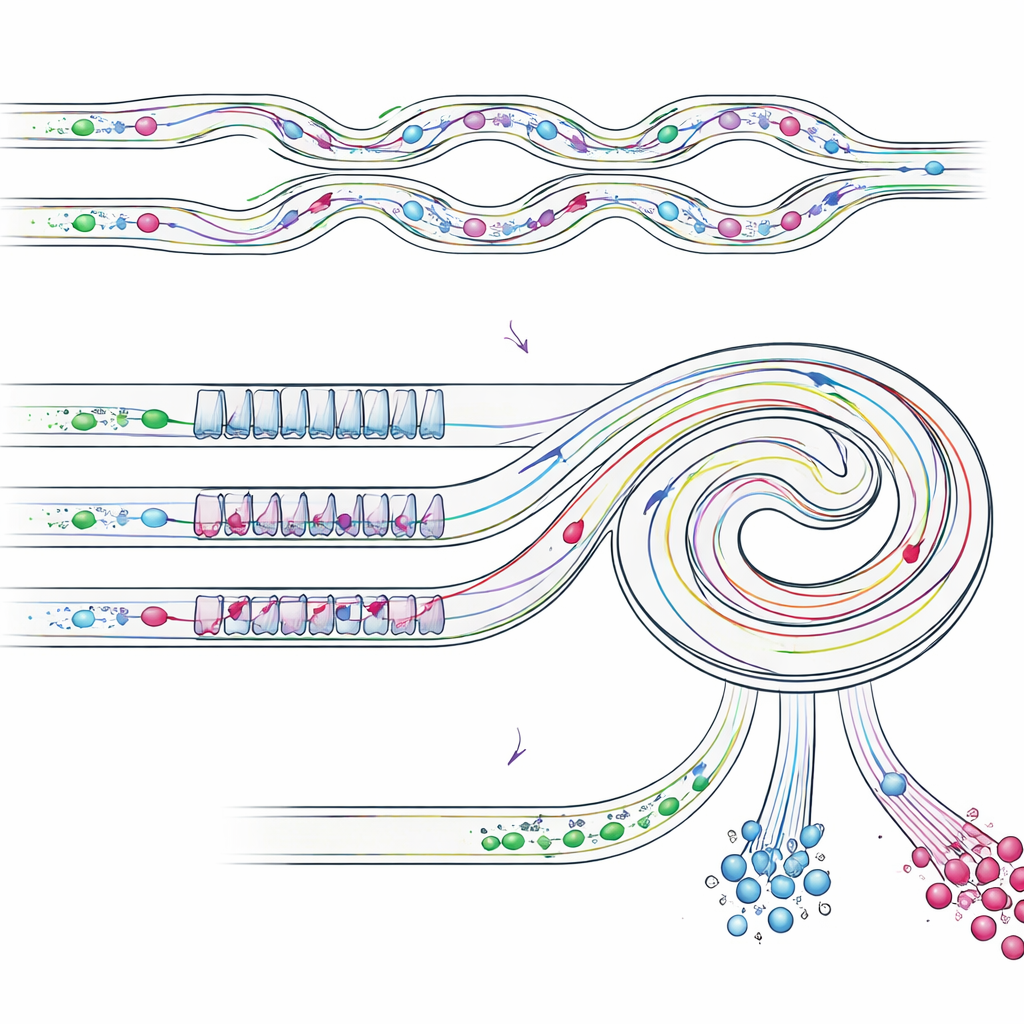
تجربة الجهاز
لفحص مدى كفاءة تصميمهم، استخدم الفريق أولاً حبيبات بلاستيكية ذات أحجام معروفة لتقليد خلايا الدم والخلايا الورمية المفردة والعناقيد. أظهروا أن الشريحة المتسلسلة استرجعت أكثر من 87% من حبيبات "الخلايا المفردة" وحوالي 92% من حبيبات "العناقيد"، مع إزالة معظم حبيبات "خلايا الدم" الأصغر. ثم انتقلوا إلى خلايا سرطان رئة حقيقية (خلايا A549) مخلوطة بخلايا دم بيضاء. في هذه الاختبارات، استعاد الجهاز نحو 82% من خلايا السرطان إجمالاً، مع نقاوة بنحو 76% في الكسر المُخصَّب وحوالي 80% نقاوة لعناقيد الخلايا. أخيراً، عالجوا عينات انصباب جنبي فعلية من ثلاثة مرضى بسرطان الرئة. بدءاً من سائل كانت فيه خلايا الورم والعناقيد أقل من 1% من جميع الخلايا، أنتجت الشريحة كسوراً وصلت فيها الخلايا الخبيثة المفردة إلى نحو 68% من جميع الخلايا، وشكلت العناقيد حوالي 35% من الخلايا في مجرى مخرج مخصص.
ما الذي قد يعنيه هذا للمرضى
باستخدام التدفق السائلي فقط وشكل القنوات، يمكن لهذا الجهاز سحب كل من خلايا الورم المفردة والعناقيد السليمة بسرعة وبلطف من أحجام كبيرة من سائل المريض دون علامات كيميائية أو أدوات معقدة. تظل الخلايا المُخصّبة مناسبة لاختبارات قياسية مثل صبغة المناعة المضيئة والمجهرية، مما ينسجم بسلاسة مع سير العمل الموجود في المستشفيات. وبينما شملت الدراسة الحالية عدداً صغيراً من المرضى وستحتاج إلى تجارب أكبر لإثبات تأثيرها على التشخيص والتنبؤ بالنتيجة، تُظهر هذه العمل فكرة قوية: "مركزِر خلايا" سريع وخالٍ من العلامات يكشف كل من عدد وحالة تجمّع خلايا الورم في الانصبابات الجنبية. على المدى الطويل، قد تُحسّن هذه الأدوات تقييم الخباثة، وتوجّه خيارات العلاج المخصص، وتوفر نافذة أوضح على كيفية انتقال السرطانات.
الاستشهاد: Zhu, Z., Ren, H., Zhang, Z. et al. Cascading inertial microfluidics for high-throughput, multi-scale enrichment of tumor cells and intact clusters towards enhanced malignancy diagnosis. Microsyst Nanoeng 12, 101 (2026). https://doi.org/10.1038/s41378-026-01235-y
الكلمات المفتاحية: الخزعة السائلة, فرز الخلايا ميكروفلويديكياً, عناقيد خلايا الورم, انصباب جنبي, تشخيص السرطان