Clear Sky Science · ar
صفائِح نانوية هجينة من WS2 مدوَّنة بالنحاس ومُعدّلة بالـPEG للعلاج المتعدِّد الأوضاع المستهدف للسرطان
لماذا تهم العلاجات الأذكى للسرطان
لا يزال العديد من مرضى سرطان الثدي يواجهون علاجات قاسية قد تضر الأنسجة السليمة دون أن توقف الورم تمامًا. تصف هذه الدراسة نوعًا جديدًا من الصفائح المهندَسة النانوية، صغيرة جدًّا بحيث لا تُرى بالعين المجردة، مصمَّمة للتجوّل في الجسم، والتوجّه نحو أورام الثدي، ومهاجمتها بعدة آليات منسَّقة في وقت واحد. عبر دمج الحرارة والكيمياء ودواء سرطاني تقليدي في حزمة مستهدفة واحدة، يسعى الباحثون لجعل العلاج أقوى وفي الوقت نفسه ألطف على بقية الجسم. 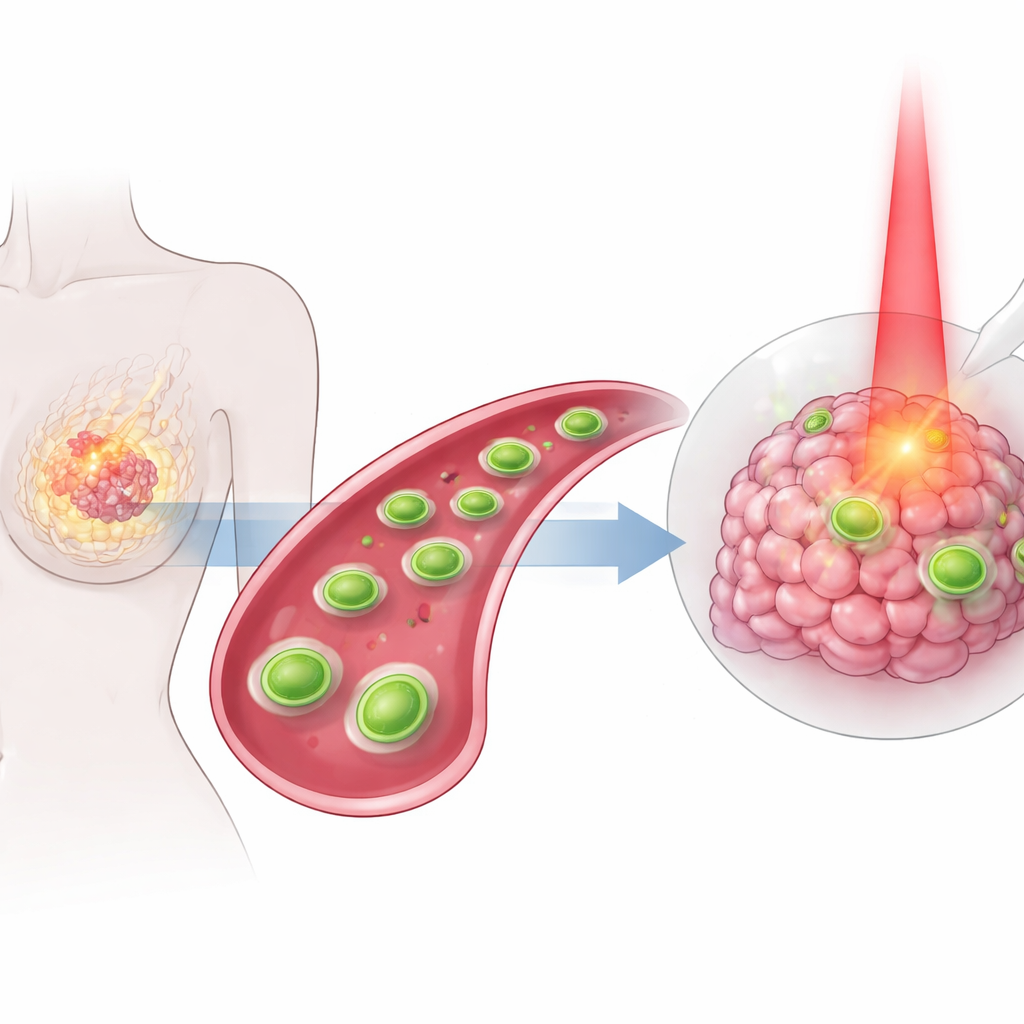
صفائح دقيقة مبنية لحمل وتوصيل العلاج
جوهر النهج هو مادة فائقة الرقة مصنوعة من التنجستن والكبريت، على شكل صفائح نانوية. هذه الصفائح تمتص بشكل طبيعي الضوء القريب من تحت الحمراء وتحوّله إلى حرارة. أنشأ الفريق هذه الصفائح ثم خشنّ سطحها بعناية بحيث تستطيع احتواء مكوّنات مفيدة أخرى. رُسّخ ذرات النحاس بشكل مبعثر على الصفائح، وأضيف طلاء ناعم ومرن أشبه بـ"معطف مطري" جزيئي لمساعدة الجسيمات على الاختلاط جيدًا في سوائل الجسم وتجنّب التكتّل. أخيرًا، أُلصِق حمض الفوليك — وهو فيتامين تمتصه العديد من خلايا الورم بشراهة — كجهاز توجيه، وحُمِّل دواء العلاج الكيميائي الشائع دوكسوروبيسين على السطح. النتيجة النهائية هي منصة طبقية صغيرة يمكنها الدوران في الدم والتعرّف على خلايا الورم وحمل حمولة كبيرة من العلاج.
كيف تعمل الفيزياء والكيماوات والدواء معًا
بمجرد وصول هذه الجسيمات إلى الورم، تحدث عدة أمور معًا. عندما يُسلّط على منطقة الورم ليزر أحمر لطيف، تسخن صفائح التنجستن‑الكبريت بكفاءة، مما يرفع درجة الحرارة المحلية بما يكفي لإجهاد وإتلاف الخلايا السرطانية دون تسخين مفرط لباقي الجسم. في الوقت نفسه، تتفاعل ذرات النحاس على الصفائح مع جزيئات البيروكسيد الطبيعية الموجودة بمستويات أعلى داخل الأورام. يحول هذا التفاعل البيروكسيد إلى مؤكسدات شديدة العدوانية وقصيرة العمر تهاجم مكونات الخلية من الداخل. كما أن الأورام تميل لأن تكون أكثر حموضة قليلًا من الأنسجة السليمة؛ في هذا الوسط الأشد حمضية، وتحت تأثير التسخين بالليزر، يضعف الربط بين الصفيحة والدوكسوروبيسين، مما يسمح بإطلاق مزيد من الدواء تمامًا حيث يُحتاج إليه. هذه التأثيرات الثلاثة — الحرارة والهجوم الكيميائي والكيماوي الموجَّه — مصمَّمة لتقوية بعضها البعض. 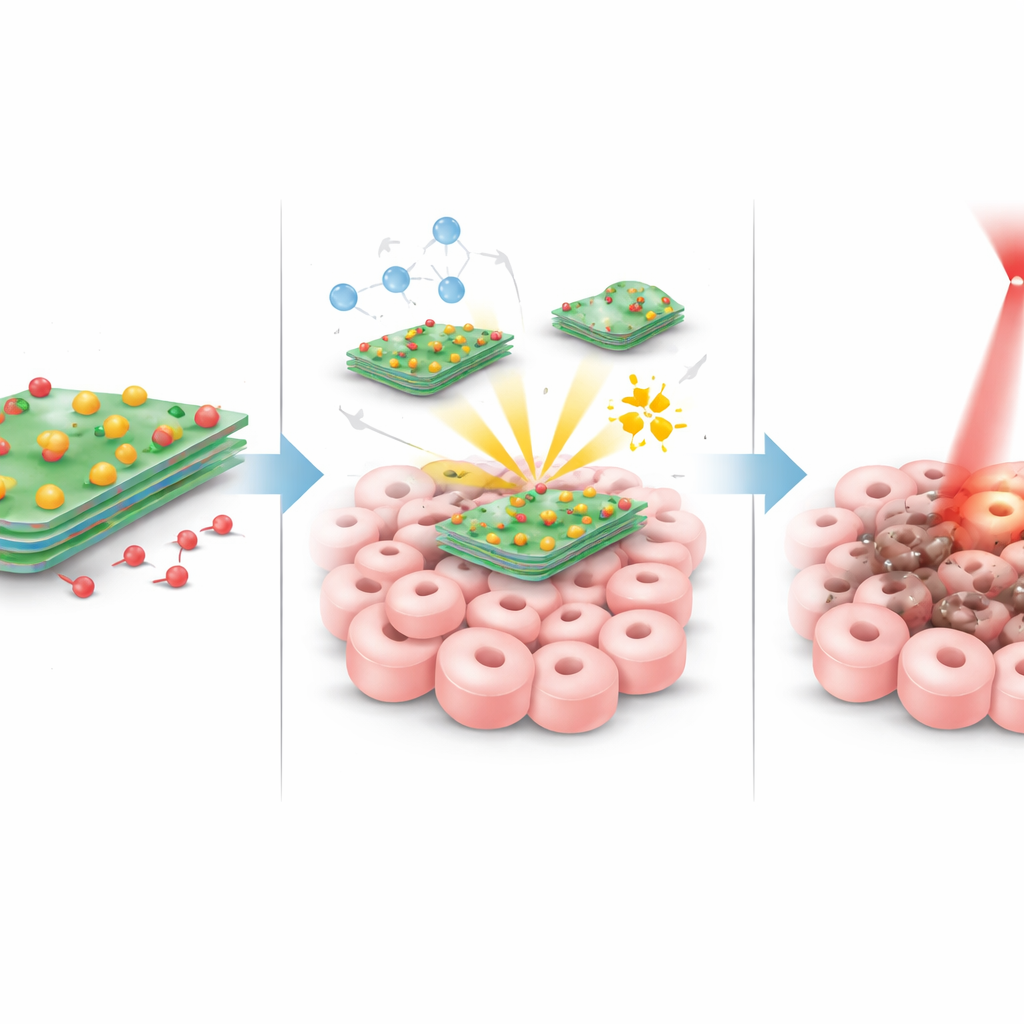
دليل من الخلايا والفئران الحاملة للأورام
في أطباق المختبر، لم تُظهر الصفائح المطلية بمفردها ضررًا كبيرًا للخلايا الطبيعية، ما يشير إلى سلامة أساسية جيدة. لكن عندما حُمِّلت بالدوكسوروبيسين وتعرّضت لضوء الليزر في وجود بيروكسيد، تسببت في موت قوي لخلايا سرطان الثدي، أعلى بكثير من أي علاج منفرد. أظهر الباحثون أيضًا أن الجسيمات تولِّد اندفاعًا من المؤكسدات التفاعلية داخل خلايا الورم، مؤكّدين نشاط كيمياء النحاس. في الفئران الحاملة لأورام الثدي، تراكمت الجسيمات المغطاة بحمض الفوليك بشكل أقوى ولمدة أطول في نسيج الورم مقارنة بالجسيمات غير المستهدفة. عندما تلقّت الفئران التوليفة الكاملة — الجسيمات المستهدفة زائد تعرّض للضوء الأحمر — تقلَّصت أورامها بشكل كبير، وارتفعت مدة بقائها على قيد الحياة، وظل وزن أجسامها وصحّة أعضائها طبيعيًا إلى حد كبير، مشيرًا إلى آثار جانبية محدودة مقارنة بعلاج الدواء القياسي.
ماذا قد يعني هذا لمستقبل رعاية السرطان
تشير النتائج مجتمعة إلى أن هذه الصفائح المهندَسة تعمل كأداة متعددة الوظائف لعلاج السرطان: تسعى إلى الأورام، وتسوّيها حراريًا، وتسمِّمها من الداخل عبر كيمياء تفاعلية، وتوصِل دواء مثبتًا بدقة أكبر، مع حماية معظم بقية الجسم. لا يزال العمل في مرحلة دراسات حيوانية، وهناك أسئلة مهمة مفتوحة حول السلامة على المدى الطويل والتحلل وكيفية أفضل تصنيع مثل هذه الجسيمات لاستخدام البشر. ومع ذلك، يظهر التصميم كيف أن جمع عدة علاجات متواضعة في حزمة ذكية واحدة مصممة لبيئة الورم يمكن أن ينتج تأثيرًا كليًا أقوى بكثير. إذا أكدت الدراسات المستقبلية سلامتها وفعاليتها، فقد تساعد مثل هذه المنصات النانوية متعددة الوظائف في جعل علاج سرطان الثدي أكثر استهدافًا وكفاءة وأقل إيلامًا للمرضى.
الاستشهاد: Li, D., Wen, C., Wu, H. et al. PEGylated Cu-doped WS2 hybrid nanosheets for targeted multimodal cancer therapy. Microsyst Nanoeng 12, 121 (2026). https://doi.org/10.1038/s41378-026-01218-z
الكلمات المفتاحية: علاج سرطان الثدي, طب النانوي, العلاج الحراري الضوئي, توصيل الدواء الموجَّه, العلاج الكيميائي الديناميكي