Clear Sky Science · ar
نظام روبوتي لنقل الخلايا قائم على نمذجة مقاومة الميكروببت
نقل خلايا دقيقة دون مجهر
تعتمد البيولوجيا الحديثة غالبًا على مهمة تبدو بسيطة بشكل مدهش: التقاط خلية واحدة بأنبوب زجاجي ووضعها في مكان آخر. هذا ضروري لعلاجات الخصوبة، وتجميد الأجنّة، والعلاجات المعتمدة على الخلايا، والبحوث الأساسية. ومع ذلك، يتطلب هذا اليوم تقريبًا دائمًا مجهرًا ضخمًا ومشغلًا بشريًا مدرّبًا يراقب كل حركة. يصف هذا البحث نظامًا روبوتيًا جديدًا قادرًا على نقل خلايا مفردة بين قطرات سائل دون أي رؤية مجهرية على الإطلاق، مما يفتح الباب أمام "مصانع خلايا" مغلقة ومؤتمتة بالكامل يمكنها العمل بسرعة أكبر وتكلفة أقل وبضرر أقل للخلايا الحساسة.
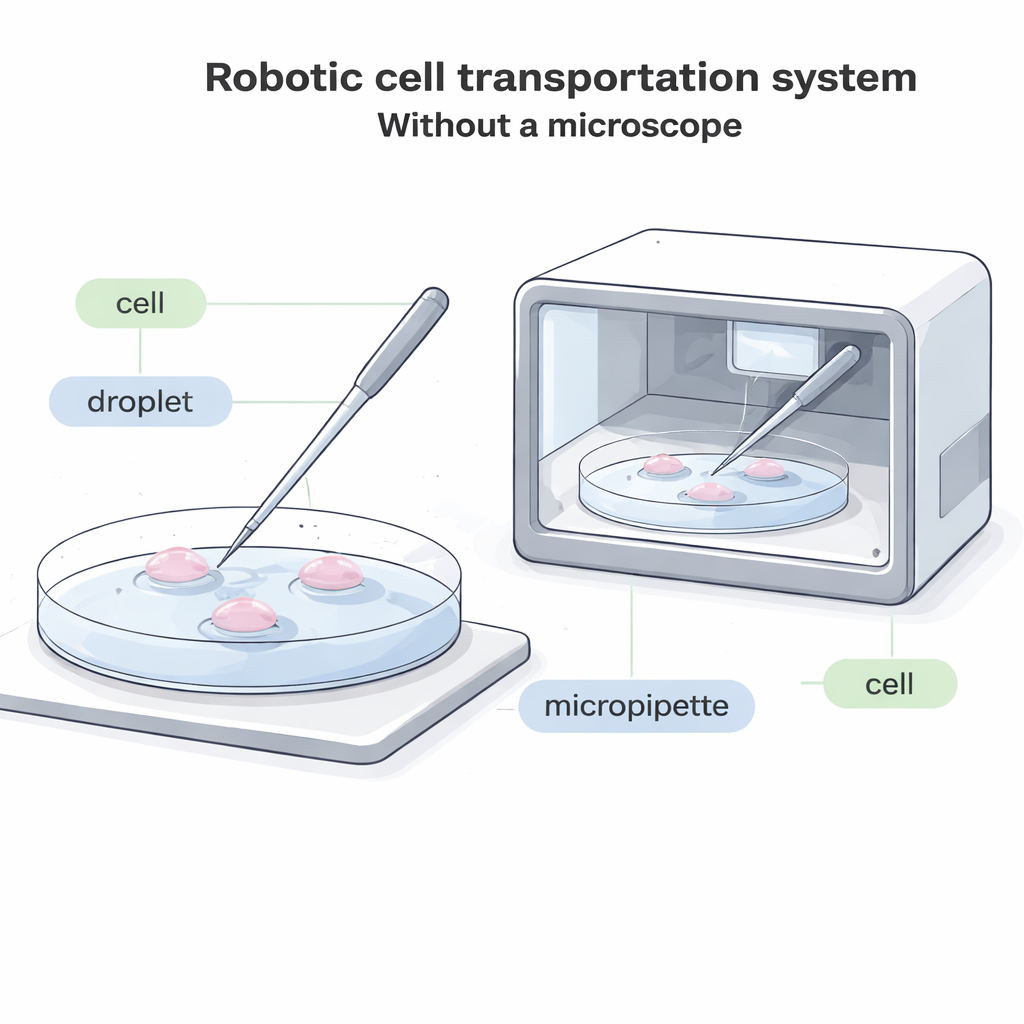
لماذا يحتاج نقل الخلايا إلى تحديث
في المختبرات الحالية، ينظر المشغل عبر المجهر ويستخدم أنبوبًا زجاجيًا رفيعًا يسمى ميكروببت للهبوط على قعر الصحن، وامتصاص خلية واحدة برفق، ونقلها إلى قطرة سائلة جديدة، ثم دفعها خارجًا. هذه العملية بطيئة، وتتطلب تركيزًا بصريًا كبيرًا، ومن الصعب أتمتتها. في أنظمة مستقبلية كثيرة — مثل الأجهزة المدمجة والمغلقة التي تنمي الأجنّة أو خلايا أخرى داخل صندوق — لا يوجد مساحة كافية لمجهر تقليدي. في حالات أخرى، تُوسَم الخلايا بصبغات متوهجة قد تتلاشى أو تتضرر بالضوء، لذا فإن تقليل المراقبة الميكروسكوبية الساطعة مهم. الأنظمة "العمياء" الحالية التي لا تعتمد على الصور تعمل فقط مع خلايا كبيرة بشكل غير اعتيادي، مما يترك معظم أنواع الخلايا الشائعة دون حل آلي جيد.
قشة خاصة مزودة "بحلق إيقاف" مدمج
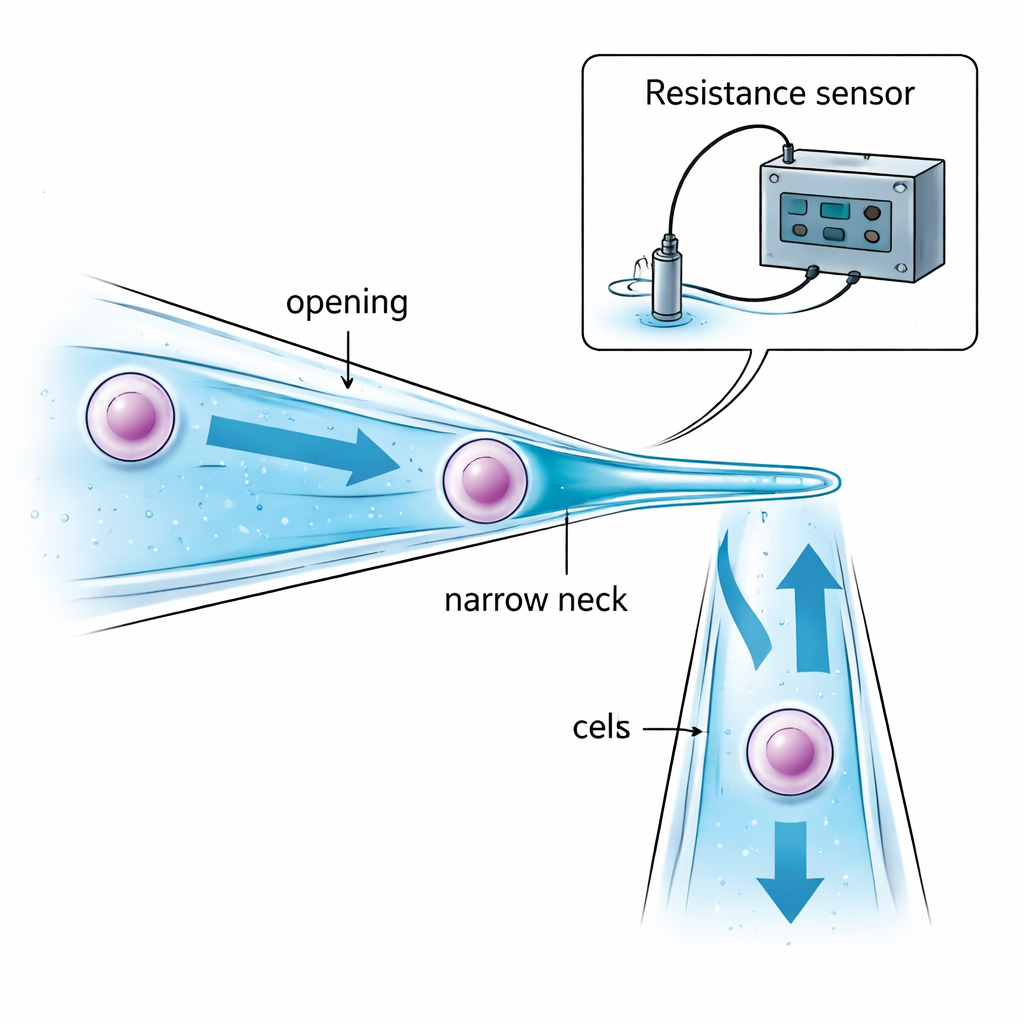
واجه الباحثون المشكلة بإعادة تصميم الميكروببت نفسه. بدلًا من أنبوب زجاجي مستقيم بنفس القطر طوال طوله، صنعوا ميكروببت ذو عنق ضيّق. فتحتها أعرض قليلًا من الخلية المستهدفة بحيث يمكن سحب الخلية إلى الداخل. أعمق داخل الأنبوب، يضيق الأنبوب بلطف إلى "عنق" أصغر من الخلية. عندما تسحب الشفط الخلية نحو هذا التضيّق، تتوقف الخلية وتُحتجز داخل الأنبوب — بدلًا من أن تتدلّى عند الطرف وتتعرض للزيت أو الهواء بين القطرات. اختيار دقيق لحجم الفتحة وحجم العنق والمسافة بينهما يضمن إمكانية التقاط الخلية بأمان دون ضغط مفرط، وأن مقدارًا صغيرًا فقط من السائل يُنقل من قطرة إلى أخرى، مما يقلل التلوث.
الاستماع إلى الإشارات الكهربائية بدلًا من النظر
دون مجهر، يجب أن يعرف الروبوت ثلاث أمور على الأقل: متى يكون طرف الزجاج قريبًا بما يكفي من قعر الصحن، ومتى تم التقاط الخلية بنجاح عند العنق، ومتى تم إطلاقها بالكامل في القطرة الجديدة. حلّ الفريق ذلك بمراقبة تغيّرات صغيرة في المقاومة الكهربائية في السائل داخل الميكروببت وحوله. عندما يقترب الميكروببت المائل من قعر الصحن، يضيق الفراغ السائل بينهما وتزداد المقاومة الكهربائية بطريقة متوقعة، مما يشير إلى هبوط آمن قبل الاتصال مباشرة. عندما تسد الخلية العنق الضيق، يُقيَّد المسار الكهربائي عبر السائل وتقفز المقاومة فجأة؛ وعند دفع الخلية للخارج، تنخفض المقاومة بنفس الحدة. تسمح النماذج الرياضية لهذه المقاومات — "المقاومة الفجوية" و"مقاومة الشفط" و"مقاومة الحقن" — للحاسوب بتفسير هذه الإشارات في الزمن الحقيقي واتخاذ قرار متى يوقف الشفط أو يطلق الضغط، كل ذلك دون تغذية بصرية.
اختبار الروبوت عمليًا
للاختبار العملي، بنى الباحثون إعدادًا روبوتيًا كاملاً يجمع بين تحكم في الحركة، وتحكم في الضغط، واستشعار المقاومة، وحاسوب مضيف. جربوه على خلايا سرطانية صغيرة تُعرف بخلايا هيلّا (حجمها حوالي 10 ميكرومترات) وعلى خلايا بويضية خنزيرية أكبر بكثير (حوالي 150 ميكرومتر). استطاع النظام اكتشاف الهبوط والالتقاط والإطلاق بشكل موثوق اعتمادًا فقط على إشارات المقاومة عبر نطاق واسع من أحجام الميكروببت. في مقارنات مباشرة، نقل الروبوت خلايا هيلّا بمعدل نجاح 90٪ — أفضل من طريقة آلية سابقة معتمدة على الرؤية — ونقل بويضات خنزير بمعدل نجاح 95٪، أعلى من النهج الميكروسكوبي القياسي. أوقات التشغيل لكل خلية كانت مماثلة أو أسرع من الأساليب التي يتحكم فيها الإنسان، ويرجع ذلك أساسًا إلى أن العنق الضيق يلغي الحاجة لتعديل الشفط بدقة متعددة المرات لوضع الخلية.
حفظ حيوية الخلايا والتوسع
يجب على أي مساعد روبوتي في مختبر الأحياء أن يتجنب إيذاء الخلايا التي يتعامل معها. بعد النقل بالنظام الجديد، رُبّيت خلايا هيلّا والبويضات الخنزيرية ليوم واحد وصُبغت بصبغة تضيء فقط في الخلايا الحية. كانت معدلات البقاء للطريقة الجديدة مساوية أو قريبة من تلك الناتجة عن النقل الموجه بالمجهر وعن الخلايا الضابطة التي لم تُلمس، مما يشير إلى أن الضغط الميكانيكي اللطيف عند العنق الضيق لا يقلل بشكل ملحوظ من حيوية الخلية عندما تُضبط العتبات بشكل صحيح. بالنظر إلى المستقبل، يقترح المؤلفون أن استشعار المقاومة والتحكم بالضغط ذاتهما يمكن بناؤهما داخل شرائح ميكروفلويدية مدمجة. سيسمح ذلك بتشغيل قنوات عديدة بالتوازي، مما يمكن من أنظمة معالجة خلايا مغلقة وعالية الإنتاج تناسب طب التكاثر الآلي، وعلاجات الخلايا، وأجهزة زراعة الخلايا طويلة الأمد حيث يصعب إدخال الميكروسكوبات.
ماذا يعني هذا لعمل الخلايا في المستقبل
لغير المتخصصين، الرسالة الأساسية هي أن نقل الخلايا المفردة لم يعد بحاجة لأن يعتمد على شخص يراقب عبر مجهر. من خلال تشكيل دقيق لأنبوب زجاجي و"الاستماع" إلى كيفية تدفق الكهرباء عبر السائل المحيط، يمكن للروبوت أن يشعر متى هبط، ومتى أمسك خلية، ومتى أطلقها — كل ذلك في الظلام وفي أماكن ضيقة. هذا يجعل من العملي أكثر تصميم أنظمة زراعة خلايا مغلقة وتعمل ذاتيًا تحمي العينات الهشة، وتبسط تدفقات العمل السريرية، وتقرّب عمليات التلاعب بالخلايا على مستوى المختبر إلى تشغيل آلي أشبه بالمصانع.
الاستشهاد: Zhao, Q., Liu, M., Zhu, R. et al. Robotic cell transportation system based on micropipette resistance modeling. Microsyst Nanoeng 12, 65 (2026). https://doi.org/10.1038/s41378-026-01193-5
الكلمات المفتاحية: التلاعب بالخلايا, الميكروببت, الروبوتات, الميكروفلويديك, الأتمتة