Clear Sky Science · ar
الفتك الصناعي بتثبيط MCL-1 وعلاج CAR-T في لمفوما خلايا B العدوانية
لماذا يهم هذا لعلاج السرطان
لمفوما خلايا B العدوانية هي سرطانات دموية سريعة النمو تعود غالبًا بعد العلاج. حتى الاستراتيجيات الحديثة القوية مثل علاج CAR-T، الذي يعيد برمجة خلايا المناعة لدى المريض لمهاجمة السرطان، تفشل لدى نحو نصف المرضى على المدى الطويل. تستكشف هذه الدراسة طريقة لتحويل تلك الضعف إلى ميزة: استخدام دواء يستهدف بروتين بقاء رئيسي في خلايا اللمفوما ليقتل الأورام ويجعل الخلايا المتبقية أسهل للقضاء عليها بواسطة خلايا CAR-T.
مشكلة الخلايا اللمفاوية العنيدة
غالبًا ما تقود فرط فعالية جين يسمى MYC لمفوما خلايا B العدوانية، حيث يدفع هذا الجين الخلايا إلى الانقسام بسرعة ويساعدها أيضًا على الاختفاء من الجهاز المناعي. يمكن للعلاجات القياسية وحتى علاج CAR-T أن تترك وراءها جيوبًا صغيرة من خلايا اللمفوما التي تتحمل الأدوية وتسبب الانتكاس لاحقًا. تعيش هذه الخلايا «المثابرة» والمقاومة في بيئة ورمية مزدحمة بخلايا مناعية تثبط الاستجابة وتمنع خلايا T القاتلة من العمل. تساءل الباحثون عما إذا كان حجب MCL-1، وهو بروتين تعتمد عليه خلايا اللمفوما لتجنب الموت المبرمج، قد يكشف عن ضعف مخفي في هذا النظام.
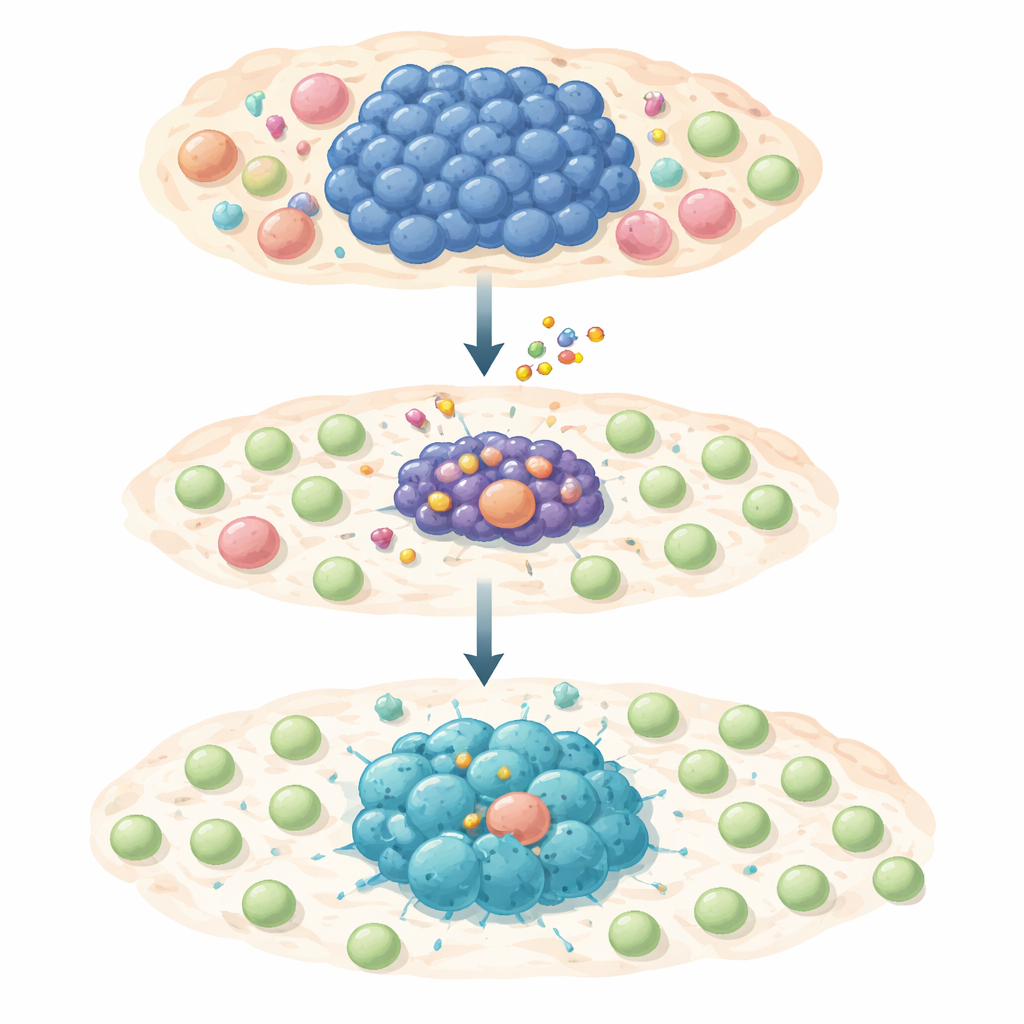
هجوم ثنائي على بقاء الورم وإخفائه
اختبر الفريق دواءً انتقائيًا يحجب MCL-1، S63845، على مجموعة واسعة من خطوط خلايا اللمفوما البشرية المعتمدة على MYC. كانت معظم هذه الخلايا السرطانية شديدة الحساسية للدواء وخضعت للموت المبرمج عندما تم حجب MCL-1. مع ذلك، نجت نسبة صغيرة على المدى القصير أو الطويل وأصبحت متحملة للدواء أو مقاومة تمامًا. عندما فحص الباحثون هؤلاء الناجين بتفصيل، وجدوا أن نشاط MYC قد خفّ بينما تم تفعيل جزيء آخر، STAT1، ومسار إنذار الإنترفيرون المرتبط به. أدى هذا التحول إلى تشغيل جينات تقود إشارات التهابية وكيموكينات — «شرر» جزيئية يمكنها استدعاء خلايا T إلى منطقة الورم.
إيقاظ الحيّ المناعي
لمعرفة كيفية تجسيد ذلك في كائن حي، عالج المؤلفون فئرانًا حاملة لدرنات لمفوما مدفوعة بـ MYC بجرعة منخفضة من مثبط MCL-1. قلص الدواء عبء الورم مع الحفاظ على الخلايا B الطبيعية، لكن تأثيره تجاوز مجرد تقليل الحجم. أظهرت الأورام المعالجة مزيدًا من خلايا CD4 وCD8 T، وقلة في الخلايا T المُنهَكَة، وقلة في الخلايا التنظيمية T، وقلة في الخلايا النخاعية المكبِّحة، وهي كلها علامات على بيئة أكثر ودية للمناعة. أكدت تسلسل RNA على مستوى الخلية الواحدة للخلايا الورمية والمحيطة أن الخلايا اللمفاوية المتبقية أظهرت انخفاضًا في MYC وزيادة في STAT1 وإشارات إنترفيرون والتهابية أقوى، بينما أعيد تجديد النسيج المحيط بخلايا T نشطة وخلايا قاتلة طبيعية بدلًا من الخلايا المكبِّحة.
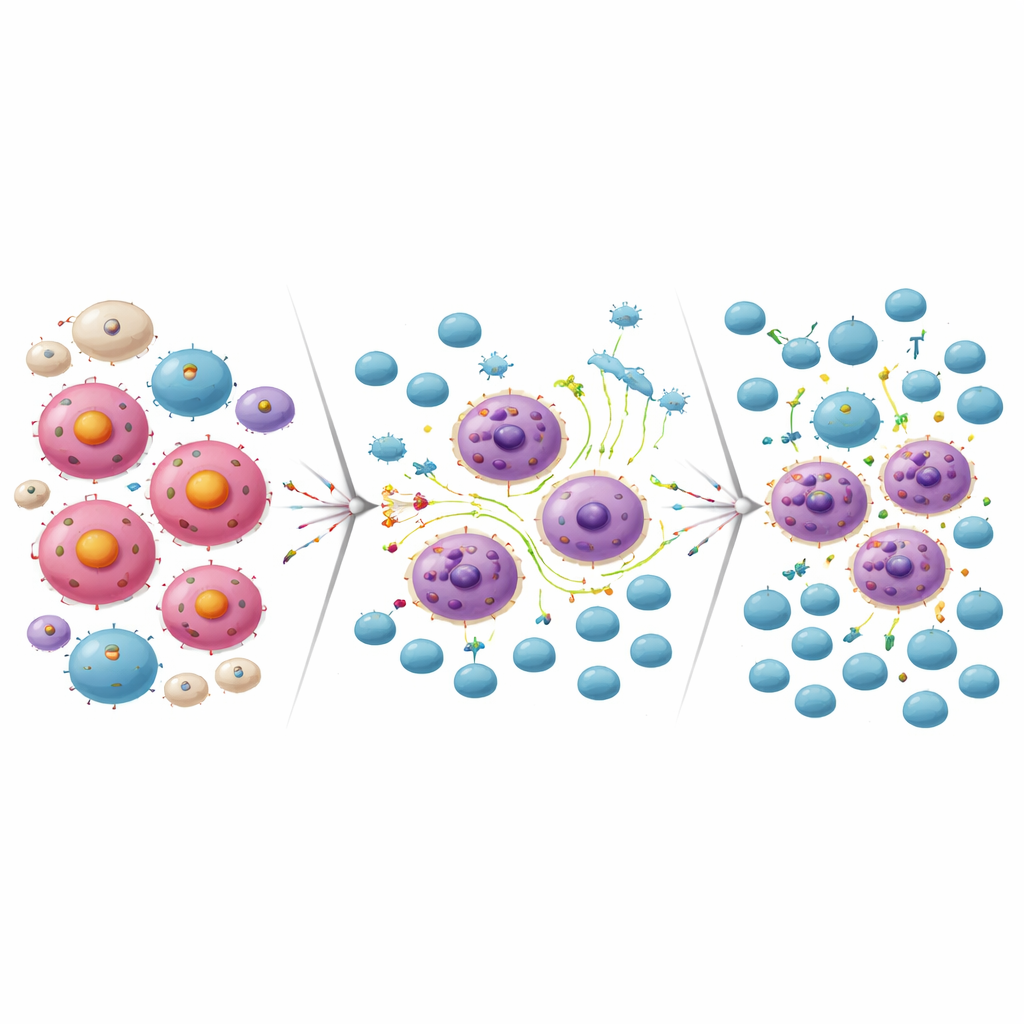
تحويل المقاومة إلى فرصة لخلايا CAR-T
جعلت إعادة البرمجة الالتهابية نفسها التي ساعدت بعض خلايا اللمفوما على النجاة من حجب MCL-1 تلك الخلايا أكثر عرضة للهجوم المناعي. في المختبر، قتلت خلايا CAR-T الموجهة ضد CD19 بكفاءة خلايا اللمفوما التي أصبحت مقاومة لدواء MCL-1. وبالمقابل، كانت خلايا اللمفوما التي طورت مقاومة لعلاج CAR-T ضد CD19 شديدة الحساسية لمثبط MCL-1. عندما جمع الباحثون جرعة دون مميتة من دواء MCL-1 مع خلايا CAR-T في مزارع خلوية، قضيا معًا على عدد أكبر بكثير من خلايا اللمفوما مقارنة بكل علاجٍ على حدة. في نماذج الفئران، أدى إعطاء مثبط MCL-1 يتبعه خلايا CAR-T ضد CD19 إلى إزالة تكاد تكون كاملة للورم وبقايّة أطول بشكل ملحوظ مقارنة بالعلاجات الفردية.
ضربة مزدوجة ذات إمكانات علاجية
ببساطة، تقترح الدراسة استراتيجية «ضربة مزدوجة». أولًا، يضرب دواء حابس لـ MCL-1 معظم اللمفوما ويجبر الخلايا السرطانية الناجية على الدخول في حالة ملتهبة ومرئية بشدة تجذب خلايا T وتزيل الدرع المناعي الواقٍ. ثانيًا، تستغل خلايا CAR-T ضد CD19 هذا الضعف المكتشف حديثًا لاستئصال المرض المتبقي. بضرب كلٍّ من دوائر بقاء الورم الداخلية وحيّه الوقائي، قد يقلل هذا النهج المركب الانتكاسات ويقرب لمفوما خلايا B العدوانية من نواتج مرضية طويلة الأمد.
الاستشهاد: Gao, J., Zhao, X., Yin, Q. et al. Synthetic lethality of MCL-1 inhibition and CAR-T therapy in aggressive B-cell lymphoma. Leukemia 40, 638–648 (2026). https://doi.org/10.1038/s41375-026-02884-8
الكلمات المفتاحية: لمفوما خلايا B, علاج CAR-T, تثبيط MCL-1, البيئة الدقيقة للورم, مقاومة الدواء