Clear Sky Science · ar
تنشيط مستمر وقوي لإشارة NF-κB داخل الخلايا البائية يقود إلى تكون لمفوما شبيهة بـ SLL/CLL ويتغلب على الاعتماد على البيئة الدقيقة
عندما تنحرف خلايا الجهاز المناعي
يعتمد جهازنا المناعي على الخلايا البائية للتعرّف على الجراثيم وتكوين ذاكرة للعدوى السابقة. تستقصي هذه الدراسة ما يحدث عندما يكون مفتاح تحكّم رئيسي داخل الخلايا البائية، يُدعى NF-κB، عالقًا في وضع "تشغيل". تُظهر النتائج كيف يمكن لهذا الإشارة المستمرة أن تحوّل الخلايا البائية الطبيعية إلى خلايا شبيهة باللوكيميا واللمفوما تشبه اللمفوما اللمفاوية المزمنة البشرية (CLL)، وكيف يمكنها حتى تحرير هذه الخلايا السرطانية من الدعم الطبيعي الذي تحصل عليه من محيطها. قد تشير فهم هذه العملية إلى طرق جديدة لعلاج سرطانات الدم التي يصعب شفاؤها.
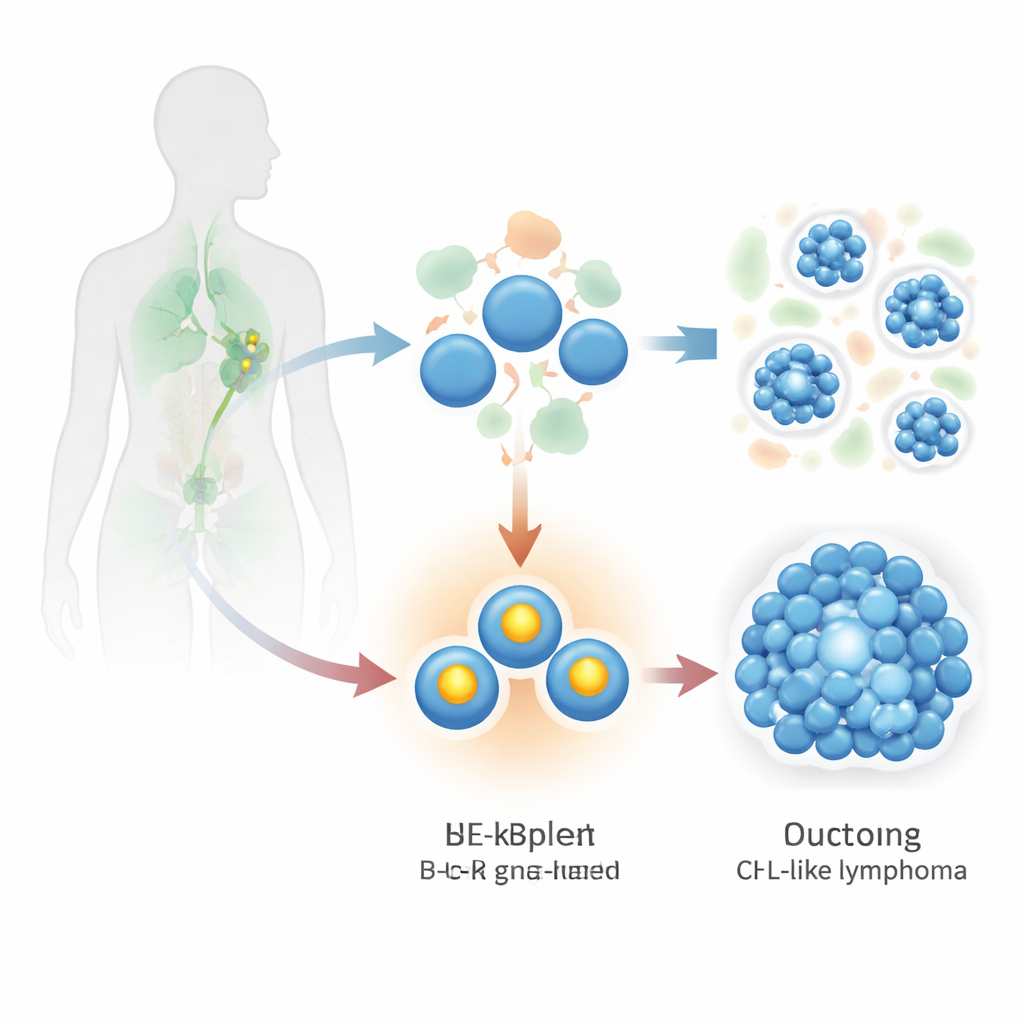
مفتاح تحكّم رئيسي في خلايا الجهاز المناعي
يعمل NF-κB كعائلة من البروتينات تشبه مفتاحًا رئيسيًا للجينات التي تتحكم في بقاء الخلايا ونموها والاستجابات المناعية. في الظروف الصحية، يتفعل NF-κB فقط عندما تتلقى الخلايا البائية إشارات من عدوى أو من خلايا مساعدة في العقد اللمفاوية. ومع ذلك، في العديد من اللمفوما البشرية وCLL، يكون NF-κB نشطًا بشكل مزمن. طرح المؤلفون سؤالًا بسيطًا لكنه قويًا: إذا أجبروا NF-κB على أن يبقى نشطًا باستمرار وخصوصًا في الخلايا البائية للفأر، هل سيكون ذلك وحده كافيًا لبدء السرطان، وهل ستؤثر شدة تلك الإشارة؟
رفع مستوى الإشارة في الخلايا البائية
لاختبار ذلك، مهندس الباحثون فئرانًا تنتج خلاياها البائية نسخة دائمة النشاط من بروتين يُدعى IKK2، وهو محرك رئيسي لمسار NF-κB "القصصي". حمل بعض الفئران نسخة واحدة من الجين المعدّل لـ IKK2، بينما حمل البعض الآخر نسختين، مُحدثين مستويات أضعف أو أقوى من نشاط NF-κB. في الحيوانات الصغيرة سنًا، أدت كلا المستويين إلى تضخّم الطحال وزيادة مجموعات معينة من الخلايا البائية، لكن الإشارة القوية تسببت في توسع لافت لفرعيّة خاصة من الخلايا البائية تُعرف بالخلايا B1a. تعيش هذه الخلايا عادةً في التجاويف الجسدية ويُعتقد أنها مصدر محتمل لـ CLL البشري. أكدت التحليلات الجينية أن جينات الهدف لدى NF-κB قد فُعّلت بطريقة تعتمد على الجرعة: وجود IKK2 نشط مرتين أدى إلى برامج جينية لـ NF-κB أقوى بوضوح.
من فرط النمو إلى سرطان شبيه بـ CLL
مع تقدّم الفئران في العمر، طور أولئك الذين لديهم أقوى إشارة NF-κB تقريبًا بشكل موحّد مرضًا بطيء النمو لكنه قاتل في النهاية ويشبه عن كثب اللمفوما اللمفاوية الصغيرة والـ CLL لدى البشر. أصبح طحالهم متضخمًا بشكل هائل ومملوءًا بخلايا صغيرة شبيهة بـ B1a موجبة لـ CD5 غزت أعضاء أخرى. كما طورت الفئران الحاملة لنسخة واحدة فقط من جين IKK2 النشط مرضًا أيضًا، لكن في عمر متأخر وبأنواع أورام أكثر تنوعًا. أظهرت الخلايا البائية السرطانية أنماطًا متكررة في مستقبلات المستضد لديها، مماثلة لما يُرى في CLL البشري، مما يشير إلى أن جزيئات ذات طابع ذاتي أو مُعدّلة منها تساعد في انتقاء وتوسيع هذه النسائل. عندما نُقلت هذه الخلايا الورمية إلى فئران جديدة، نمت عدوانيًا، مؤكدة أنها لمفوما حقيقية.
تعزيز نموذج معروف لللوكيميا
دمج الفريق بعد ذلك نشاط NF-κB المستمر مع محرك آخر معروف للوكيميا، بروتين يُدعى TCL1، الذي بمفرده يسبب مرضًا شبيهًا بـ CLL في الفئران. أدى إضافة نسخة أو نسختين من IKK2 النشط إلى تسريع المرض بشكل كبير: ماتت الفئران في وقت مبكر بكثير وأظهرت انتشارًا هائلًا لخلايا مناعية خبيثة شبيهة بـ B1a عبر الطحال والعقد اللمفاوية ونخاع العظم والتجاويف الجسدية. كشفت تحليلات التعبير الجيني أن هذه الأورام المزدوجة أطلقت العديد من المسارات المرتبطة بانقسام الخلايا والالتهاب وأشكال CLL البشرية العدوانية ذات التكهن السيئ، بما في ذلك بصمات مرتبطة بالتحول إلى متلازمة ريتشر السريعة النمو. حتى عندما نُشّط NF-κB في جزء صغير فقط من الخلايا المرشحة، تفوقت تلك الخلايا بسرعة على الباقي، مما يُظهر ميزة نمو ذاتية قوية خلوية المنشأ.
التحرر من الاعتماد على البيئة المحيطة
عادةً ما تعتمد خلايا CLL في المرضى اعتمادًا كبيرًا على خلايا الدعم المحيطة، مثل الخلايا البينية في العقد اللمفاوية ونخاع العظم، التي توفر إشارات البقاء والنمو. في نموذج سابق، تطلّب هذا الدعم بروتينًا يُدعى PKC-β في الخلايا غير السرطانية؛ بدونه، فشلت خلايا CLL المزروعة في النمو. في هذه الدراسة الجديدة، استطاعت خلايا اللوكيميا المدفوعة بواسطة TCL1 والتي حملت كذلك تنشيطًا شديدًا لـ NF-κB أن تنمو حتى في فئران تفتقر تمامًا إلى PKC-β، بينما لم تستطع خلايا TCL1 العادية ذلك. في زراعات المختبر، كانت الخلايا التي تحمل كل من TCL1 وأعلى إشارة NF-κB وحدها قادرة على الاستمرار في الانقسام لأيام عديدة دون تحفيز إضافي. تُبيِّن هذه النتائج أن النشاط الداخلي المكثف لـ NF-κB يمكن أن يحل محل الإشارات الأساسية عادةً من البيئة الدقيقة ويجعل خلايا اللوكيميا أكثر اعتمادًا على نفسها.
ما الذي يعنيه هذا للمرضى
تُبرهن هذه الدراسة أن الإشارة القوية والمستمرة لـ NF-κB في الخلايا البائية ليست مجرد مرافق بل يمكن أن تكون محركًا مباشرًا لللمفوما والمرض الشبيه بـ CLL. من خلال تعزيز نمو وتجدد خلايا شبيهة بـ B1a، والتعاون مع جينات مُروّجة للسرطان مثل TCL1، وتقليل اعتماد الورم على محيطه، يساعد NF-κB في نشوء أمراض أكثر عدوانية ومقاومة للعلاج. للمرضى، يوحي ذلك بأن العلاجات التي تهدف إلى كبح إشارات NF-κB، أو حجب العوامل الرئيسية التي تفعّلها، قد تكون ذات قيمة خاصة في حالات CLL عالية الخطورة واللمفوما المرتبطة بها، خصوصًا في الحالات التي لم تعد تستجيب للأدوية التي تستهدف بيئة الورم.
الاستشهاد: Soberón, V., Osswald, L., Moore, A. et al. Strong constitutive NF-κB signaling in B cells drives SLL/CLL-like lymphomagenesis and overcomes microenvironmental dependencies. Leukemia 40, 522–539 (2026). https://doi.org/10.1038/s41375-025-02844-8
الكلمات المفتاحية: اللمفوما اللمفاوية المزمنة, الخلايا البائية, NF-kappaB, بيئة الميكروالورم, نموذج الفأر TCL1