Clear Sky Science · ar
الطفر ة JAK2V617F تعيد برمجة العامل الحساس لنقص الأكسجين HIF-1 لتوليد مجموعة تنظيمية غير تقليدية للنقص الأكسجين في الأورام المكونة للدم
لماذا يهم هذا الأمر في سرطان الدم
بعض سرطانات الدم التي تنمو ببطء، المعروفة باسم الأورام المفرطة التكوُّن المكونة للدم، قد تتوهج بصمت لسنوات قبل أن تتحول فجأة إلى ليمفوما أو سرطان دم عدواني. يطرح هذا البحث سؤالاً بسيطاً لكنه حاسم: كيف تستولي طفرة شائعة المحرِّكة للسرطان على نظام الخلية المدمج لاستشعار الأكسجين، وهل يمكن استهداف هذا الاستيلاء تحديداً دون الإضرار بالخلايا السليمة؟ قد تفتح الإجابات طريقاً جديداً لعلاج المرضى ذوي المخاطر العالية مع الحفاظ على الأنسجة الطبيعية التي تعتمد أيضاً على إشارات استشعار الأكسجين.
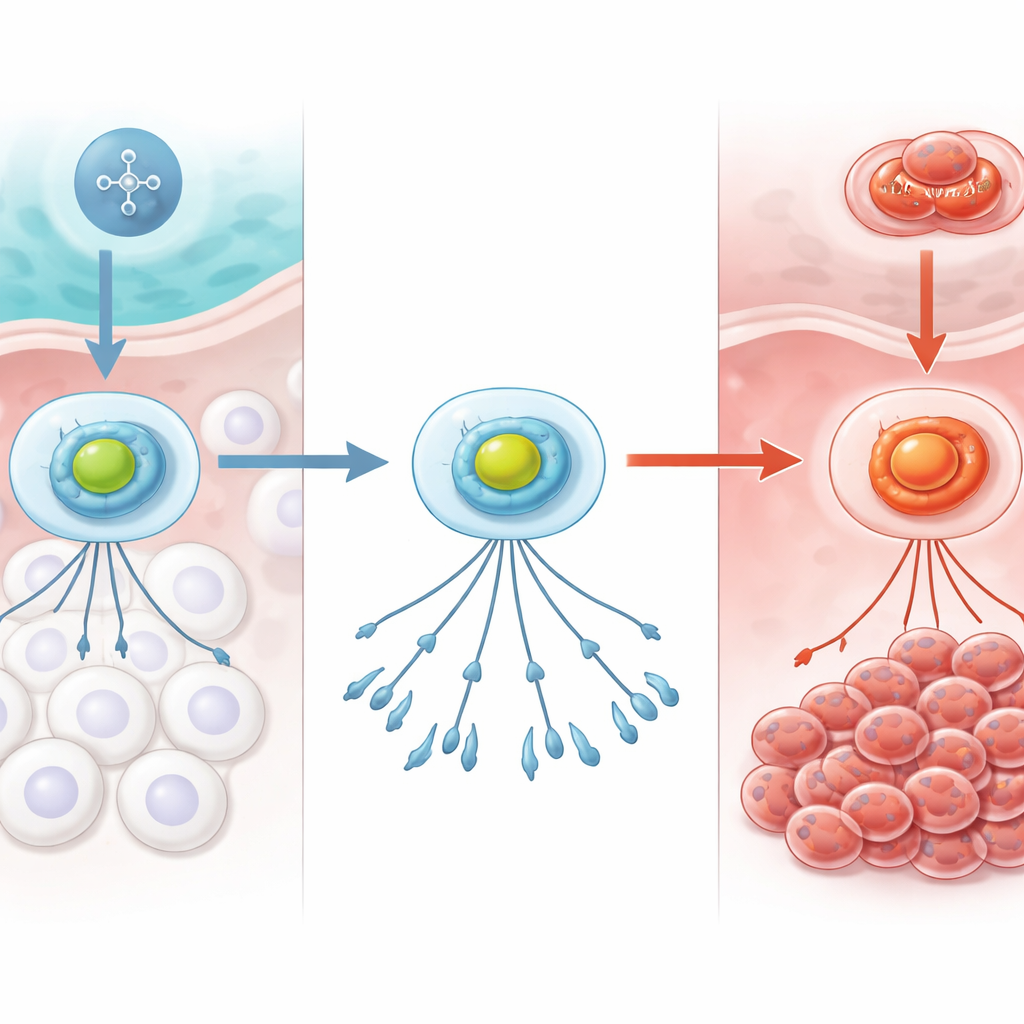
نظام إنذار الجسم للأكسجين
تراقب الخلايا باستمرار كمية الأكسجين المتاحة. في قلب هذا النظام يوجد مركب بروتيني يُدعى HIF‑1، والذي يتصرف مثل إنذار للأكسجين. في الظروف العادية المشبعة بالأكسجين، يتم تكسير وحدة فرعية من HIF‑1 بسرعة، ما يبقي الإنذار مطفأً. عندما ينخفض الأكسجين، يتوقف هذا التحطيم، يستقر HIF‑1، ينتقل إلى حمض الخلايا النووي (DNA)، ويفعِّل جينات تساعد الخلايا على التكيف، على سبيل المثال بتغيير كيفية استخدام الطاقة أو بناء أوعية دموية جديدة. في السرطان، يمكن استغلال هذا النظام لصالح الورم، مما يساعد الخلايا الخبيثة على التعامل مع بيئات ضاغطة مثل نخاع العظم منخفض الأكسجين.
عندما تعيد طفرة توصيل الإنذار
ركز الباحثون على طفرة تُسمى JAK2V617F، وهي شائعة جداً في الأورام المفرطة التكوُّن المكونة للدم. أظهرت أعمال سابقة أن هذه الطفرة تُبقي إنذار HIF‑1 مفعّلاً حتى عندما يتوفر الأكسجين بكثرة. باستخدام خطوط خلوية معدّلة وراثياً، قارن الفريق ربط HIF‑1 بالحمض النووي في حالتين: نقص الأكسجين الحقيقي، والأكسجين الطبيعي بوجود طفرة JAK2V617F. وجدوا أنه في الخلايا الطافرة يرتبط HIF‑1 بعدد أقل من المناطق في الجينوم، ويصبح أقل استجابة لتغيرات الأكسجين، ويتفاعل مع مجموعة مختلفة من البروتينات الشريكة، معظمها يشارك في معالجة الرنا. بعبارة أخرى، لا تقوم الطفرة ببساطة بتشغيل HIF‑1 بشكل دائم — بل تعيد ضبط الإنذار نحو مجموعة مختلفة من الأهداف.
برنامج جيني خاص بالسرطان
من هذه التجارب، عرّف المؤلفون عدداً من مجموعات الجينات المعتمدة على HIF‑1، بما في ذلك ما أسموه بصمة النقص الأكسجيني JAK2V617F. ثم درسوا مدى انشغال هذه البصمات في خلايا الدم من 172 مريضاً مصابين بأورام مفرطة التكوُّن إيجابية لـ JAK2V617F. على نحو مفاجئ، لم تكن برامج جينات HIF‑1 المرتبطة عادةً بنقص الأكسجين تتنبأ بمدى مرضية المرضى أو بمدى بقائهم على قيد الحياة. بالمقابل، فصلت بصمة النقص الأكسجيني الخاصة بالطفرة المرضى ذوي الحالات الأشد ارتباطاً وكان لها صلة بسوء البقاء العام. الكثير من الجينات في هذه المجموعة كانت نشطة بشكل خاص في خلايا سلف المحببات الكبرى (megakaryocyte progenitors)، وهي خلايا نخاع العظم التي تنمو بشكل مفرط وتقود التندب في هذه الاضطرابات، وبعضها يشارك في إصلاح تلف الحمض النووي — عملية يمكن أن تساعد الخلايا السرطانية على النجاة من الضغوط الضارة.
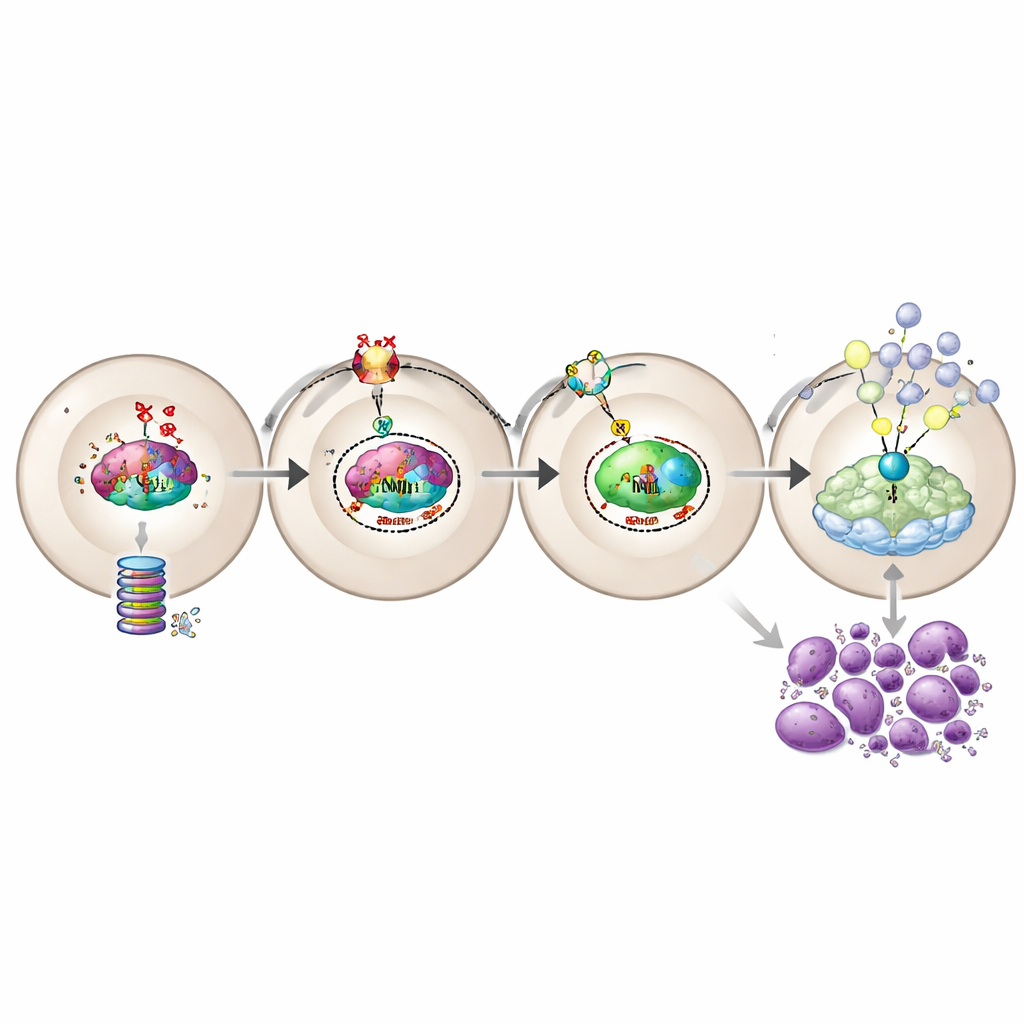
دلائل للتدهور المفاجئ في المرض
خوف رئيسي لدى المرضى هو التحول المفاجئ من مرض مزمن إلى لمفوما/سَرْطان دم عدواني من نوع "طور الانفجار". من خلال تحليل عينات متطابقة من المرضى قبل وبعد هذا التحول، استخلص الفريق مجموعة أصغر مكونة من 13 جيناً، أطلقوا عليها اسم بصمة HIF1‑MPN‑BP، التي ارتفعت أو انخفضت مع التحول. كانت هذه المجموعة مرتبطة بقوة بنقاط مخاطرة أعلى، وببقاء أسوأ، وبالتندب الأشّد في نخاع العظم. والأهم أن هذا النمط بدا خاصاً بأمراض مدفوعة بطفرة JAK2V617F، وليس سمة عامة لكل أنواع السرطانات الدموية. العديد من الجينات في هذه المجموعة هي أهداف دوائية محتملة، مما يشير إلى قائمة مركزة من المرشحين للعلاجات المستقبلية التي تهدف إلى منع التقدم.
إيجاد المساعد الخفي للطّفرة
كيف تُبقي JAK2V617F HIF‑1 نشطاً بشكل مستقل عن الأكسجين؟ باستخدام أساليب كيمياء البروتين، اكتشف المؤلفون أنه في الخلايا الطافرة يحمل HIF‑1 علامتين كيميائيتين غير معروفتين من قبل (فسفرة) داخل منطقة عادةً ما تتحكم في تحلله. تتبعوا هذه التغييرات إلى PIM1، إنزيم كيناز يُفعَّل أسفل مسار إشارة JAK2. أدى حجب PIM1 بأدوية تجريبية إلى خفض مستويات HIF‑1 في الخلايا الطافرة، بينما ترك الاستجابة الطبيعية لنقص الأكسجين إلى حد كبير سليمة. كما قلل تثبيط PIM1 انتقائياً من تعبير جينات HIF1‑MPN‑BP الخطرة ودفع الخلايا الطافرة نحو موت الخلايا، مع إبقاء نظيراتها غير الطافرة سالمة إلى حد كبير.
ماذا يعني هذا للمرضى
تُظهر هذه الدراسة أن نفس بروتين استشعار الأكسجين، HIF‑1، يتصرف بشكل مختلف جداً اعتماداً على كيفية تفعيله. في الأورام المفرطة التكوُّن المدفوعة بـ JAK2V617F، يثبّت محور الإشارة JAK2–PIM1 HIF‑1 بطريقة تنقله بعيداً عن السيطرة الطبيعية بالأكسجين وتقيّص نشاطه إلى مجموعة جينات معززة للمرض. وبما أن هذا البرنامج المعدّل مرتبط بشدة بشدة المرض وخطر التحول، ويمكن تخفيفه عن طريق حجب PIM1، فإنه يقدم مساراً واعداً لاستهداف نشاط HIF‑1 الخبيث مع الحفاظ على دوره الأساسي في الأنسجة السليمة. قد تساعد العلاجات التي تستغل هذا الاختلاف يوماً ما في منع تدهور سرطانات الدم بطيئة الالتهاب إلى ليمفوما مهددة للحياة.
الاستشهاد: Kealy, D., Ellerington, R., Bansal, S. et al. JAK2V617F reprograms Hypoxia Inducible Factor-1 to induce a non-canonical hypoxia regulon in myeloproliferative neoplasms. Leukemia 40, 609–621 (2026). https://doi.org/10.1038/s41375-025-02843-9
الكلمات المفتاحية: أورام مفرطة التكوُّن المكونة للدم, JAK2V617F, HIF-1, كيناز PIM1, التحوّل إلى طور الطفرات الانفجارية