Clear Sky Science · ar
ألنكتاماب، مُحرّك خلايا تي ثنائي التكافؤ يستهدف مستضد نضج الخلايا البائية لمرضى المايلوما المتكررة أو المقاومة: نتائج دراسة أولى من المرحلة 1 على البشر
لماذا يهم هذا الدواء الجديد للسرطان
بالنسبة للأشخاص الذين يعيشون مع المايلوما المتعددة، وهو سرطان دم يعود في معظم الأحيان بعد العلاج، كل خيار جديد قد يعني وقتاً أطول وجودة حياة أفضل. تختبر هذه الدراسة علاجاً مناعياً من الجيل التالي يُدعىألنكتاماب، مصمّم لمساعدة خلايا الدفاع في الجسم على العثور على خلايا المايلوما وقتلها. يطرح البحث سؤالاً عملياً يهم المرضى والأطباء على حد سواء: هل يمكن إعطاء هذا العلاج القوي عن طريق حقنة بسيطة تحت الجلد، مع تأثيرات مضادة للسرطان قوية ولكن بآثار جانبية خطيرة أقل؟
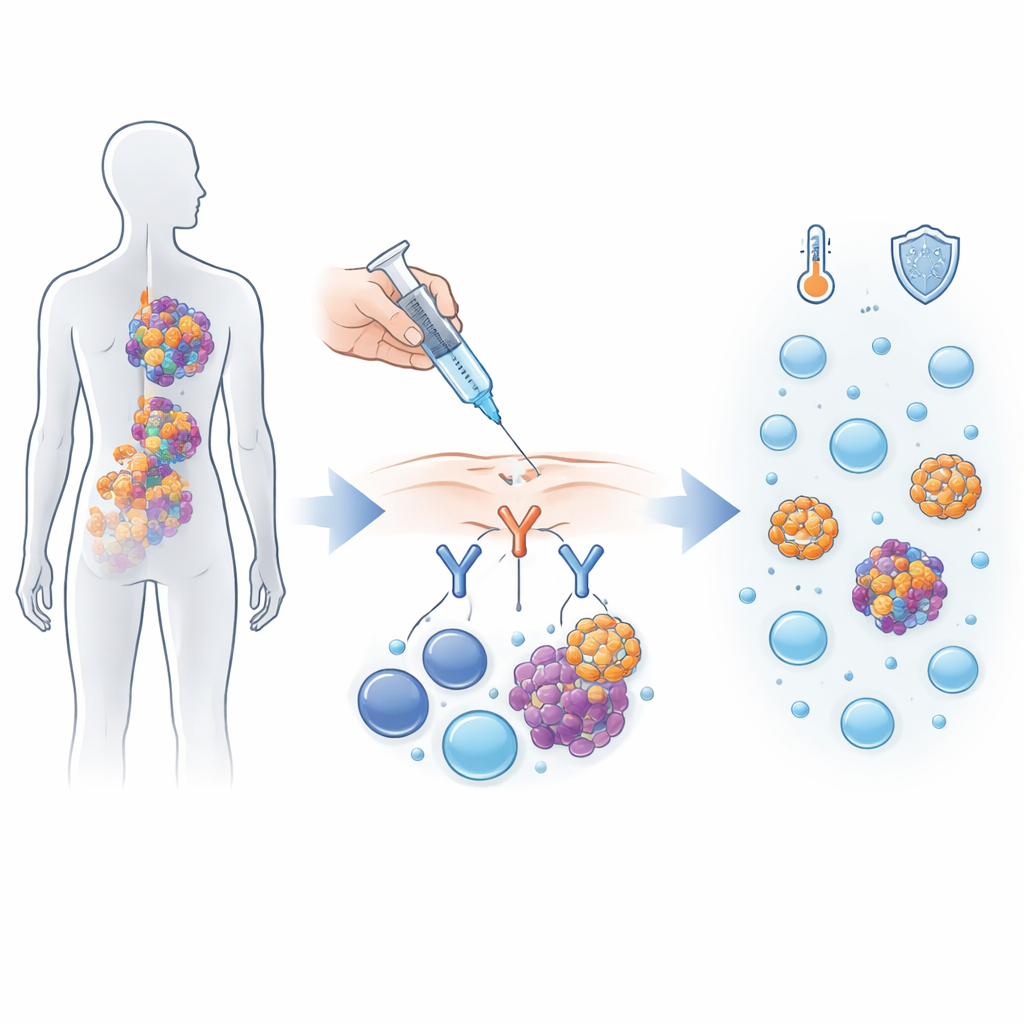
طريقة ذكية لإعادة توجيه الجهاز المناعي
ينتمي ألنكتاماب إلى فئة جديدة من الأدوية تعمل كوسيط جزيئي بين خلايا السرطان والخلايا المناعية. تحمل خلايا المايلوما علامة على سطحها تُسمى BCMA، بينما تحمل خلايا تي علامة مختلفة تسمى CD3. ألنكتاماب مبني ب"ذراعين" تلتصقان بـBCMA و"ذراع" يلتصق بـCD3، مما يقرب خلايا تي من خلايا المايلوما لتمكينها من مهاجمتها. في هذه التجربة الأولى على البشر، تلقى 165 شخصاً مصابين بالمايلوما التي عادت بعد ثلاث فئات علاجية على الأقل ألنكتاماب، إما عن طريق التسريب الوريدي أو عن طريق حقن تحت الجلد.
من التسريب إلى الحقن
في البداية، كان يُعطى الدواء عبر الوريد، لكن هذا النهج تسبب في تفاعلات مناعية أعنف، بما في ذلك حادثة تهدد الحياة لمضاعفة تُدعى متلازمة تحرير السيتوكينات، حيث يفرز الجهاز المناعي فجأة كميات كبيرة من إشارات الالتهاب. وبسبب هذه المخاوف على السلامة وفائدة متواضعة فقط، تحوّلت الدراسة إلى الجرعات تحت الجلد، التي تُطلق الدواء بشكل أكثر تدريجاً. عُولج خمسة وتسعون مريضاً بهذه الطريقة باستخدام جدول "تصعيد خطوة بخطوة": جرعات مبدئية صغيرة تليها جرعات مستهدفة أعلى، مع تقليل تردد الحقن تدريجياً مع مرور الوقت من أسبوعي إلى مرة كل أربعة أسابيع إذا استمر العلاج.
كيف كان أداء المرضى وما واجهوه
من بين جميع المرضى الذين تلقوا الحقن تحت الجلد، شهد نحو 59% انكماشاً في السرطان بنسبة لا تقل عن النصف، وأصبح ما يقرب من النصف "سلبياً من حيث المرض المتبقي الأدنى"، ما يعني أن اختبارات حساسة للغاية لم تعد تجد خلايا المايلوما في نقي العظم لديهم. عند الجرعة الموصى بها وهي 30 ملليغرام، كانت الاستجابات أقوى: استجاب نحو 71% وأحرز أكثر من نصف المرضى سلبية المرض المتبقي الأدنى. حافظ كثير من المرضى على ضبط المرض لفترة تقارب السنة أو أكثر، حتى مع تخفيف جدول الجرعات. كانت الآثار الجانبية شائعة لكنها في الغالب قابلة للإدارة. حدثت تفاعلات مناعية شبيهة بالحمى في نحو ثلاثة من كل خمسة مرضى، لكنها كانت جميعها خفيفة أو متوسطة. وقعت حالات انخفاض في عدد خلايا الدم البيضاء والتهابات، ما يعكس قوة الدواء وضعف جهاز المناعة لدى المرضى، ومع ذلك كانت الالتهابات الخطيرة أقل تكراراً مما أُبلغ عنه مع عدة أدوية مشابهة.
لماذا كان مسار الحقن أكثر أماناً
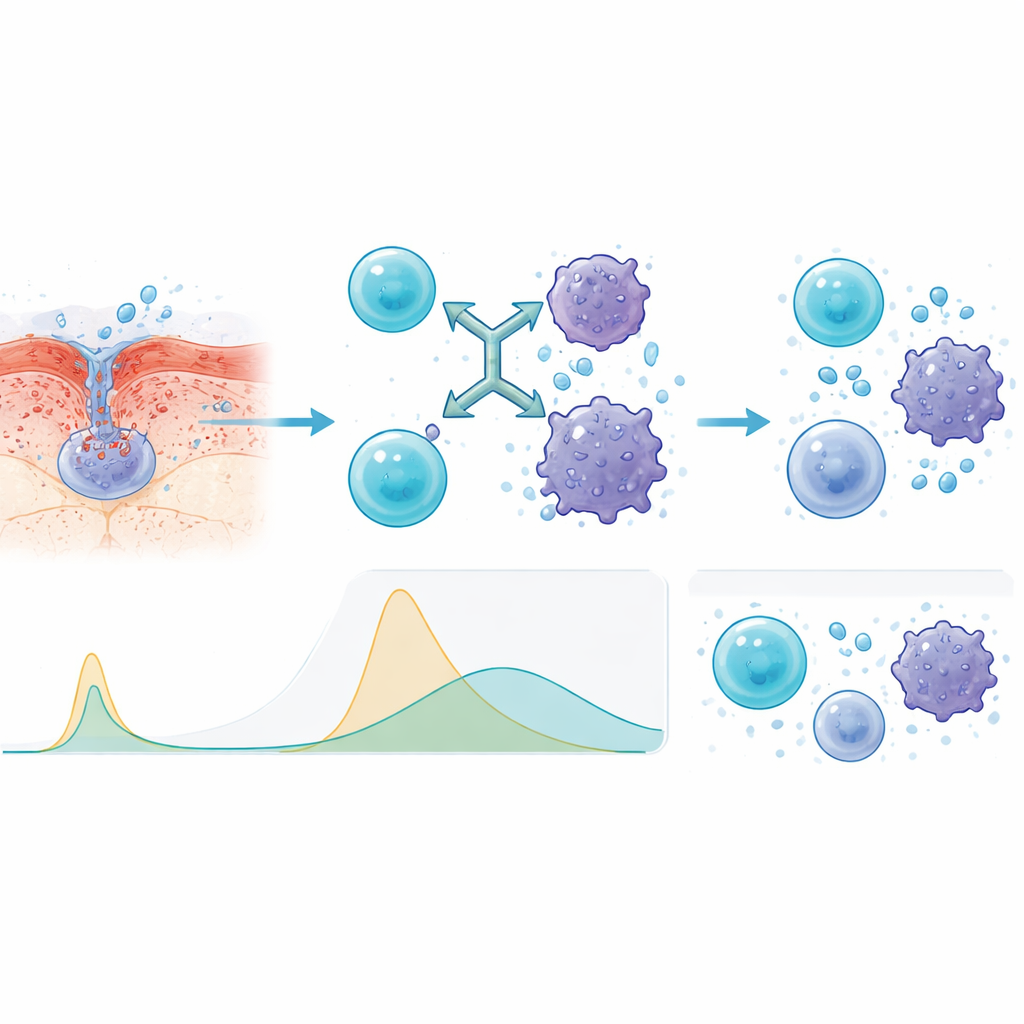
لفهم سبب أفضلية طريقة الحقن تحت الجلد، قاس الباحثون جزيئات الإشارة المناعية في الدم. مقارنةً بالتسريب الوريدي، أنتجت الحقن قمماً أبطأ وأقل في إشارات الالتهاب الأساسية مثل الإنترلوكينات وعامل نخر الورم. يعني هذا النمط المسطح أن الجهاز المناعي لا يزال مفعلاً ضد السرطان، لكن بدون الاندفاع المفاجئ ذاته الذي قد يجعل المرضى يمرضون بشدة. كما وجد الفريق أن الأشخاص الذين أظهر دمهم مستويات أقل من BCMA المتساقط في البداية — وهو علامة على مرض أقل عدوانية أو أقل تقدماً — كانوا يميلون إلى الاستجابة بشكل أفضل والبقاء في سكون طويل الأمد.
ماذا يعني هذا لرعاية المايلوما مستقبلاً
على الرغم من أن الشركة قررت منذ ذلك الحين عدم الاستمرار في تطوير ألنكتاماب لأسباب استراتيجية، فإن الدروس المستفادة من هذه التجربة مهمة. تُظهر الدراسة أن محرّكاً مناعياً مصمماً بعناية يمكن أن يُعطى كحقنة بسيطة، وفق جدول يصبح أقل طلباً مع مرور الوقت، مع الحفاظ على استجابات عميقة وطويلة الأمد في كثير من الأشخاص المصابين بمايلوما يصعب علاجها. وتشير أيضاً إلى أن تصعيد الجرعة تدريجياً وتفادي القمم الحادة في تنشيط المناعة يمكن أن يحد من التفاعلات الخطيرة دون أن يضعف القوة المضادة للسرطان. من المرجح أن توجه هذه الرؤى تصميم علاجات مناعية مستقبلية، مما يقدّم أملاً في أن يحصل المزيد من المرضى المصابين بالمايلوما المتكررة على علاجات فعّالة ليست قوية فحسب، بل أيضاً أكثر أماناً وأسهل للتعايش معها.
الاستشهاد: Bar, N., Martin, T., Hofmeister, C.C. et al. Alnuctamab, a bivalent B-cell maturation antigen-targeting T cell engager for patients with relapsed or refractory multiple myeloma: results from a phase 1, first-in-human study. Leukemia 40, 481–490 (2026). https://doi.org/10.1038/s41375-025-02841-x
الكلمات المفتاحية: المايلوما المتعددة, العلاج المناعي, جسم مضاد ثنائي التحديد, BCMA, محرّك خلايا تي