Clear Sky Science · ar
محفز Notch القابل للذوبان يُمكّن نضوج الأميلوبلاست البشري وتكوّن نسيج شبيه بالمينا لتجديد الأسنان
لماذا إصلاح مينا الأسنان صعب للغاية
المينا، الغلاف الأبيض اللامع الذي يغطي أسناننا، هو أصلب مادة في جسم الإنسان—ولكن بمجرد أن تفقده الأسنان، لا يمكن استعادته طبيعياً. يعاني أكثر من 90% من البالغين من فقدان أو تلف في المينا، ومع ذلك لا تمتلك أسناننا وسيلة طبيعية لإعادة بناء هذه الدرع الواقية. تصف هذه الدراسة طريقة لزراعة خلايا بشرية مفرزة للمينا في المختبر، ودفعها إلى حالة ناضجة تماماً، وحتى تحفيزها على تكوين معدن شبيه بالمينا في الحيوانات. يفتح هذا العمل مساراً نحو علاجات مستقبلية قد تصل يومًا إلى إصلاح الأسنان بأنسجة حية بدلاً من الحشوات والتيجان.
بناء مينا الأسنان من الخلايا الجذعية
تُصنع المينا بواسطة خلايا متخصصة تُدعى الأميلوبلاستات، التي تموت بعد بزوغ السن عبر اللثة. بدونها، لا تستطيع الأسنان البالغة تكوين مينا جديدة. استخدم الباحثون خلايا جذعية مستحثة متعددة القدرات بشرية—خلايا بالغة أعيد برمجتها إلى حالة شبيهة بالجنين—لخلق «أميلوبلاستات مستحثة». في أعمال سابقة، كانت هذه الخلايا المزروعة مخبرياً قادرة على البدء في التشبه بالخلايا الطبيعية المكوّنة للمينا لكنها توقفت قبل الوصول إلى النضج الكامل، وكانت تعمل بشكل صحيح فقط عندما تُنمو على اتصال وثيق مع الأودونتوبلاستات، الخلايا التي تُشكّل العاج الأساسي. هذا أثار سؤالاً رئيسياً: ما الذي توفره الأودونتوبلاستات تماماً بحيث تحتاجه الأميلوبلاستات لاستكمال تطورها؟
الحوار المفقود بين خلايا السن
لفك شفرة هذا الحوار الخلوي، استفاد الفريق من خرائط التعبير الجيني خلية بخلية للأسنان النامية لدى البشر والفئران. بحثوا عن مسارات إشارات تبدو أنها تعمل تحديدًا من الأودونتوبلاستات إلى الأميلوبلاستات خلال النافذة الزمنية الحرجة لتكوّن المينا. برز مسار واحد: Notch، وهو نظام اتصال مباشر خلية إلى خلية يستخدم على نطاق واسع في التطور الجنيني. في هذه الخرائط السنية، كانت الليجاندات الشبيهة بالدلتا (وخاصة DLL1 وDLL4) موجودة أساساً على الأودونتوبلاستات، بينما تركزت مستقبلات Notch على الأميلوبلاستات الناضجة. عندما عطل الباحثون نشاط Notch بدواء في نظام التشارك الخلوي لديهم، قلّ إنتاج الأميلوبلاستات للبروتين الرئيسي للمينا، إناملين، بشكل حاد—دليل قوي على أن إشارة Notch أساسية لنضوج الخلايا المكوّنة للمينا. 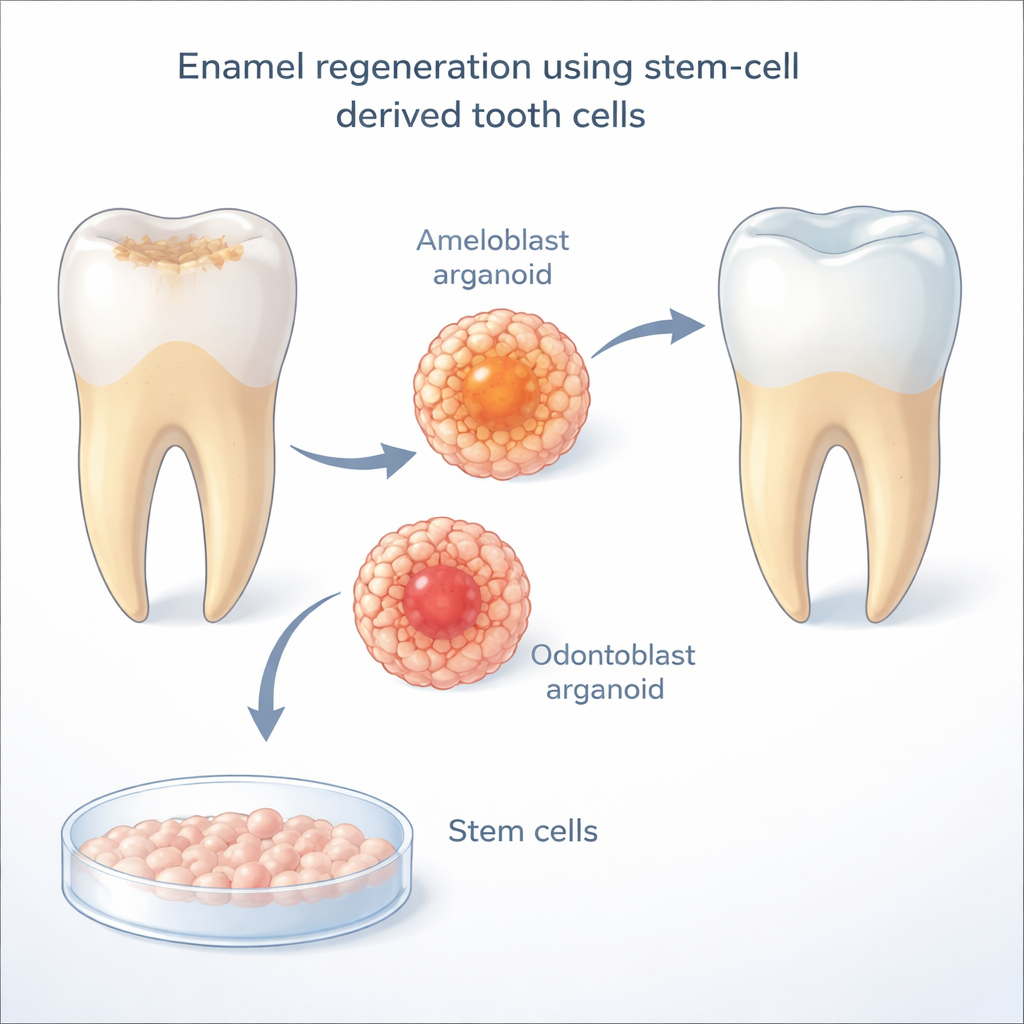
مفتاح بروتيني مصمَّم بالذكاء الاصطناعي لخلايا المينا
للانتقال خطوة أبعد، أراد الفريق تشغيل Notch بطريقة دقيقة وقابلة للتحكم، دون الاعتماد على أودونتوبلاستات حقيقية. استخدموا بروتينًا اصطناعيًا يُدعى C3‑DLL4، صُمّم بأدوات حسابية. هذا الجزيء القابل للذوبان يُرتب ثلاث نسخ من مجال الإشارة DLL4 في هيكل ثلاثي الصُّلب، مما يسمح له بتجميع وتنشيط مستقبلات Notch على الخلايا المجاورة بطريقة تشبه تأثير الخلية المجاورة الطبيعية. في خطوط الخلايا المبلّغة بالمؤشرات، فعّل C3‑DLL4 بقوة الجينات التابعة لـNotch. عند إضافته إلى عضويات الأميلوبلاست المبكرة—عناقيد خلوية ثلاثية الأبعاد مزروعة من الخلايا الجذعية—حفز تحولًا واسعًا في النشاط الجيني. انتقلت العضويات من ملف غير ناضج إلى ملف يطابق الأميلوبلاستات الإفرازية والناضجة تمامًا، حيث شغلت جينات مميزة مثل AMELX وENAM وMMP20 وODAM وKLK4 وTUFT1 وWDR72. كان تعطيل نشاط Notch له التأثير المعاكس، مع توقف النضج وتعطّل إنتاج بروتينات المينا.
من العضويات إلى نسيج شبيه بالمينا
لافت للنظر، عندما نُقلت عضويات الأميلوبلاست المنشَّطة بـNotch وزُرعت تحت كبسولة الكلية في فئران ناقصة المناعة—موقع آمن ومزوّد جيدًا يُستخدم غالبًا لاختبار الأنسجة البشرية—بدأت تلك العضويات في ترسيب مادة كثيفة ومعدنية. أكدت صور الميكرو‑CT عالية الدقة وتقنيات تلوين العظام التقليدية وجود عقيدات متكلسة حيث لا يوجد مثل هذا النسيج عادة. أظهرت الميكروسكوبات طبقات منظمة ومستقطبة من خلايا بشرية تعبّر عن بروتينات المينا الرئيسية وWDR72، وهو عامل مرتبط بتمعدن المينا السليم. وعلى الرغم من أن هذه المادة تُوصف بشكل أدق بأنها «شبيهة بالمينا» وليست مينا طبيعية تمامًا، فإنها تُظهر أن الأميلوبلاستات البشرية المهندَسة قادرة، من حيث المبدأ، على ترسيب معدن صلب داخل جسم حي. 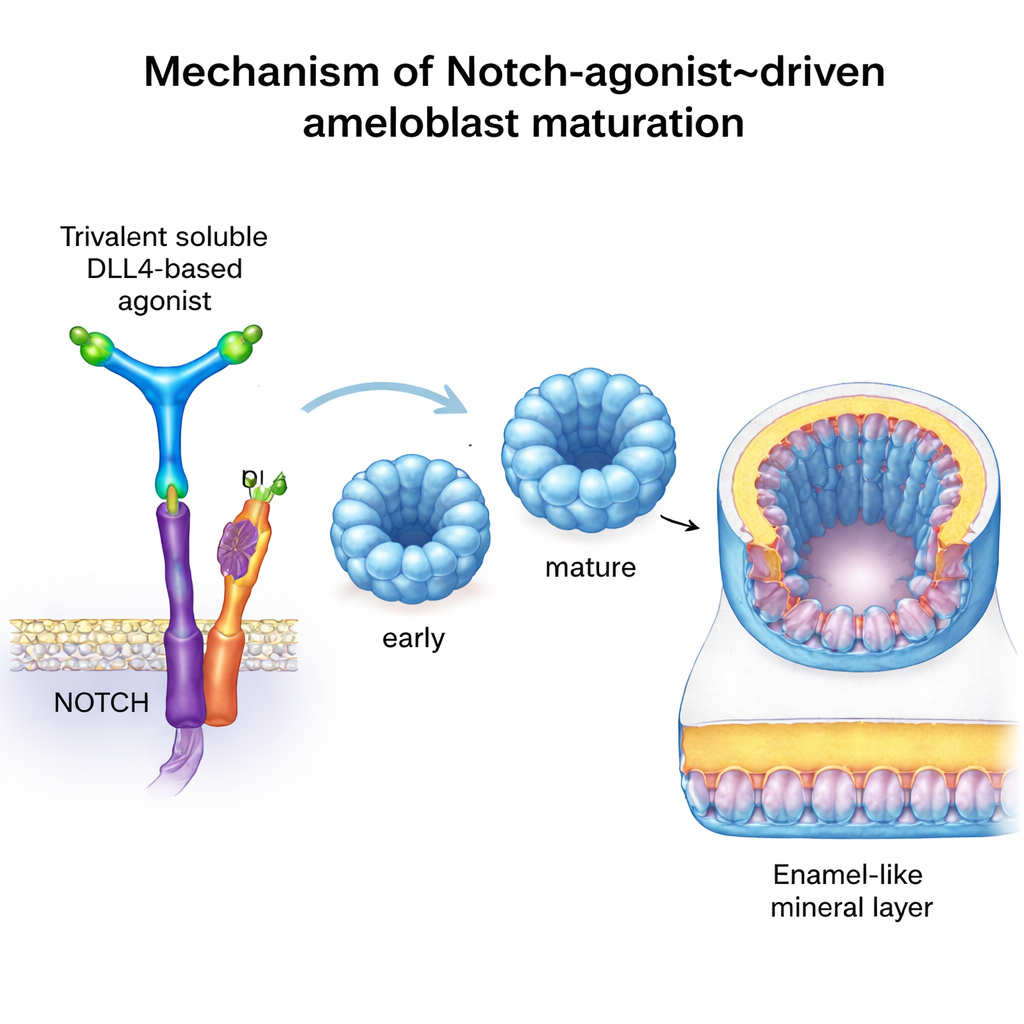
حل لغز جيني وراء ضعف المينا
تناولت الدراسة أيضًا لغزًا طويل الأمد حول جين يُدعى DLX3، التي تُسبب طفراته أنواعًا معينة من عيوب المينا الموروثة وتزيد من خطر التسوس. ينشط DLX3 في كل من الأميلوبلاستات والأودونتوبلاستات، مما يجعل من الصعب تحديد نوع الخلايا المتضرر عندما تحدث مشكلة. باستخدام نظام العضويات الخالي من الأودونتوبلاستات والتحرير الجيني بتقنية CRISPR، أزال الباحثون DLX3 تحديدًا في سلالة الأميلوبلاست. استمرت الخطوات المبكرة لتكوين الأميلوبلاست، لكن مرحلة النضج النهائية انهارت: تراجعت بشكل كبير مستويات بروتينات المينا الأساسية مثل إناملين وAMELX وMMP20 وKLK4 وTUFT1 وWDR72 على مستوى الحمض النووي الريبي والبروتين. يظهر ذلك أن DLX3 مطلوب مباشرة داخل الأميلوبلاستات البشرية لإكمال برنامج صنع المينا، مما يساعد على تفسير سبب ارتباط المتغيرات القريبة من هذا الجين بأسنان هشة وعُرضة للتسوس.
ماذا قد يعني هذا لرعاية الأسنان المستقبلية
معًا، ترسم هذه النتائج خارطة طريق خطوة بخطوة من الخلايا الجذعية إلى عضويات منتجة للمينا إلى نسيج شبيه بالمينا في الجسم الحي، يتحكم فيها «مفتاح تشغيل» Notch قابل للضبط وجين DLX3. وعلى الرغم من أن تجديد الأسنان سريريًا ما زال بعيدًا، فإن هذا العمل يوفر أرضية اختبار قوية لفهم أمراض الأسنان الجينية، وفحص علاجات جديدة، وصقل استراتيجيات لإعادة بناء المينا المفقودة بخلايا حية بدلًا من مواد خاملة. للمرضى، الأمل طويل المدى هو أن تكون زيارات طبيب الأسنان يومًا ما فرصة لإصلاح الأسنان البالية أو المتسوسة بمينا حيوية مُهندَسة تتصرف أشبه بالمينا الحقيقية.
الاستشهاد: Patni, A.P., Mout, R., Alghadeer, A. et al. Soluble Notch agonist enables human ameloblast maturation and enamel-like tissue formation for tooth regeneration. Int J Oral Sci 18, 25 (2026). https://doi.org/10.1038/s41368-026-00429-4
الكلمات المفتاحية: تجديد المينا, عضويات الأميلوبلاست, إشارات Notch, DLX3, خلايا جذعية سنّية