Clear Sky Science · ar
تعاونهما Gli2 وGli3 في الوساطة بين إشارة Hedgehog ومسار TGF-β في الخلايا الأولية اللحيمية لتنظيم تكوّن جذور الأسنان
لماذا تهم جذور الأسنان أكثر مما تتوقع
معظمنا لا يفكر في أسنانه إلا عند الألم أو عند رؤيتها في المرآة. لكن ما يثبت كل سن في الفك — الجذر — لا يقل أهمية عن التاج المرئي. تحافظ الجذور الصحية على ثبات الأسنان للقرع والكلام طوال الحياة. يستكشف هذا البحث كيف أن إشارات دقيقة داخل أنسجة الفك تُملي على الخلايا غير الناضجة كيفية بناء جذور أسنان قوية، عملاً يمكن أن يساعد يوماً ما في الوقاية من عيوب الجذر أو إصلاحها التي تؤدي إلى ارتخاء الأسنان وفقدانها.
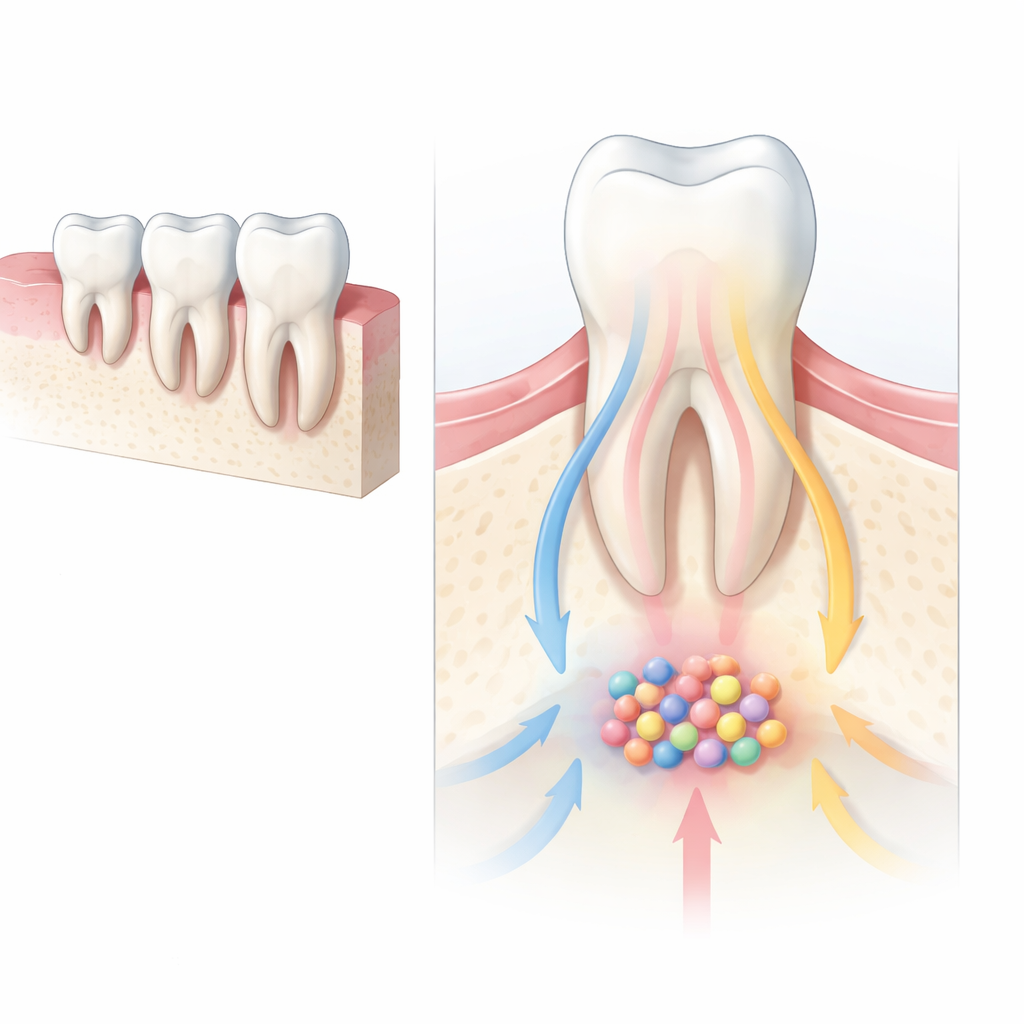
الخلايا السائرة التي تبني وجوهنا
في مراحل مبكرة من التطور، تهاجر مجموعة خاصة من الخلايا تُسمى خلايا القِمّة العصبية القحفية إلى الوجه والفكَّين الناميَين، حيث تتحول إلى عظام وغضاريف وأنسجة داعمة للأسنان. عندما يفشل هذا التحول تحدث تشوهات وجهية وسنية خطيرة عند الولادة. إشارة رئيسية توجه هذه الخلايا هي مسار Hedgehog، الذي يعمل كـ"نظام تحديد مواقع جزيئي" يساعد الخلايا على تقرير أين تذهب وماذا تصبح. ركز الباحثون على بروتينين مساعدين يتحكمان بواسطة Hedgehog، هما Gli2 وGli3، ليفحصوا كيف يوجهان معاً الخلايا التي تبني في نهاية المطاف جذور طواحين الفأر.
مفتاحا جين يعملان كفريق
باستخدام نماذج فئران معدلة بدقة، أوقف الباحثون بشكل انتقائي عمل Gli2 أو Gli3 أو كليهما في مجموعة من الخلايا الأولية المكوِّنة للجذر الموجودة قرب أطراف الجذور النامية. إلغاء Gli2 وحده لم يغير كثيراً من تشكل الجذر، لكن إلغاء Gli3 أدى إلى جذور أقصر ملحوظاً، وتأخر بزوغ الأسنان، وقلة العظم الداعم حول الأسنان. عندما أُزيل كل من Gli2 وGli3 معاً، تفاقمت المشاكل كثيراً: كانت الجذور حوالي نصف طولها الطبيعي، تأخر بزوغ الأسنان، وتناقص العظم الذي يحتضن الجذور بصورة كبيرة. تُظهر هذه التجارب أن Gli2 وGli3 لا يعمَلان بمعزل عن بعضهما؛ بل يتعاونا لتشكيل الجذر وهياكل الدعم المحيطة به.
توجيه الخلايا لتأدية المهام الصحيحة
لفهم سبب فشل الجذور، نظر الفريق عن كثب في المصير الطبيعي للخلايا الأولية المكوِّنة للجذر. في الأسنان السليمة، تتمايز هذه الخلايا إلى أودونتوبلاستات منتجة للعاج داخل الجذر، وخلايا أربطة ليفية تربط الجذر بالعظم، وخلايا مكوِّنة للعظم في التجويف. عندما اختفى Gli3، وخاصة عندما اختفت كل من Gli2 وGli3، تعطلت هذه المسارات: انخفضت مؤشرات هوية العاج والرباط بشكل كبير، وظهرت خلايا مكوِّنة للعظم بالقرب من الجذور بمعدلات أقل. أظهر تتبع نسل هذه الخلايا أن كثيراً منها بقي أعلى في منطقة السن بدلاً من الاستقرار في الجذر ورباطه، ما يشير إلى أن "خيارات مهنهم" الطبيعية قد أعاقت. في الوقت نفسه، انخفض عدد الخلايا المنقسمة في منطقة الجذر، فقلّت اللبنات المتاحة لبناء الجذر.
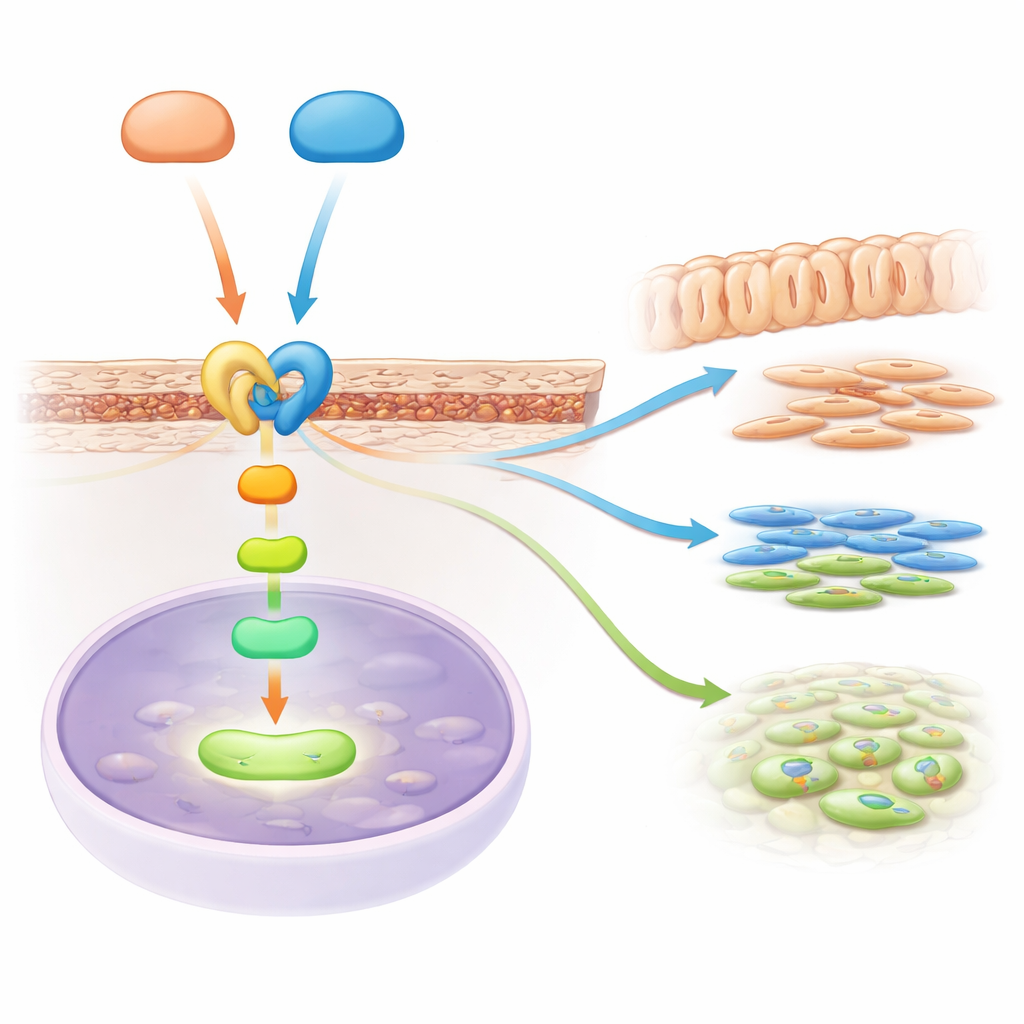
تتابع إشاري يربط مسارين رئيسيين
القصة لم تتوقف عند إشارة Hedgehog. من خلال قراءة الجينات المفتوحة أو المغلقة، اكتشف العلماء أن مساراً رئيسياً آخر، إشارة TGF-β، انخفضت عندما فقدت الخلايا Gli2 وGli3. يعرف عن TGF-β أنه يعزز تكوّن العاج والعظم. حدّد الفريق جزيئاً محورياً في التتابع، مستقبل يُدعى Acvr2b، يستقر على سطح الخلايا الأولية للجذر ويساعد على نقل إشارات عائلة TGF-β إلى داخل الخلية. أظهروا أن كلا من Gli2 وGli3 يرتبطان فيزيائياً بمنطقة التحكم في جين Acvr2b، معززين نشاطه. بدون هذين المساعدين، انخفضت مستويات Acvr2b في منطقة الجذر، وكانت رسائل TGF-β الداخلية أقل نشاطاً، مما أضعف التعليمات التي تحفز نمو الجذر وتمايزه.
إعادة برمجة جزئية لبرنامج بناء الجذر المعيب
لاختبار ما إذا كان إحياء إشارة TGF-β يمكن أن يساعد، عالج الباحثون فئراناً تفتقر إلى كل من Gli2 وGli3 بدواء ينشط هذا المسار. رغم أنه لم يستعد الجذور إلى حالتها الطبيعية بالكامل، فقد أطال العلاج الجذور، وزاد مقدار العظم المحيط، وحسّن تكوّن العاج وأنسجة الرباط مقارنة بالفئران الطافرة غير المعالجة. تشير هذه الإنعاش الجزئي إلى أن سلسلة Gli2/Gli3–Acvr2b–TGF-β هي طريق رئيسي تحول إشارات Hedgehog إلى نمو هيكلي لجذور الأسنان.
ما يعنيه هذا لمستقبل العناية بالأسنان
بعبارة بسيطة، يوضح هذا العمل أن مفتاحيْن جينييْن، Gli2 وGli3، يعملان معاً لمساعدة خلايا الفك الشابة على استقبال إشارات Hedgehog ومن ثم، عبر تتابع يشمل TGF-β، اتخاذ قرار بأن تصبح خلايا متخصصة تبني وتدعم جذور الأسنان. عندما ينهار هذا التواصل، تصبح الجذور قصيرة، وتبزغ الأسنان بشكل سيء، ويصبح العظم الداعم رقيقاً. لا يوضح فهم هذه الشبكة الإشارية كيف تتكوّن جذور الأسنان الطبيعية فحسب، بل يشير أيضاً إلى استراتيجيات جديدة لتوجيه الخلايا الجذعية أو الخلايا الأولية لإصلاح الجذور التالفة أو تجديدها مستقبلاً في العلاجات السنية.
الاستشهاد: Zhou, T., Huang, L., Xie, Y. et al. Gli2 and Gli3 synergistically mediate HH-TGF-β crosstalk in mesenchymal progenitor cells to orchestrate tooth root morphogenesis. Int J Oral Sci 18, 30 (2026). https://doi.org/10.1038/s41368-026-00427-6
الكلمات المفتاحية: تطور جذر السن, خلايا القِمَّة العصبية القحفية, إشارة Hedgehog, مسار TGF-β, خلايا جذعية سنية