Clear Sky Science · ar
خريطة نسخية خلوية مفردة تكشف آليات تواصل مميزة بين المناعة والخلايا الغضروفية في التهاب مفصل الفك الصدغي التنكسي الناجم عن أنواع مختلفة من اضطراب الإطباق
لماذا يهم مفصل فكك
المفاصل الصغيرة أمام أذنيك، المسماة مفاصل الفك الصدغي (TMJs)، تتيح لك التحدث والمضغ والتثاؤب والضحك. عندما تصاب بالتهاب مفصلي تنكسي، قد تصبح الحركات اليومية مؤلمة وصعبة. تستخدم هذه الدراسة تحليل الجينات الخلوي المفرد المتقدم في الفئران لفحص هذه المفاصل خلية بخلية، كاشفة كيف تؤدي مشاكل الإطباق المختلفة إلى أنواع مختلفة من الضرر — وكيف قد يوجّه ذلك علاجات أكثر دقة.
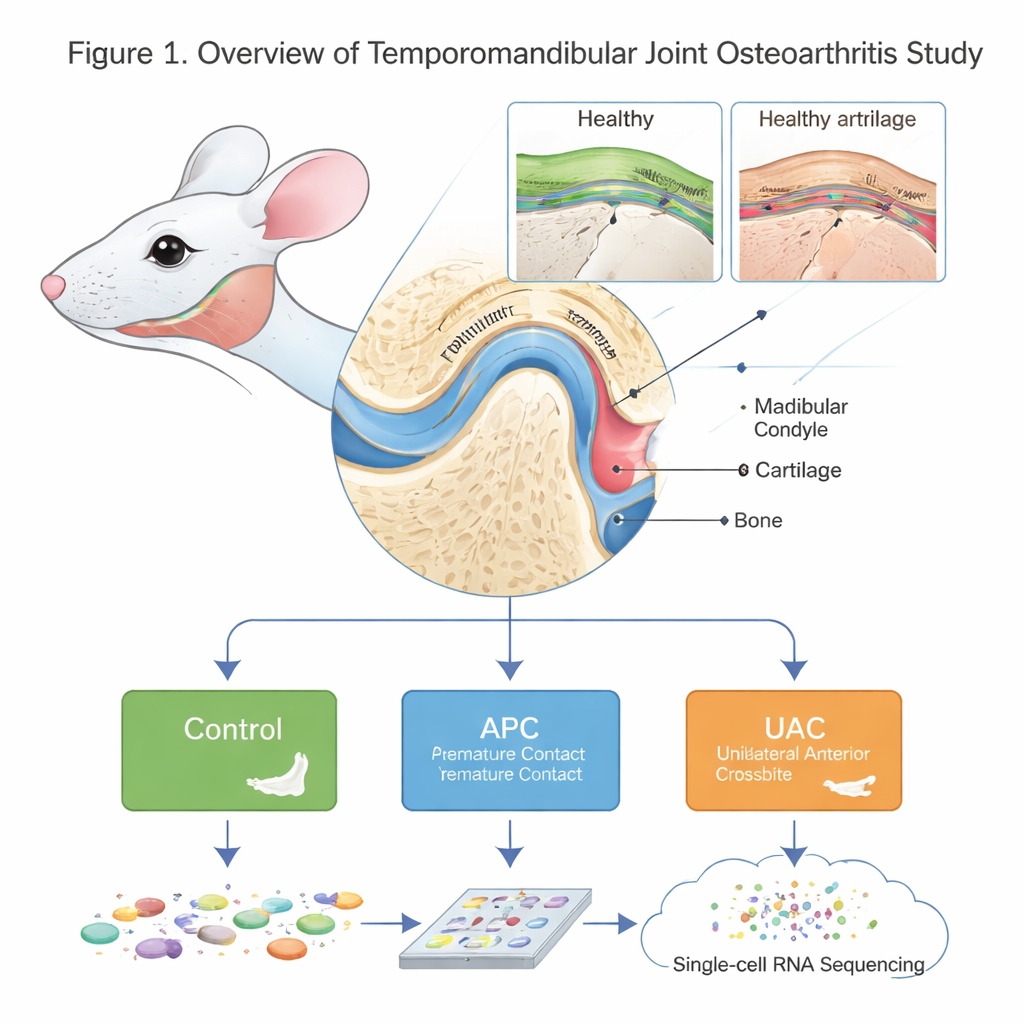
النظر عن كثب إلى مفصل صغير لكنه معقَّد
المفصل الصدغي الفكي ليس مفصلاً بسيطاً. طرفه المدور، الحدبة الفكية، مغطى بنوع خاص من الغضروف ومدعوم بالعظم تحته. يسبب التهاب المفصل التنكسي في هذا المفصل (TMJOA) ألماً وتيبّساً وفقدان وظيفة، لكن أسبابه المجهرية والجزيئية كانت صعبة التفكيك. أنشأ الباحثون «خريطة خلوية» مفصّلة لحدبة الفك عند الفئران في الحالة الصحية والمرَضية باستخدام تسلسل الحمض النووي الريبي الخلوي المفرد، وهي تقنية تقرأ أي الجينات نشطة في آلاف الخلايا الفردية. قارَنوا الفئران السليمة بنموذجين لعدم توازن الإطباق — التماس السابق الأمامي المبكر (APC)، حيث تلتقي الأسنان الأمامية مبكراً جداً، والعضة المتقاطعة الأمامية الأحادية الجانب (UAC)، حيث تعض جهة واحدة من الأسنان الأمامية بطريقة خاطئة — وكلاهما معروف بأنه يحمّل المفصل بشكل زائد.
أنواع كثيرة من خلايا الغضروف، ليست واحدة فقط
تقليدياً، وُصِف غضروف الحدبة بطبقات عامة — خلايا متكاثرة وناضجة وتضخمية. تُظهر هذه الدراسة أن الصورة الحقيقية أكثر تنوعاً بكثير. حدَّد الفريق عدة أنواع فرعية من الخلايا الغضروفية، كلٌ منها بنمط نشاط جيني ودور محتمل خاص به. وُجدت خلايا جذعية قرب السطح تتصرف كمخزون إصلاحي، وخلايا غضروفية ليفية مشاركة في مصفوفة تشبه الندبة والشفاء، وخلايا مرتبطة بالالتهاب تُنتج إشارات التهابية، وخلايا مرتبطة بالتَكلُّس والتضخُّم التي تساعد على تحويل الغضروف إلى عظم، وخلايا إصلاحية تُخفف الضغط والالتهاب. في المفاصل السليمة، تتواجد هذه الأنواع الفرعية بنمط مكاني منتظم وتتبع مساراً تطورياً سلساً من الخلايا الجذعية إلى حالات أكثر نضجاً.
عندما تخلّ مشاكل الإطباق بترتيب الخلايا في المفصل
أدى كلا النموذجين APC وUAC إلى ترقّق الغضروف وخشونة السطح وآفات تشبه التهاب المفاصل التنكسي في الحدبة. على المستوى الخلوي، انخفضت نسبة الخلايا الغضروفية بينما ارتفعت الخلايا المناعية. في نموذج APC، حدثت زيادة كبيرة في أنواع معينة من الخلايا الغضروفية المتكلسة والتضخمية واضطر الانسداد الطبيعي للتقدّم من الخلايا الجذعية إلى الخلايا الناضجة. في UAC، لوحظ أيضاً ازدياد في الخلايا الغضروفية الليفية والإصلاحية، مما يوحي بمحاولة أقوى للإصلاح وإعادة التشكيل. أكدت الميكروسكوبيّة أن الخلايا فقدت طبقاتها المنظمة وأصبحت مضغوطة وغير منظّمة في الغضروف المريض، وهو ما يتطابق مع مسارات التطور المضطربة المُستنتجة من بيانات التعبير الجيني.
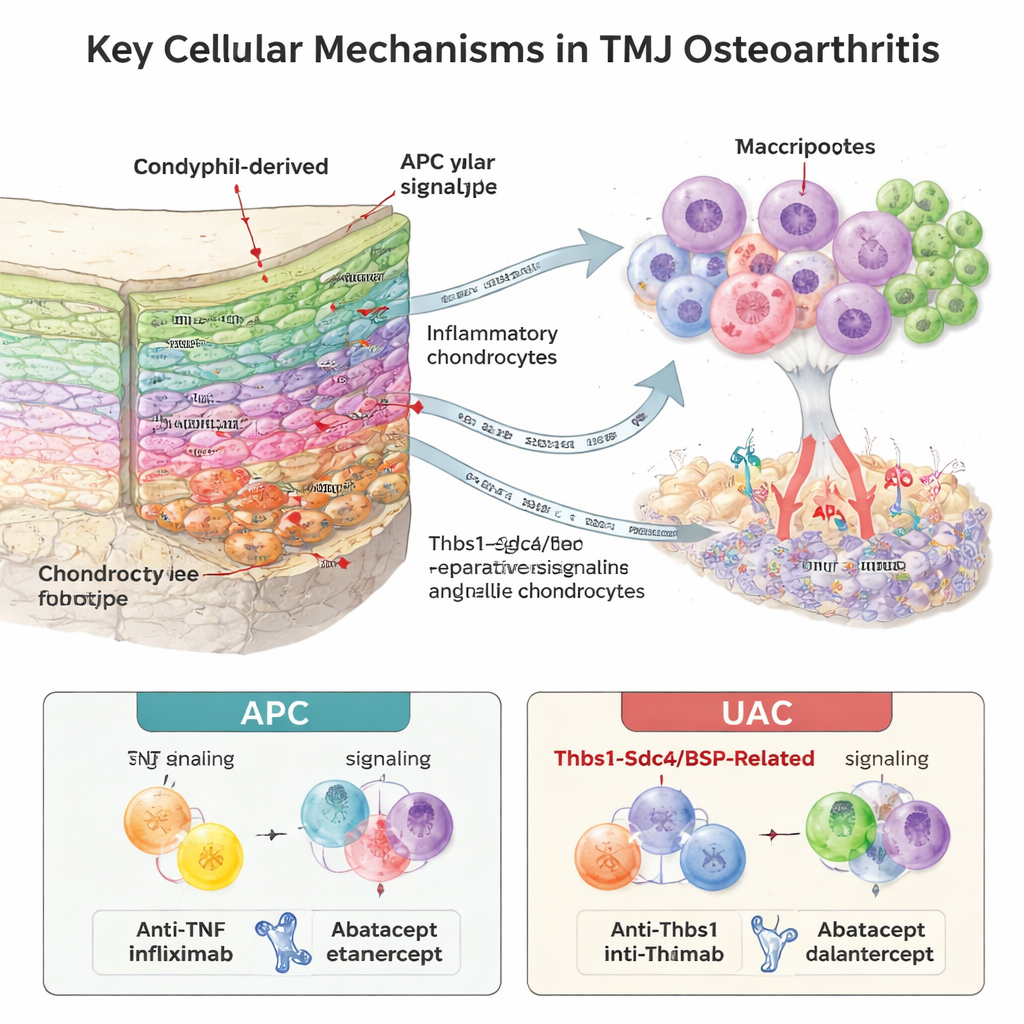
الخلايا المناعية والأوعية الدموية والغضروف تتبادل الكلام
احتوى العظم والنخاع الداعم للحدبة على «بيئة مجهرية» مناعية غنية بشكل مفاجئ. وجد الباحثون تسعة أنواع من الخلايا المناعية، مع توسع قوي في العدلات (خلية بيضاء سريعة الاستجابة) في المفاصل المريضة، خصوصاً مرحلة نضجية محددة. من خلال تحليل الجزيئات الإشارية والمستقبلات التي تُعبر معاً، استنتجوا وجود «تواصل» مكثف بين الخلايا المناعية والخلايا الغضروفية. في نموذج APC أصبحت العدلات المصدر الرئيسي لعامل النخر الورمي ألفا (TNF‑alpha)، إشارة التهابية قوية أرسلت رسائل ضارّة إلى خلايا الغضروف. في نموذج UAC ظهر نمط مختلف: كانت الإشارات المرتبطة بالعظم والغضروف التي تشمل بروتين سيلكون العظم (BSP) ومسار Thbs1–Sdc4 أكثر بروزاً، وكانت هذه مرتبطة ارتباطاً وثيقاً بنمو أوعية دموية جديدة عند حدود الغضروف‑العظم. تداخلت المناطق الغنية بـBSP مع علامات تكوّن الأوعية، مشيرة إلى أن الأوعية الغازية والخلايا المناعية المستدعاة تقود معاً تآكل الغضروف.
علاجات مخصّصة لإجهادات مفصلية مختلفة
لاختبار ما إذا كانت هذه الإشارات المميزة مهمة فعلاً، عالج الفريق الفئران أثناء تطور المرض بأدوية تحجب مسارات محددة. في التهاب المفصل التنكسي الناجم عن APC حمى حجب TNF‑alpha باستخدام الدواء إيتانرسبت (etanercept) الغضروف بوضوح، بينما لم يحدث اختلاف كبير مع دواء يستهدف مستقبلات جذب العدلات (Navarixin). على النقيض، في التهاب المفصل الناجم عن UAC خفف Navarixin بشكل كبير من تلف الغضروف، متسقاً مع عملية مرضية تعتمد أكثر على غزو الأوعية وإعادة التشكيل المدفوعة بالعدلات، بينما كان لإيتانرسبت تأثير أضعف. تشير هذه النتائج إلى أن التهاب مفصل الفك الصدغي التنكسي ليس مرضاً واحداً بل مجموعة من الحالات المرتبطة بكيفية تعرض المفصل للإجهاد، وأن العلاجات الفعّالة قد تحتاج إلى التكيّف مع الأنماط الميكانيكية والخلوية الخاصة بكل مريض.
ماذا يعني هذا للأشخاص المصابين بألم الفك
بالنسبة لشخص يعاني من طقطقة الفك أو ألم أو صعوبة في الفتح، تؤكد هذه الدراسة فكرتين رئيسيتين. أولاً، يُحافظ على المفصل عبر مجتمع متنوع من الخلايا الغضروفية والمناعية التي قد تحمي النسيج أو تضرّه تبعاً لكيفية تفعيلها. ثانياً، قد تدفع مشاكل الإطباق المختلفة هذا المجتمع إلى مسارات ضارة مميزة — واحدة مدفوعة بالالتهاب التقليدي، وأخرى مدفوعة بنمو أوعية دموية غير طبيعي وإعادة تشكيل العظم‑الغضروف. على المدى الطويل، قد يساعد هذا النوع من الخرائط الخلوية المفردة أطباء الأسنان والأطباء على تخطي العلاجات ذات المبدأ الواحد نحو نهج يجمع بين تصحيح الإطباق وأدوية موجهة تُختار وفق نمط التلف المفصلي الخاص بالمريض.
الاستشهاد: Wang, K., Li, Y., Xiang, S. et al. Single-cell transcriptional atlas reveals distinct immune-chondrocyte crosstalk mechanisms in temporomandibular joint osteoarthritis induced by different types of occlusal disorder. Int J Oral Sci 18, 22 (2026). https://doi.org/10.1038/s41368-025-00424-1
الكلمات المفتاحية: التهاب مفصل الفك الصدغي التنكسي, تسلسل الحمض النووي الريبي خلوي مفرد, الخلايا الغضروفية, العدلات, اضطراب الإطباق